Las inyecciones locales de glucocorticoides son frecuentemente utilizadas en el tratamiento del síndrome de pinzamiento subacromial (SPSA); sin embargo, su eficacia es aún motivo de controversia.
ObjetivoComparar la eficacia de la inyección subacromial de metilprednisolona más lidocaína contra lidocaína sola en el tratamiento del SPSA.
Material y métodoSe incluyó a pacientes con SPSA definido por un resultado positivo en la prueba de la inyección de Neer, quienes fueron aleatorizados para recibir una inyección de 2 ml (40 mg/ml) de acetato de metilprednisolona más 1 ml de lidocaína al 1% (27 sujetos) o 3 ml de lidocaína al 1% (29 sujetos). Se comparó el cambio desde la línea basal en la calificación de una versión validada al español del Shoulder Disability Questionnaire (S-SDQ) de la intensidad del dolor y de los arcos de movilidad a los 15 y 30 días, y luego cada mes por 5 meses más.
ResultadosEl análisis mediante un modelo general lineal con ajuste para el tiempo de evolución y la intensidad del dolor en la línea basal no detectó diferencias en el cambio de la calificación S-SDQ y los arcos de movilidad entre los grupos de estudio en ningún momento del seguimiento. El grupo de lidocaína sola presentó mayor disminución en la intensidad del dolor durante todo el seguimiento.
ConclusionesLa inyección subacromial de acetato de metilprednisolona no fue más eficaz que la inyección de lidocaína sola en pacientes con SPSA.
Local glucocorticosteroid injections are frequently used in the treatment of subacromial impingement syndrome (SIS), however its efficacy is still controversial.
ObjectiveTo compare the efficacy of the subacromial injection of methylprenisolone acetate plus lidocaine (MPL) versus lidocaine alone (LA) in SIS.
Material and methodConsecutive SIS subjects, defined as a positive Neer’s injection test were randomized to a subacromial injection of 2 mL methylprednisolone acetate (40 mg/mL) plus 1 mL of 1% lidocaine (27 patients); or 3 mL of 1% lidocaine (29 patients) were studied. The change from baseline of the score of a Spanish validated version of the Shoulder Disability Questionnaire (S-SDQ), pain intensity, and shoulder range of motion were measured at 15 and 30 days, and afterward every month for five months.
ResultsAfter adjusting for duration of symptoms and pain intensity at baseline by way of a general lineal model,we did not find differences in the change of S-SDQ scores and shoulder range of motion between the study groups. Subjects randomized to LA had greater improvement of pain intensity than MPL subjects during the entire follow-up.
ConclusionsA subacromial injection of methylprednisolone acetate was not more efficacious than the injection of lydocaine alone in patients with SIS.
El dolor de hombro es una causa frecuente de búsqueda de atención médica, su prevalencia se ha establecido en 20% en la población general1. La tendinopatía del manguito de los rotadores es la causa más frecuente de hombro doloroso, y el síndrome de pinzamiento subacromial (SPSA), una tendinopatía angiofibroblástica producida por el machacamiento del manguito de los rotadores en el estrecho coracoacromiohumeral, es la causa más común de tendinopatía del manguito de los rotadores2–4.
El enfoque terapéutico conservador basado en fisioterapia, rehabilitación y fármacos antiinflamatorios no esteroideos puede no ser exitoso en una significativa proporción de los pacientes con SPSA, cuando esto sucede, una inyección local de glucocorticoides en el espacio subacromial es una intervención terapéutica frecuentemente empleada3,4. Sin embargo, la eficacia de esta modalidad terapéutica es aún materia de controversia5–8. Recientemente, Koester et al9, después de realizar una revisión sistemática sobre el tópico, concluyeron que hasta el momento hay poca evidencia reproducible para apoyar la eficacia de la inyección subacromial de glucocorticoides en el manejo de los pacientes con SPSA. Por estos motivos, usando una versión validada al español del Shoulder Disability Questionnaire10 como la variable de respuesta primaria, decidimos realizar un ensayo clínico controlado, aleatorizado, doble ciego, para evaluar la eficacia de la inyección de acetato de metilprednisolona más lidocaína en el espacio subacromial, en comparación con la inyección de lidocaína sola en el tratamiento de pacientes con SPSA que no han respondido a antiinflamatorios no esteroideos.
Material y métodoPacientesEntre febrero de 2002 y diciembre de 2003, cada paciente con sospecha clínica de SPSA referido a los servicios de Ortopedia y Reumatología del Hospital de Especialidades del Centro Médico Nacional Ignacio García Téllez del Instituto Mexicano del Seguro Social en Mérida, Yucatán, México, fue invitado a participar en el estudio. Los criterios de inclusión fueron: edad de 18 años o más, hombro doloroso de más de 7 días de duración que no hubiese respondido a antiinflamatorios no esteroideos y el diagnóstico de SPSA definido por el cumplimiento de los criterios para tendinitis del manguito de los rotadores del grupo de Southampton11 y un resultado positivo después de la realización de la prueba de Neer de la inyección subacromial de lidocaína12,13. Los criterios de exclusión fueron: tener acromion en gancho, osteofito de la articulación acromioclavicular o depósito cálcico en la región subacromial presentes en una radiografía anteroposterior del hombro; sujetos con historia de alergia a lidocaína, la presencia de cualquier enfermedad reumática inflamatoria sistémica o de hipertensión arterial o diabetes no controladas.
MedicionesLa medida de respuesta primaria fue el cambio desde la línea basal en la calificación de una versión validada al español del Shoulder Disability Questionnaire (S-SDQ)10,14, en esta escala una mayor puntuación significa mayor limitación funcional. Las medidas de respuesta secundarias fueron el cambio en la intensidad del dolor evaluada mediante una escala basal analógica de 100mm y en las medidas goniométricas de los arcos de movilidad del hombro.
MétodosLos pacientes fueron captados por un investigador (ABP), quien realizó la prueba de la inyección de Neer y registró los datos en la línea basal. Tres días más tarde, los sujetos que cumplieron criterios de elegibilidad y aceptaron participar en el estudio fueron asignados por sorteo para recibir, mediante una vía de abordaje lateral, una inyección en el espacio subacromial, ya sea una mezcla de 2ml de una suspensión de acetato de metilprednisolona (40mg/ml) más 1ml de lidocaína al 1% o 3ml de lidocaína al 1%, que lo realizó otro investigador (JAN) que estaba cegado a los valores del estado basal. La secuencia de asignación de tratamientos fue generada en el módulo de aleatorización del programa estadístico True Epistat. Se aseguró el cegamiento del tratamiento recibido por los pacientes. Después de esta intervención, todos los pacientes se sometieron a un programa estándar de fisioterapia y rehabilitación proporcionado por otro investigador (JRP), el uso de medicamentos antiinflamatorios fue continuado de acuerdo con los requerimientos de cada paciente. Se permitió el uso de analgésicos simples como única terapia de rescate en caso de dolor intenso. Las mediciones del S-SDQ, la intensidad del dolor y los arcos de movilidad del hombro fueron realizadas a los 15 y a los 30 días de las inyecciones de tratamiento, y luego, cada mes por 5 meses más por un investigador (ABP), quien estaba cegado al tratamiento recibido.
Aspectos éticosEl protocolo fue aprobado por el Comité Local de Investigación de la unidad donde se realizó el estudio. Todos los pacientes firmaron una carta de consentimiento informado antes de ingresar en el estudio.
Análisis estadísticoSe usó un modelo general lineal para comparar el cambio en la calificación del S-SDQ, la intensidad del dolor y los arcos de movilidad de hombro entre los grupos de tratamiento. Debido a que en el tiempo basal tanto la duración de los síntomas antes del ingreso al estudio como la intensidad del dolor fueron diferentes entre los grupos de estudio, ambas características se incluyeron como covariables en el modelo antes citado. La significación estadística se estableció en 0,05. Los datos se almacenaron y se analizaron con el programa estadístico SPSS para Windows (versión 11.5).
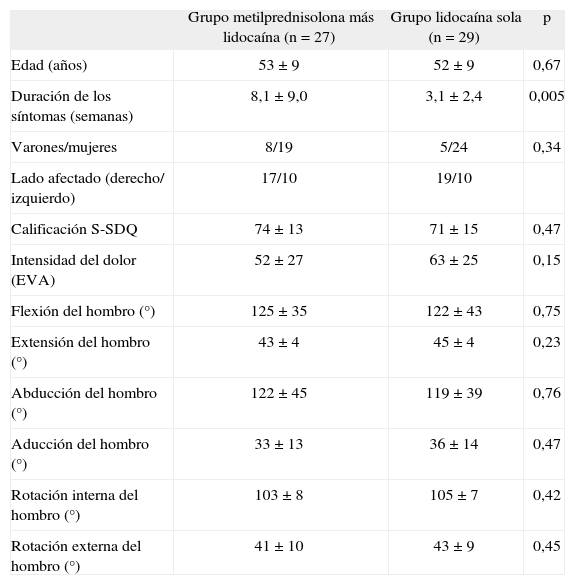
ResultadosCaracterísticas clínicas y demográficas en la línea basal Se incluyó un total de 56 pacientes; 27 fueron asignados a metilprednisolona más lidocaína y 29 a lidocaína sola. La mayoría de las variables clínicas y demográficas fueron equiparables entre los grupos de estudio al inicio del seguimiento; sin embargo, la duración de los síntomas antes del ingreso en el estudio fue significativamente mayor en el grupo de pacientes que recibió metilprednisolona. Adicionalmente, el grupo de pacientes que recibió lidocaína sola presentó una marcada tendencia hacia una mayor intensidad del dolor en la línea basal (tabla 1).
Características clínicas y demográficas al inicio del estudio
| Grupo metilprednisolona más lidocaína (n = 27) | Grupo lidocaína sola (n = 29) | p | |
| Edad (años) | 53 ± 9 | 52 ± 9 | 0,67 |
| Duración de los síntomas (semanas) | 8,1± 9,0 | 3,1 ± 2,4 | 0,005 |
| Varones/mujeres | 8/19 | 5/24 | 0,34 |
| Lado afectado (derecho/ izquierdo) | 17/10 | 19/10 | |
| Calificación S-SDQ | 74 ± 13 | 71 ± 15 | 0,47 |
| Intensidad del dolor (EVA) | 52 ± 27 | 63 ± 25 | 0,15 |
| Flexión del hombro (°) | 125 ± 35 | 122 ± 43 | 0,75 |
| Extensión del hombro (°) | 43 ± 4 | 45 ± 4 | 0,23 |
| Abducción del hombro (°) | 122 ± 45 | 119 ± 39 | 0,76 |
| Aducción del hombro (°) | 33 ± 13 | 36 ± 14 | 0,47 |
| Rotación interna del hombro (°) | 103 ± 8 | 105 ± 7 | 0,42 |
| Rotación externa del hombro (°) | 41 ± 10 | 43 ± 9 | 0,45 |
Los datos se presentan como número o media ± desviación estándar.
EVA: escala analógica visual de 0–100mm; S-SDQ: Shoulder Disability Questionnaire.
Más del 80% de los pacientes en ambos grupos completaron más de 3 meses de seguimiento. Después de ello, la tasa de pérdida de pacientes en ambos grupos excedió el 20%. Sólo 15 (55,6%) pacientes en el grupo de metilprednisolona y 17 (58,6%) del grupo de lidocaína sola completaron los 6 meses de seguimiento. No hubo diferencias en el tiempo de seguimiento promedio entre los grupos de estudio: grupo metilprednisolona, 4,7 ± 1,7 meses; grupo lidocaína sola, 4,7 ± 1,7 meses (p = 0,96). A excepción del intervalo de abducción, que fue mayor en el grupo de pacientes que terminaron los 6 meses de seguimiento (132° ± 46° frente a 105° ± 31°; p = 0,01), no hubo diferencias significativas en las demás características clínicas y demográficas al inicio del estudio entre los pacientes que finalizaron el seguimiento y los que no lo hicieron.
Efectos adversosUn paciente del grupo metilprednisolona tuvo dolor intenso después de la inyección. El dolor duró aproximadamente 2h y fue controlado con una dosis oral de dextropropoxifeno. No se detectaron otros efectos adversos.
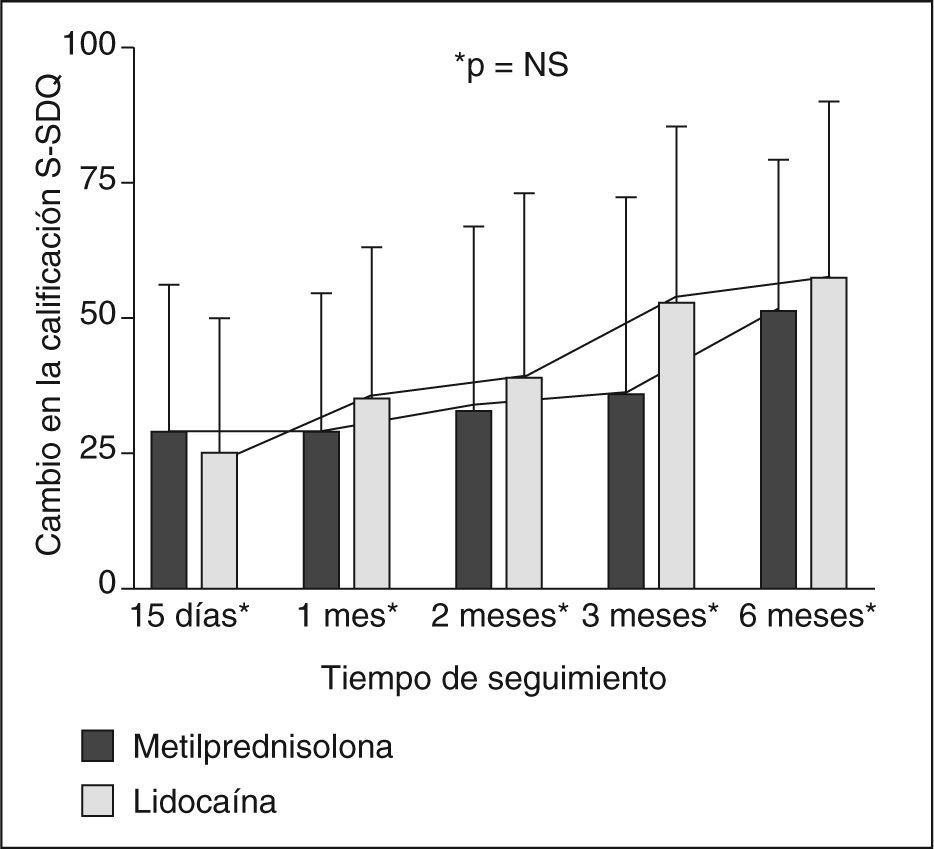
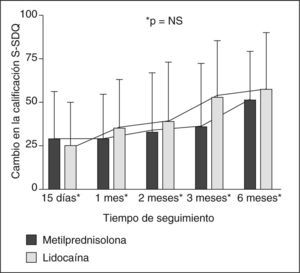
Cambios en la calificación del S-SDQUna tendencia para un mayor grado de mejoría funcional fue apreciable en el grupo de lidocaína sola a partir del primer mes de seguimiento. Sin embargo, esto no alcanzó significación estadística en ninguna de las evaluaciones (fig. 1).
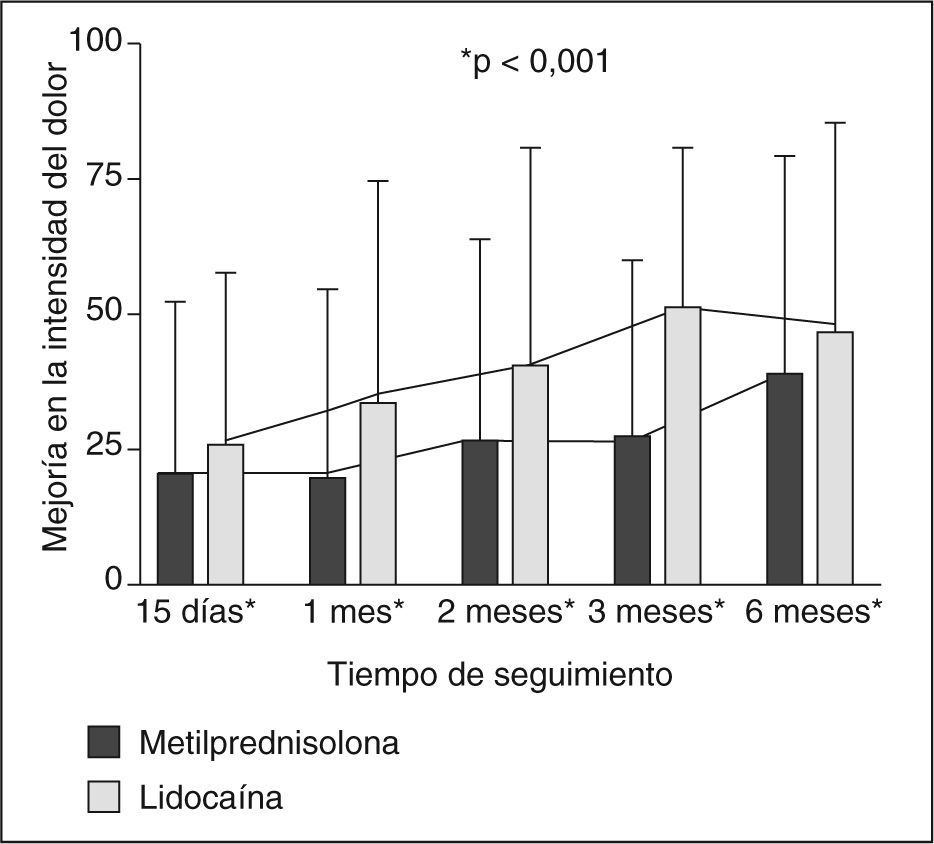
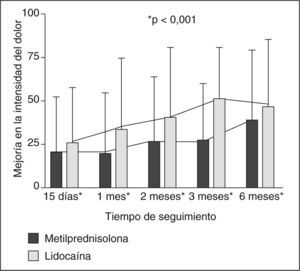
Cambio en la intensidad del dolorEn todas las evaluaciones, los sujetos asignados a lidocaína sola tuvieron una mayor disminución en la intensidad del dolor en comparación con el grupo que recibió metilprednisolona (fig. 2).
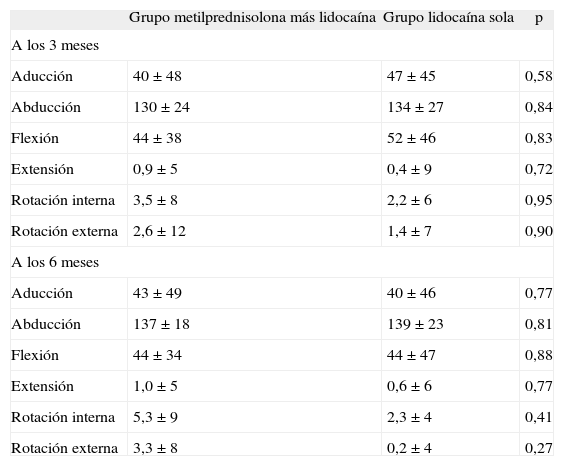
Cambio en los arcos de movilidadNo se detectaron diferencias entre los grupos de estudio en el cambio en los arcos de movilidad del hombro a los 3 y los 6 meses de seguimiento (tabla 2).
Comparación del cambio (en grados) de los arcos de movilidad del hombro durante el estudio
| Grupo metilprednisolona más lidocaína | Grupo lidocaína sola | p | |
| A los 3 meses | |||
| Aducción | 40 ± 48 | 47 ± 45 | 0,58 |
| Abducción | 130 ± 24 | 134 ± 27 | 0,84 |
| Flexión | 44 ± 38 | 52 ± 46 | 0,83 |
| Extensión | 0,9 ± 5 | 0,4 ± 9 | 0,72 |
| Rotación interna | 3,5 ± 8 | 2,2 ± 6 | 0,95 |
| Rotación externa | 2,6 ± 12 | 1,4 ± 7 | 0,90 |
| A los 6 meses | |||
| Aducción | 43 ± 49 | 40 ± 46 | 0,77 |
| Abducción | 137 ± 18 | 139 ± 23 | 0,81 |
| Flexión | 44 ± 34 | 44 ± 47 | 0,88 |
| Extensión | 1,0 ± 5 | 0,6 ± 6 | 0,77 |
| Rotación interna | 5,3 ± 9 | 2,3 ± 4 | 0,41 |
| Rotación externa | 3,3 ± 8 | 0,2 ± 4 | 0,27 |
Los datos reflejan la media ± desviación estándar.
Nuestros resultados, derivados de un ensayo clínico, aleatorizado, a doble ciego, mostraron que una inyección subacromial local de una mezcla de metilprednisolona más lidocaína no fue más eficaz que la inyección de lidocaína sola en pacientes con SPSA. Un efecto terapéutico de las cointervenciones usadas (fisioterapia y antiinflamatorios) no se puede excluir como explicación para estos resultados. Sin embargo, debido a que estas cointervenciones son medidas estándar recomendadas por el consenso de expertos para el tratamiento del SPSA, eliminarlas del protocolo de tratamiento fue considerado como antiético por nuestro grupo. De manera no esperada, los sujetos que recibieron lidocaína sola tuvieron mayor reducción en la intensidad del dolor que los asignados a metilprednisolona durante todo el tiempo de seguimiento.
Reconocemos que nuestros resultados deben ser tomados con cautela debido a varias limitaciones de nuestro estudio, como la elevada proporción de pérdida de pacientes, la aplicación de las inyecciones sin guía ultrasonográfica y la ausencia de estudios de imagen tanto ultrasonográfica como de resonancia magnética (RM) en la evaluación diagnóstica de nuestros pacientes. Relacionado con este último punto, creemos necesario comentar que, aunque de acuerdo con el consenso de expertos la prueba de la inyección subacromial de lidocaína es el estándar para el diagnóstico del SPSA4, en especial para propósitos de investigación, en el contexto de diagnóstico clínico individual de la práctica clínica cotidiana las nuevas técnicas de imagen, como la RM o el ultrasonido, han permitido incrementar la eficacia para el diagnóstico del síndrome, en especial en situaciones de incertidumbre diagnóstica, o para la evaluación de la presencia y la magnitud de disrupción tendinosa. En tales casos, la imagen por RM ha mostrado tener adecuadas sensibilidad y especificidad, aunque su alto costo y la disminución de su rendimiento en casos de desgarros parciales o tendinopatía aislada son limitaciones establecidas15,16. La imagen por ultrasonido de alta resolución, cuando es realizada por un operador eficiente, es una alternativa de bajo costo con indicaciones y exactitud diagnóstica similares a las de la RM17,18. De manera adicional, comunicaciones recientes han indicado que la guía ultrasonográfica para colocación de la inyección de glucocorticoides podría mejorar el resultado clínico de los pacientes con afección de la región subacromial19.
Frecuentemente se ofrece a los pacientes con dolor de hombro las inyecciones locales de glucocorticoides; sin embargo, a pesar del gran número de comunicaciones dedicadas al tema, su eficacia no está aún bien establecida debido a que sólo un pequeño número de estas comunicaciones cumplen con los requerimientos mínimos para considerarlas como evidencia científica sólida, o bien sus conclusiones son contradictorias5,7,20. Green et al5,6 han realizado una serie de revisiones sistemáticas sobre las intervenciones terapéuticas para hombro doloroso y han concluido que la inyección subacromial de glucocorticoides, en comparación con placebo, resulta sólo en una ligera mejoría en la abducción del hombro, mientras que no detectaron diferencias cuando compararon las inyecciones de glucocorticoides contra el tratamiento con antiinflamatorios no esteroideos. Conclusiones similares encontramos en revisiones sistemáticas posteriores7–9. Algunos informes más recientes, realizados en atención médica primaria han indicado que las inyecciones de glucocorticoides son más eficaces que la fisioterapia o la manipulación solamente a corto plazo. Después de un seguimiento prolongado, las diferencias entre los grupos de tratamiento se vuelven inapreciables21–25.
Sólo en un pequeño número de ensayos clínicos se ha estudiado específicamente la eficacia de la inyección de glucocorticoides en SPSA. Blair et al26 realizaron un estudio a doble ciego de 26 semanas de seguimiento, en el que compararon la inyección de 80mg de acetónido de triamcinolona contra la inyección de lidocaína en 40 pacientes con desgarro del manguito rotador detectado por estudio de RM y evaluaron la función del hombro mediante una escala no validada, la intensidad del dolor mediante una escala Likert y los arcos de movilidad. Al final del seguimiento los sujetos que recibieron triamcinolona presentaron mejoría significativa tanto en la intensidad del dolor como en la flexión anterior y la rotación externa del hombro, pero no encontraron diferencias en el estado funcional. Plafki et al27 comunicaron que 19/40 sujetos con SPSA, diagnosticados por una maniobra positiva de Neer o Hawkins, quienes habían recibido una inyección de glucocorticoides, tuvieron una "respuesta favorable", en comparación con 0/10 pacientes que habían recibido una inyección de anestésico local. Por el contrario, Akgun et al28, en un estudio de 3 meses de seguimiento en sujetos con una sólida definición de SPSA, en quienes evaluaron la capacidad funcional del hombro mediante una escala funcional validada, encontraron que la inyección de glucocorticoide resultó solamente en una mejoría a corto plazo, en comparación con inyección local de lidocaína. Finalmente, Alvarez et al29, quienes usaron también una sólida definición de caso para SPSA, no encontraron diferencias en 3 escalas funcionales del hombro y en los arcos de movilidad después de 24 semanas de seguimiento entre los pacientes que recibieron una inyección de glucocorticoides y los que recibieron lidocaína.
Consideramos que nuestros resultados son concordantes con los encontrados en los últimos dos informes debido a que usamos un diseño metodológico parecido que comprendió el uso de la prueba de la inyección de Neer, que es considerada el estándar para el diagnóstico de SPSA, como definición de caso, además de una escala funcional validada (S-SDQ) para evaluar la función del hombro como medida de respuesta primaria.
Concluimos que en pacientes con SPSA, la inyección subacromial de acetato de metilprednisolona no fue más eficaz que la inyección de lidocaína sola. Consideramos que estos resultados podrían ser aplicables solamente a los pacientes que reciben antiinflamatorios no esteroideos y un programa de fisioterapia y rehabilitación como cointervenciones.