Los pacientes con artritis reumatoide (AR) tratados con fármacos modificadores del curso de la enfermedad están expuestos a desarrollar infecciones potencialmente graves como la leishmaniasis. L. infantum es endémica en el Mediterráneo, hecho que obliga ante un paciente con AR que presenta fiebre y pancitopenia, a descartar este proceso. Un diagnóstico de sospecha precoz, puede evitar un curso y pronóstico fatal.
Patients with rheumatoid arthritis (RA) treated with disease-modifying antirheumatic drugs are susceptible to severe infections such as leishmaniasis. As L. infantum is endemic in the Mediterranean region, it is necessary to rule this infectious process out in any RA patient presenting with fever and pancytopenia. An early diagnosis based on a high suspicion can prevent a fatal outcome.
Las infecciones forman parte del espectro de posibles comorbilidades asociadas a la artritis reumatoide (AR) per se, así como las debidas al uso de su tratamiento convencional. Su elevada incidencia ha sido descrita tanto con los glucocorticoides e inmunosupresores, como con el uso de terapias biológicas (TB). Entre los tratamientos, el fármaco más usado en primera línea es el metotrexato (MTX), que permite un mejor control de la enfermedad, aunque no está exento de efectos adversos graves como la toxicidad hematológica, y que pueden aparecer hasta en un 15% de los pacientes con AR1.
Hasta el día de hoy, el espectro de infecciones oportunistas descritas es muy amplio y va desde primo-infecciones por Nocardia o Pneumocystis carinii, infecciones por hongos como Cándida, Aspergillus, Cryptococcus o Histoplasma e infecciones virales, principalmente por herpes zóster. Sorprendentemente, aunque están descritos, son escasos los casos de infección por Leishmania2–4. Dada la baja incidencia en nuestra área de leishmaniasis visceral (LV), no existe una recomendación de cribado antes de iniciar una TB, y solo se recomienda un control serológico periódico a estos pacientes si viven en zonas con elevada incidencia5,6.
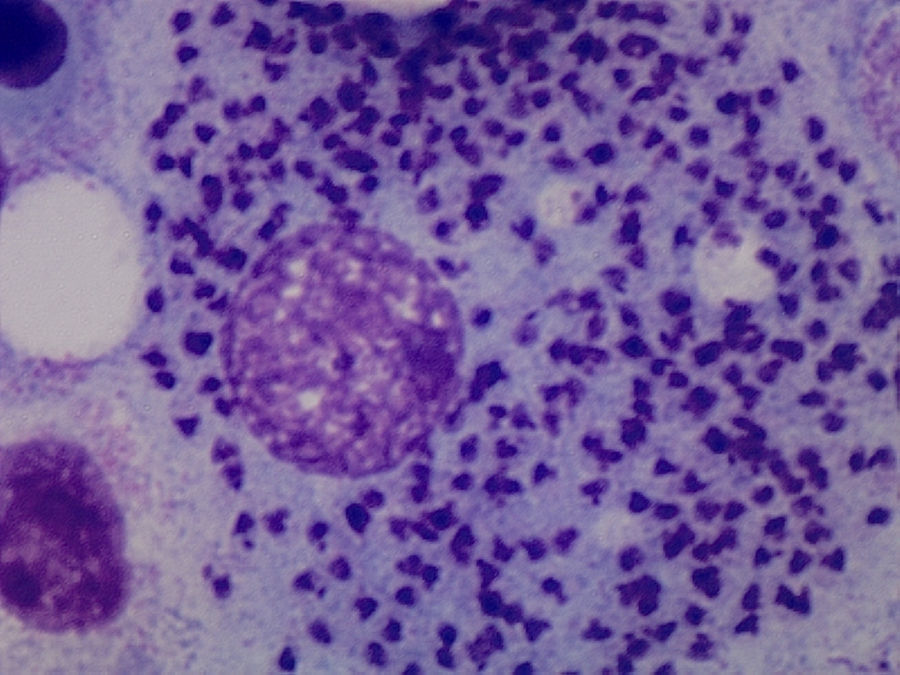
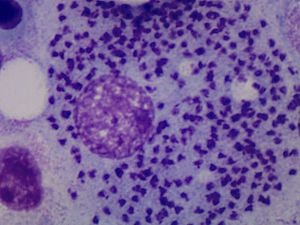
Caso clínicoMujer de 64 años, con antecedente de artroplastia de cadera bilateral, diagnosticada de AR en el año 2002 a raíz de poliartritis simétrica, erosiva, y seropositiva (FR+, ACPA+). De manera progresiva se vió afectada por una artritis asimétrica, y aditiva de grandes y pequeñas articulaciones. Recibió como tratamiento de fondo del curso de su enfermedad MTX 15mg/semana (vo), ácido fólico 5mg/semana, indometacina 25mg/8h y dosis bajas de prednisona. No presentaba antecedentes epidemiológicos de interés. En 2012, la paciente comienza con un cuadro de astenia importante y episodios de picos febriles, que en el momento de la evaluación actual llevaba ya 2 meses de evolución y se acompañaba de pancitopenia (leucocitos: 3.200 [linfocitos: 1.100], Hb: 9g/l, plaquetas: 91.000) observada en una analítica de rutina. Se decide ingreso para estudio. En la exploración física destaca una palidez cutáneo-mucosa, ausencia de adenopatías, y la exploración por aparatos fue anodina. Se suspendió el tratamiento con MTX ante la sospecha de posible toxicidad hematológica. Se realizó una ecografía abdominal y una TC toracoabdominal, que demostró una esplenomegalia. Se realizaron determinaciones serológicas de HIV, VHB y VHC que fueron negativas, y un aspirado de médula ósea (AMO), que confirmó preservación de celularidad medular, y afectación difusa intra y extracelular por leishmaniasis (fig. 1). Una vez establecido el diagnóstico de LV se inició tratamiento con anfotericina B liposomal a dosis de 3mg/kg hasta recibir 10 dosis. A las 10 semanas, la paciente quedó afebril y de forma paulatina el hemograma fue mejorando hasta la normalización. En la actualidad, la paciente sigue asintomática con hidroxicloroquina, y presenta un buen control clínico de la AR.
DiscusiónLos pacientes con AR pueden presentar un amplio espectro de comorbilidades extra-articulares asociadas: entre estas, las alteraciones hematológicas y las infecciones representan un porcentaje elevado, motivo por el cual el diagnóstico diferencial es muy amplio. Durante las visitas de monitorización y seguimiento de los pacientes con AR se realiza un seguimiento del perfil analítico: hematológico y bioquímico, acorde con las guías de práctica clínica recomendadas7. Ante la presencia de una citopenia aislada o de una pancitopenia, se deben estudiar las complicaciones de la propia enfermedad, la toxicidad farmacológica asociada, las infecciones nosocomiales y se debe descartar, también, un proceso hematológico.
La leishmaniasis se entiende como un conjunto de síndromes causados por la infección del protozoo del género Leishmania muy extendidos en zonas tropicales, mientras que L. infantum es endémica en el Mediterráneo. Pueden presentar 3 perfiles clínicos: la forma cutánea, la forma mucosa y la forma visceral. Esta última puede ser mortal en ausencia de tratamiento. Se transmiten por la picadura de un mosquito flebotomo. Dependiendo de la especie de Leishmania, del género del mosquito transmisor y de la localización geográfica, los reservorios principales son perros, roedores o personas. La LV puede presentarse de forma silente o, por el contrario, de forma florida (Kala-azar) con una péntada característica: fiebre prolongada, pérdida de peso, hepatoesplenomegalia, pancitopenia e hipergammaglobulinemia. Durante su curso, la enfermedad subclínica se puede volver sintomática en pacientes que reciben fármacos inmunosupresores como glucocorticoides, MTX o TB. El diagnóstico de leishmaniasis se puede realizar de 3 maneras: clínica, parasitaria e inmunológica. Se considera recomendable confirmar el diagnóstico parasitológico, visualizando el protozoo en los tejidos o en frotis. El AMO, en caso de duda diagnóstica, proporciona resultados satisfactorios. El diagnóstico diferencial del cuadro florido de LV, se debe hacer con procesos malignos hematológicos, linfáticos y con procesos infecciosos como el paludismo. Actualmente, el tratamiento de elección de la LV en países desarrollados es la anfotericina B liposómica.
Al revisar la literatura llama la atención que hay menos casos descritos de pacientes con AR en tratamiento con MTX que pacientes con AR en tratamiento con anti-TNF que desarrollan infección por Leishmania. Se desconoce el por qué. Tampoco parece existir en estos pacientes un factor común predisponente a la infección. El MTX disminuye la respuesta inmune celular, inhibe la quimiotaxis de los neutrófilos y la proliferación de linfocitos T y se ha relacionado con el desarrollo de infecciones por gérmenes oportunistas, entre los que se encuentra la Leishmania.
Los pacientes con AR en tratamiento con MTX tienen mayor predisposición a desarrollar LV que la población general, seguramente debido a las alteraciones inmunológicas relacionadas con su enfermedad de base y con el tratamiento que reciben.
El TNF es una citocina implicada en la respuesta inmunomediada ante una infección, especialmente contra patógenos intracelulares. Los anti-TNF son cada vez más utilizados en la AR y su uso se ve claramente relacionado con un aumento del número de infecciones oportunistas en estos pacientes.
El diagnóstico de LV debe de ser considerado entre los pacientes con sospecha de infección que presentan enfermedad reumática inflamatoria y reciben MTX que además residen en áreas donde la Leishmania es endémica.
La importancia de un diagnóstico precoz, realizado durante las visitas de seguimiento de la enfermedad de base permitió establecer el diagnóstico de LV en este caso. Iniciar un tratamiento específico de forma temprana es fundamental para mejorar el pronóstico de una enfermedad potencialmente grave. A este hecho se le añade que, aunque infrecuente, no debemos olvidar que la leishmaniasis es endémica en el Mediterráneo.
ConclusiónEl manejo actual de los pacientes con AR es muy satisfactorio8. La mejora en la monitorización, y la aparición de nuevas dianas terapéuticas, ofrece tasas de supervivencia más elevadas. El pronóstico es asimismo más favorable, pero estas mismas terapias que inducen en ocasiones, la remisión, conllevan algunos riesgos añadidos9,10.
El presente trabajo describe un proceso infeccioso sobreañadido a la propia AR, en parte debido a la susceptibilidad de la enfermedad inflamatoria crónica, junto con el riesgo añadido que confieren las terapias inmunosupresoras como el MTX. Debemos recoger la comorbilidad de la AR, haciendo énfasis en los procesos infecciosos por gérmenes clásicos, sin obviar las infecciones por gérmenes oportunistas más infrecuentes como la Leishmania.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.