Desde la aparición de la aspirina hace más de 100 años, se ha demostrado las ventajas de utilizar este medicamento en el control de diversos estados patológicos. Posteriormente, los antiinflamatorios no esteroideos (AINE) han aportado una aplicación más segura y conservan la capacidad antiinflamatoria. A pesar de ello, las complicaciones gastrointestinales de los AINE han limitado notablemente su utilización, principalmente en población mayor de 65 años de edad, por los factores de riesgo gastrointestinal, que impiden su prescripción confiable en estos grupos de enfermos, en quienes algunas enfermedades reumáticas, como la osteoartrosis, son más comunes. Esto llevó al desarrollo de los antiinflamatorios inhibidores selectivos de la ciclooxigenasa 2, que han mostrado una mayor seguridad gastrointestinal y mantienen la misma capacidad antiinflamatoria.
Seguridad cardiovascularRofecoxibA partir de 1999 cuando aparecieron en el mercado los primeros inhibidores selectivos de la ciclooxigenasa (coxib), en diversos ensayos clínicos se hizo evidente que estas nuevas moléculas podrían tener efectos diferentes de los AINE en cuanto al perfil de seguridad. Esto fue notorio al conocer los resultados del estudio VIGOR (Vioxx and Gastrointestinal Outcomes Research)1, en el que se comparó 50mg de rofecoxib/día contra 500mg/12h de naproxeno en una población de aproximadamente 8.000 personas con artritis reumatoide, las que no se les permitió utilizar dosis antiagregante plaquetaria de ácido acetilsalicílico a pesar de que un porcentaje de esa población tenía factores de riesgo cardiovascular.
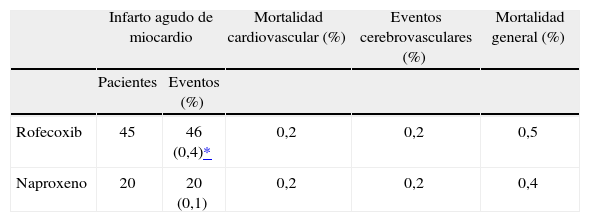
El objetivo primario del estudio fue valorar la seguridad gastrointestinal del medicamento, comparado con naproxeno. Un hecho que no debe pasar inadvertido fue que se utilizó el doble de la dosis (50mg) que habitualmente se utiliza en la práctica clínica y que los pacientes con artritis reumatoide tienen mayores morbilidad y mortalidad cardiovascular que la población general. En los resultados del estudio se observó que la dosis de rofecoxib produjo una reducción del 54% en los eventos adversos digestivos altos. Sin embargo, también se demostró que naproxeno se asoció a un número significativamente menor de eventos adversos cardiovasculares (infarto de miocardio no fatal, enfermedad cerebrovascular no fatal y muerte súbita) en comparación con rofecoxib (el 0,8% para rofecoxib contra el 0,4% para naproxeno; p < 0,05); esta diferencia se atribuyó principalmente a una incidencia elevada de infarto de miocardio en el grupo de pacientes que tomaron rofecoxib. El riesgo relativo (RR) para un evento cardiovascular fue 2,38 (intervalo de confianza [IC] del 95%, 1,39-4; p < 0,0001) (tabla 1).
Eventos vasculares y mortalidad en el estudio VIGOR
| Infarto agudo de miocardio | Mortalidad cardiovascular (%) | Eventos cerebrovasculares (%) | Mortalidad general (%) | ||
| Pacientes | Eventos (%) | ||||
| Rofecoxib | 45 | 46 (0,4)* | 0,2 | 0,2 | 0,5 |
| Naproxeno | 20 | 20 (0,1) | 0,2 | 0,2 | 0,4 |
El estudio CLASS (Celecoxib Long-term Arthritis Safety Study)2, desarrollado para analizar la seguridad gastrointestinal de celecoxib comparado con dos AINE no selectivos, incluyó aproximadamente una cantidad de sujetos similar al estudio VlGOR; sin embargo, esta población estaba compuesta por pacientes con osteoartrosis y artritis reumatoide, la primera de las cuales tiene menor riesgo cardiovascular comparada con la segunda, y por otra parte, este ensayo sí permitió utilizar dosis bajas de aspirina como antiagregante plaquetario. Los resultados mostraron que celecoxib tenía un perfil de seguridad gastrointestinal mejor que los dos AINE que se utilizaron para comparación, y en relación con la seguridad cardiovascular, se demostró que no había diferencia significativa entre celecoxib, diclofenaco e ibuprofeno (tabla 2).
Sin embargo, este ensayo reportó los datos de aproximadamente la mitad del tiempo de duración del estudio (6 de los 12 meses programados), y cuando los datos estuvieron completos, se pudo evidenciar que no había una diferencia clara en los puntos finales de seguridad gastrointestinal entre celecoxib y los AINE con los que se había comparado3.
Por otra parte, al hacer una revisión del promedio anual de infarto de miocardio y comparar los resultados de los ensayos VlGOR y CLASS, se observó que las cantidades eran similares (el 0,74 y el 0,80%, respectivamente)4.
Después de la publicación de los estudios VlGOR y CLASS, aparecieron varios tipos de ensayos que analizaban de diferente manera, y en poblaciones distintas, la seguridad cardiovascular de los coxib, con resultados que incrementaron la controversia. En este sentido, el trabajo de Konstam et al5, un análisis agrupado de 23 estudios de fase IIb a V con rofecoxib, que incluyó a 28.000 pacientes y cuyo punto de desenlace fue el establecido por el Antiplatelet Trialists’ Collaboration (APTC), que incluye muerte de origen cardiovascular, hemorrágica o desconocida, infarto de miocardio no mortal o enfermedad cerebrovascular no mortal, demostró que el riesgo relativo de que se cumpliera el punto de desenlace fue 0,84 (lC del 95%, 0,51-1,38) al comparar rofecoxib con placebo, en la comparación de rofecoxib contra AINE no naproxeno el RR fue 0,79 (lC del 95%, 0,040-1,55), aunque esta comparación se efectuó solamente en pacientes con osteoartrosis, y 1,69 (lC del 95%, 1,07-2,69) al comparar rofecoxib contra naproxeno. De esta manera se concluyó que no había ningún riesgo cardiovascular al utilizar rofecoxib comparado con placebo y con AINE no naproxeno y que la diferencia observada entre rofecoxib y naproxeno se podría deber principalmente al efecto antiplaquetario de naproxeno. Sin embargo, no se excluyó la posibilidad de que el riesgo elevado con rofecoxib fuese porque no se utilizó aspirina en la población con artritis reumatoide con un riesgo cardiovascular alto6.
En contra de la postura anterior, se publicaron diversas evidencias que confirmaban el riesgo cardiovascular elevado con rofecoxib y, en este sentido, un ensayo de casos y controles de 54.475 pacientes de más de 65 años demostró que el uso actual (la ingesta en el momento de realizar el ensayo) de rofecoxib se asociaba con un RR elevado de infarto agudo de miocardio comparado con celecoxib (odds ratio [OR] = 1,24; IC del 95%, 1,05-1,46; p = 0,011) y con fármacos distintos de los AINE (OR = 1,14; IC del 95%, 1,00-1,31; p = 0,054), y de la misma forma se demostró que el RR se elevaba al utilizar dosis de rofecoxib mayores de 25mg/día, y que esta elevación del RR ocurría preferentemente en los primeros 90 días de tratamiento7.
Esta controversia finalizó el 30 de septiembre de 2004 cuando Merck anunció que retiraba rofecoxib del mercado debido a su elevado riesgo cardiovascular, fundamentado en los resultados del estudio APPROVE que se encontraba corriendo en 2.568 pacientes con adenomas colorrectales, donde se comparaba 25mg de rofecoxib con placebo, con el fin de prevenir la recurrencia de pólipos colónicos neoplásicos. Los criterios de exclusión del ensayo fueron la hipertensión no controlada (> 165/95mmHg) y la insuficiencia cardíaca crónica; sin embargo, se pudo incluir a pacientes con riesgo cardiovascular elevado (antecedentes de infarto de miocardio) y se permitió la utilización de dosis bajas de aspirina en el 20% de la población de estudio, en un seguimiento a 3 años.
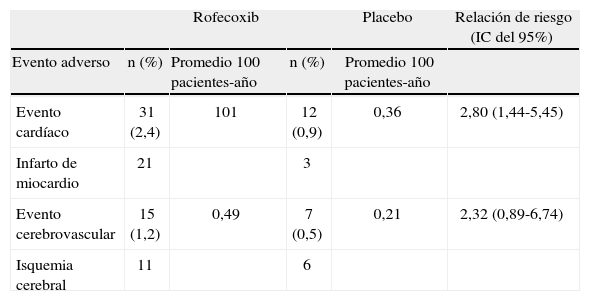
El estudio fue suspendido por razones de seguridad, después de observarse en un análisis preliminar que los pacientes que tomaban rofecoxib tenían el doble de riesgo de un evento cardiovascular que los asignados a placebo (RR = 1,96; IC del 95%, 1,20-3,19; p = 0,007). El riesgo relativo para un punto final del APTC fue 2,25 (IC del 95%, 1,24-4,08; p = 0,008). Se presentaron 25 eventos cardiovasculares confirmados en 3.315 pacientes-año en el grupo placebo (0,75 eventos por 100 pacientes-año) y 45 en 3.041 pacientes-año que tomaban rofecoxib (1,48 eventos por 100 pacientes-año). Los resultados reflejan un desequilibrio en la presencia de infarto de miocardio e isquemia cerebrovascular; sin embargo, estas diferencias se observaron después de 18 meses de tratamiento. Debe señalarse que la utilización basal de dosis bajas de aspirina o bien durante más de la mitad del seguimiento no demostró una interacción significativa entre eventos trombóticos serios y los subgrupos de análisis8. La tabla 3 muestra los eventos trombóticos serios confirmados.
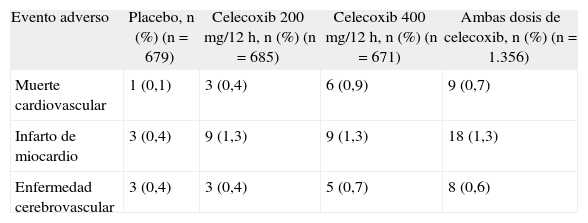
Riesgo de enfermedad vascular con celecoxib en el estudio APC
| Evento adverso | Placebo, n (%) (n = 679) | Celecoxib 200mg/12h, n (%) (n = 685) | Celecoxib 400mg/12h, n (%) (n = 671) | Ambas dosis de celecoxib, n (%) (n = 1.356) |
| Muerte cardiovascular | 1 (0,1) | 3 (0,4) | 6 (0,9) | 9 (0,7) |
| Infarto de miocardio | 3 (0,4) | 9 (1,3) | 9 (1,3) | 18 (1,3) |
| Enfermedad cerebrovascular | 3 (0,4) | 3 (0,4) | 5 (0,7) | 8 (0,6) |
Una situación muy parecida ocurrió con celecoxib. El estudio APC (Adenoma Prevention with Celecoxib) incluyó a 2.035 pacientes sometidos a polipectomía endoscópica con el fin de comparar la reducción de pólipos adenomatosos en colon y recto, 1 y 3 años después del procedimiento se comparan celecoxib 200 y 400mg 2 veces al día contra placebo, se permitía el uso de aspirina para prevención cardiovascular. Después de un seguimiento promedio de 2,8 a 3,1 años los enfermos que recibieron 200mg 2 veces al día mostraron una relación de riesgo de 2,3 (IC del 95%, 0,9-5,5) para muerte de causa cardiovascular, infarto de miocardio, enfermedad cerebrovascular o insuficiencia cardíaca, y en quienes tomaron 400mg 2 veces al día, la relación del riesgo fue 3,4 (IC del 95%, 1,4-7,8). La incidencia anual de muerte por el mismo objetivo compuesto fue 7,8 eventos por 1.000 pacientes-año en el grupo de 200mg de celecoxib 2 veces al día y de 11,4 eventos por 1.000 pacientes-año en quienes recibieron 400mg 2 veces al día. Similar a lo ocurrido en el estudio APPROVe, los enfermos que en condiciones basales tenían un mayor riesgo cardiovascular presentaron un mayor número de eventos adversos trombóticos, independientemente del uso de aspirina. Estos datos dieron mayor fundamento para sostener el concepto de que los inhibidores de COX-2 pueden incrementar el riesgo de eventos cardiovasculares serios y motivó que el ensayo se suspendiera9. La tabla 4 muestra los componentes individuales del objetivo compuesto del estudio.
Eventos adversos vasculares en el estudio APPROVe
| Rofecoxib | Placebo | Relación de riesgo (IC del 95%) | |||
| Evento adverso | n (%) | Promedio 100 pacientes-año | n (%) | Promedio 100 pacientes-año | |
| Evento cardíaco | 31 (2,4) | 101 | 12 (0,9) | 0,36 | 2,80 (1,44-5,45) |
| Infarto de miocardio | 21 | 3 | |||
| Evento cerebrovascular | 15 (1,2) | 0,49 | 7 (0,5) | 0,21 | 2,32 (0,89-6,74) |
| Isquemia cerebral | 11 | 6 |
IC: intervalo de confianza.
Etoricoxib es también una molécula inhibidora de COX-210 que ha demostrado una capacidad analgésica favorable en diferentes modelos experimentales. Los estudios en humanos sanos demostraron que no inhibe la agregación plaquetaria, ni prolonga el tiempo de sangrado, tiene una vida media de 22h que facilita la administración cada 24h y, por otra parte, en diferentes estudios clínicos se ha demostrado que es tan efectivo como la indometacina para tratar la crisis aguda de gota11 e igualmente es efectivo en osteoartrosis12 y artritis reumatoide13.
El estudio EDGE14, diseñado para analizar la tolerancia gastrointestinal de etoricoxib en osteoartrosis, mostró un mejor perfil de seguridad digestiva que diclofenaco y sin complicaciones cardiovasculares. Este ensayo de 1 año de duración incluyó a 7.111 pacientes con una edad promedio de 64 años, de los que alrededor del 4% tenía el antecedente de un evento gastrointestinal alto, el 28% tomaba aspirina desde antes de ser incluidos, el 45% sufría hipertensión arterial y el 37% estaba considerado como de alto riesgo para enfermedad cardiovascular. Se trató a todos estos pacientes con 90mg/día de etoricoxib o diclofenaco 50mg 3 veces al día.
No se presentaron diferencias en los promedios de eventos cardiovasculares entre etoricoxib y diclofenaco durante el desarrollo del estudio, y 14 días después de suspender el tratamiento se observó un riesgo relativo de eventos cardiovasculares de 1,07 (IC del 95%, 0,65-1,74) y de 1,02 (IC del 95%, 0,64-1,62) a los 28 días. En el caso de la enfermedad cerebrovascular, se observó un promedio de 0,15 en la población que recibió etoricoxib y 0,23 en quienes fueron tratados con diclofenaco. Los promedios de infarto de miocardio (por 100 pacientes-año) fueron 0,68 para etoricoxib y 0,42 para diclofenaco15,16.
Valdecoxib y parecoxibValdecoxib, así como su profármaco parecoxib, pertenece al grupo de las sulfonamidas, a dosis de 5-10mg una vez al día tiene la misma eficacia que los AINE tradicionales para tratar la osteoartrosis sintomática de rodilla y cadera16. En 10 ensayos aleatorizados y controlados demostró ser más efectivo que placebo en el tratamiento de la osteoartritis, la artritis reumatoide, la dismenorrea y la analgesia posquirúrgica. De la misma forma fue bien tolerado y mostró la misma incidencia de eventos adversos que el placebo.
En un estudio de fase III, a doble ciego, aleatorizado, controlado con placebo y con grupo paralelo en 462 pacientes sometidos a cirugía coronaria, al comparar parecoxib/valdecoxib contra el cuidado analgésico ordinario, se observó que el grupo experimental recibió menos dosis de morfina o equivalentes que los pacientes en el grupo control y tuvieron una mejoría significativa en 6 de los 8 dominios evaluados con el cuestionario Brief Pain Inventory. No se observaron diferencias en los eventos adversos en general; sin embargo, los eventos adversos serios fueron dos veces más frecuentes en el grupo parecoxib/valdecoxib (19%; 59/311 pacientes) que en los controles (9,9%; 15/151 pacientes; p = 0,015). El principal evento adverso serio que se observó fue una mayor incidencia de infección en la herida esternal en el grupo experimental (10 [3,2%]) contra el grupo control (0 [0%]) (p = 0,035). Otros eventos adversos serios entre los cuales se encontraban complicaciones cerebrovasculares, infarto de miocardio y disfunción renal también fueron proporcionalmente más frecuentes en el grupo experimental, pero no mostraron una diferencia estadísticamente significativa17.
El estudio Coronary-Artery Bypass Grafting (CABG) incluyó a 1.671 pacientes previamente sometidos a una derivación cardiopulmonar en forma electiva y que en los 3 meses antes de entrar al estudio no presentaron accidente cerebrovascular, isquemia cerebral transitoria, trombosis venosa profunda o embolia pulmonar.
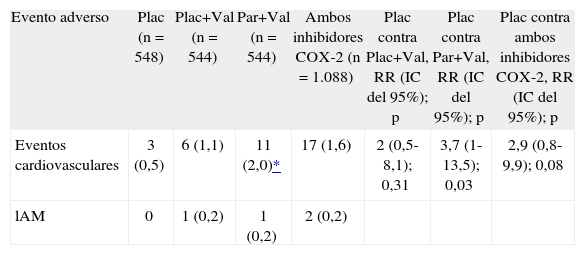
Igualmente, se excluyó a los pacientes que en los 7 días antes de ingresar al estudio sufrieron un infarto agudo de miocardio. Se aleatorizó a los pacientes en 3 grupos para recibir: parecoxib intravenoso, 3 días, seguido por valdecoxib oral hasta el día 10; placebo intravenoso seguido por valdecoxib oral, o placebo durante 10 días. Los resultados pusieron en evidencia una mayor frecuencia estadísticamente significativa de eventos cardiovasculares en el grupo que recibió parecoxib/valdecoxib que en el grupo placebo (el 2 contra el 0,5%; relación de riesgo, 3,7; IC del 95%, 1,0-13,5; p = 0,03). Tomando en cuenta los resultados es recomendable evitar estos medicamentos en la población sometida a derivaciones cardiopulmonares porque los riesgos del tratamiento con valdecoxib/parecoxib superan los beneficios en esta población18. La tabla 5 resume los eventos cardiovasculares y los infartos agudos de miocardio que se presentaron durante el ensayo CABG.
Eventos adversos vasculares en el estudio CABG
| Evento adverso | Plac (n = 548) | Plac+Val (n = 544) | Par+Val (n = 544) | Ambos inhibidores COX-2 (n = 1.088) | Plac contra Plac+Val, RR (IC del 95%); p | Plac contra Par+Val, RR (IC del 95%); p | Plac contra ambos inhibidores COX-2, RR (IC del 95%); p |
| Eventos cardiovasculares | 3 (0,5) | 6 (1,1) | 11 (2,0)* | 17 (1,6) | 2 (0,5-8,1); 0,31 | 3,7 (1-13,5); 0,03 | 2,9 (0,8-9,9); 0,08 |
| lAM | 0 | 1 (0,2) | 1 (0,2) | 2 (0,2) |
El estudio TARGET (Therapeutic Arthritis Research and Gastrointestinal Event Trial) incluyó a 18.325 pacientes mayores de 50 años, con osteoartrosis, a quienes se aleatorizó para tratarlos con lumiracoxib 400mg/día (9.156), naproxeno 500mg 2 veces al día (4.754) o ibuprofeno 800mg 3 veces al día (4.415). Se incluyó a pacientes con alto riesgo cardiovascular a los que se les permitió utilizar dosis bajas de aspirina (75-100mg/día) para profilaxis cardiovascular primaria o secundaria (el 24% de la población; n = 4.326). El objetivo primario del ensayo fue el riesgo de desarrollar complicaciones ulcerosas altas y en forma secundaria analizar la morbilidad y la mortalidad cardiovascular.
Los resultados demostraron que lumiracoxib disminuye 3-4 veces la posibilidad de presentar complicaciones ulcerosas, al compararlo con AINE19.
En relación con la seguridad cardiovascular, el grupo que comparaba lumiracoxib contra naproxeno incluyó una cantidad mayor de pacientes con antecedentes de riesgo cardiovascular (12%) que el grupo de lumiracoxib contra ibuprofeno (8%). En el total de enfermos no se observaron diferencias en el número de infartos de miocardio entre lumiracoxib y ambos AINE; sin embargo, los pacientes que recibieron naproxeno sin aspirina profiláctica tuvieron menos infartos de miocardio (4 eventos; 0,11%) que el grupo con lumiracoxib (10 eventos; 0,28%; p = 0,1454). En los pacientes que sí tomaban dosis bajas de aspirina, la incidencia fue similar20.
Los autores explicaron estos hechos por dos mecanismos, primero, la influencia del azar y, segundo, por el efecto antitrombótico de naproxeno, sin olvidar que en condiciones basales el grupo que comparó lumiracoxib contra naproxeno tenía mayores antecedentes de riesgo cardiovascular (12%).
Probables razones de una mayor mortalidad cardiovascularDespués de la introducción de los coxib en la práctica clínica, FitzGerald et al21 llamaron la atención de su efecto en la síntesis de eicosanoides endoteliales, al poner en evidencia la disminución de los metabolitos urinarios de prostaciclina (PGI-2), sin afectar a la excreción de tromboxano A2 (TXA-2) o la agregación plaquetaria. Estos resultados indicaron que al suprimir la producción endotelial de PGI-2, se permite la actividad sin oposición de la COX-1 plaquetaria que lleva a la sintesis de TXA-2 y a un probable estado protrombótico, esta situación se vio reforzada por los resultados del estudio VIGOR1 y los metaanálisis posteriores que generaron resultados conflictivos, como se mencionó anteriormente. Tratando de encontrar una explicación a estos hechos FitzGerald et al22 proponen tres explicaciones no excluyentes entre sí, la capacidad protrombótica de rofecoxib, la actividad antiagregante plaquetaria de naproxeno, y el probable efecto del azar.
¿Era trombogénico rofecoxib?La PGI-2 producida en el endotelio vascular representa una de las moléculas más importantes involucradas en la antiagregación plaquetaria; sin embargo, no solamente ella es capaz de ejercer este efecto. Debido a su naturaleza antiagregante y vasodilatadora antagoniza los efectos del TXA-2 que estimula la agregación plaquetaria y produce vasoconstricción23. Rofecoxib inhibe solamente la COX-2 por medio de la cual se produce PGI-2 sin efecto en COX-1 plaquetaria productora de TXA-2, y genera un probable estado de desequilibrio a favor de las fuerzas protrombóticas.
Sin embargo, en ratas se demostró que es necesario inhibir COX-1 y COX-2 para que haya daño gástrico24, probablemente porque COX-2 puede sustituir a COX-1 como productora de prostaglandinas citoprotectoras y, por otra parte, COX-1 también puede producir PGI-225. Estas condiciones más el hecho de que haya otras moléculas capaces de neutralizar el efecto activador/agregante plaquetario de TXA-2, como el óxido nítrico, la CD39/ecto-ADPasa26 y la molécula 1 de adhesión plaqueta-célula endotelial27, permitirían suponer que existen varios mecanismos antiagregantes plaquetarios que se mantienen operantes a pesar de la inhibición de la PGI-2 endotelial; esto a su vez nos llevaría a pensar que la sola inhibición de PGI-2 por parte de rofecoxib no fuera lo suficientemente potente como para desencadenar un fenómeno trombótico.
¿Son trombogénicos otros coxib?El estudio CLASS2 reportó que los eventos adversos cardiovasculares fueron similares entre celecoxib y los AINE de comparación (ibuprofeno y diclofenaco); se observó insuficiencia cardíaca (9 y 9 casos, respectivamente), infarto de miocardio (10 y 10 eventos, respectivamente) y enfermedad coronaria (9 y 7 episodios, respectivamente).
En un analisis posterior28 se calcularon los promedios anualizados de infarto de miocardio para el estudio VIGOR y CLASS y se observó que, en ambos casos, el promedio era mayor para ambos coxib comparados con placebo: el 0,74% (p = 0,04) para rofecoxib y el 0,80% (p = 0,02) para celecoxib.
De la misma forma, un estudio retrospectivo también demostró datos de un incremento del riesgo cardiovascular con celecoxib29.
Ciertamente estos datos requieren interpretarse con mucho cuidado, tomando en cuenta que en el tipo de estudios que los generaron pueden existir sesgos importantes y variables que no pueden controlarse o bien el efecto de éstas en otros puntos terminales, de tal forma que esto puede llevar a conclusiones no concordantes con la realidad. Previamente se mencionó un estudio proyectado para analizar la capacidad analgésica de parecoxib/valdecoxib en pacientes sometidos a cirugía de derivación coronaria, donde se demostró que la incidencia de eventos adversos serios fue 2 veces más frecuente en el grupo que recibió parecoxib/valdecoxib (19,0%; 59/311 pacientes) que en el grupo control (9,9%; 15/151 pacientes; p = 0,015), y se observó, en primer lugar, la infección de la herida esternal. Otros eventos adversos serios fueron las complicaciones cerebrovasculares, el infarto agudo de miocardio y la disfunción renal, aunque estos últimos fueron proporcionalmente mayores en el grupo que recibió el coxib, no mostraron una diferencia estadísticamente significativa; estos hechos, como hemos visto, los confirmó un estudio posterior que demostró una mayor frecuencia de eventos cardiovasculares en pacientes sometidos a derivación cardiopulmonar electiva y tratados en el postoperatorio con valdecoxib/parecoxib18.
El analisis de 40 pacientes con hipertensión esencial demostró que la inhibición selectiva de COX-2 con parecoxib, profármaco de valdecoxib, es capaz de disminuir la vasodilatación inducida por la acetilcolina en la circulación del antebrazo, situación que no ocurrió con acetilsalicilato-lisina, un inhibidor inespecífico de COX-230. Estos hallazgos pueden explicar de alguna manera las complicaciones cardiovasculares en personas que ya tienen factores de riesgo cardiovascular previamente y que se acentúan por el mecanismo de acción de los coxib.
En relación con los eventos cardiovasculares desencadenados por etoricoxib, previamente mencionamos el trabajo de Matsumoto et al13 en 816 pacientes con artritis reumatoide, a quienes se trató con etoricoxib o naproxeno y donde se confirmaron 2 eventos cardiovasculares en pacientes que tomaron etoricoxib, más una crisis de isquemia transitoria y un infarto de miocardio sin onda Q. Otro estudio muy parecido confirmó 3 eventos trombóticos cardiovasculares, angina de pecho y émbolos pulmonares en 2 pacientes que tomaban etoricoxib y un episodio de tromboflebitis en solamente un paciente del grupo placebo31.
Sin embargo, en el estudio EDGE, que incluyó a una población mucho mayor y con seguimiento de 52 semanas, la incidencia de eventos cardiovasculares no fue diferente entre etoricoxib y diclofenaco. Los promedios de infarto de miocardio (por 100 pacientes-año) fueron 0,68 para etoricoxib y 0,42 para diclofenaco. En el caso de la enfermedad cerebrovascular se observó un promedio de 0,15 en la población que recibió etoricoxib y 0,23 en quienes fueron tratados con diclofenaco14.
Previamente se mencionó que el estudio TARGET20, que analizó la seguridad gastrointestinal de lumiracoxib, mostró una mayor incidencia de infartos agudos de miocardio en el subgrupo que comparó lumiracoxib contra naproxeno que no tomaban aspirina para profilaxis cardiovascular (4 eventos [0,11%] contra 10 eventos [0,28%], respectivamente; p = 0,1454).
Estos datos nos permiten pensar que los coxib diferentes de rofecoxib no están exentos de tener un riesgo cardiovascular mayor cuando se comparan con placebo o naproxeno en una población con factores de riesgo cardiovascular previos. Ahora bien, estos efectos comunes a los coxib permitirían la especulación sobre el hecho de que los eventos adversos cardiovasculares documentados por los diferentes ensayos clínicos puedan deberse más a un efecto de clase y no al mecanismo de acción de una molécula en particular.
¿Es antiagregante plaquetario naproxeno?Esta pregunta ha generado una importante cantidad de ensayos que se han planteado como objetivo el análisis de la capacidad antiagregante de este AINE. Las evidencias en uno y otro sentido se han publicado ampliamente; sin embargo, debido al diseño de la mayor parte de los estudios no ha sido posible llegar a una conclusión inobjetable sobre su efecto antiagregante.
Cuando naproxeno se utiliza a dosis de 500mg/12h en forma regular, produce la inhibición de más del 90% del TXA-2 plaquetario durante el período de ingesta del medicamento32.
Varios estudios de casos y controles han demostrado la capacidad antiagregante plaquetaria de naproxeno. En este sentido, el trabajo de Rahme et al33 concluyó que el uso concurrente crónico de naproxeno tiene una incidencia más baja de infarto agudo de miocardio con una OR de 0,64 (IC del 95%, 0,48-0,86) comparado con los usuarios concurrentes crónicos de otros AINE y sostiene que naproxeno es un inhibidor más potente de COX-1 que ibuprofeno y diclofenaco.
El trabajo de Watson et al34 en pacientes con artritis reumatoide encontró que el riesgo de un evento tromboembólico cardiovascular durante el uso de naproxeno, contra el uso de otros AINE diferentes de naproxeno arrojó una OR de 0,65 (IC del 95%, 0,34-1,24) y el riesgo de infarto de miocardio con el uso actual de naproxeno comparado con el uso actual de otro AINE diferente de naproxeno fue de 0,40 (IC del 95%, 0,13-1,20). Esto indica que los pacientes con artritis reumatoide que actualmente usan naproxeno tienen menor riesgo de un evento tromboembólico cardiovascular, incluido infarto agudo de miocardio, que los enfermos que no utilizaron naproxeno.
Otro estudio de casos y controles35 demostró que el uso de naproxeno produjo un 16% de reducción del riesgo de infarto agudo de miocardio (OR = 0,84; IC del 95%, 0,72-0,98; p = 0,03) e indica que los pacientes que toman AINE no selectivos parecen tener un riesgo menor de eventos cardiovasculares, hechos que coinciden con el efecto protector del naproxeno.
En sentido opuesto, Ray et al36 no encontraron un efecto protector de naproxeno u otros AINE en el riesgo de enfermedad coronaria. Los RR para usuarios actuales y previos de AINE fue 1,05 (IC del 95%, 0,97-1,14) y 1,02 (IC del 95%, 0,97-1,08), respectivamente, y en forma específica para naproxeno fue 0,95 (IC del 95%, 0,82-1,09); para ibuprofeno, 1,15 (IC del 95%, 1,02-1,28), y otros AINE, 1,03 (IC del 95%, 0,92-1,16). Al comparar naproxeno contra ibuprofeno, el RR con el uso actual fue 0,83 (IC del 95%, 0,69-0,98).
Un estudio observacional retrospectivo37, en población canadiense, encontró que naproxeno no disminuye el riesgo de infarto agudo de miocardio a corto plazo, y presenta riesgos relativos muy parecidos entre naproxeno (RR = 1,0; IC del 95%, 0,6-1,7), AINE no selectivos diferentes de naproxeno (RR = 1,2; IC del 95%, 0,9-1,4), celecoxib (RR = 0,9; IC del 95%, 0,7-1,2) y rofecoxib (RR = 1,0; IC del 95%, 0,8-1,4).
Resulta difícil llegar a una conclusión válida con los resultados anteriores tomando en cuenta las limitaciones propias de estos diseños y la falta de un ensayo aleatorizado y con grupo control donde se analice el afecto antiagregante plaquetario de naproxeno contra aspirina, coxib y otros AINE inespecíficos diferentes de naproxeno. Se conoce que naproxeno administrado a dosis de 500mg/12h tiene un buen efecto antiagregante durante ese intervalo de dosis32, de tal manera que un estudio como el señalado podría aclarar con mayor exactitud algunos aspectos como la dosis-respuesta, duración de la respuesta y relaciones temporales.
Ahora bien, es muy probable que todavía no estemos frente a una situación completamente definida en relación con el riesgo potencial de los coxib, tomando en cuenta que no contamos con ensayos aleatorizados, a doble ciego, controlados con placebo en poblaciones sin riesgo cardiovascular, o bien con bajo o alto riesgo, para determinar la dosis adecuada de cada fármaco, el nivel de riesgo de cada uno, el tiempo en que es más probable que ocurra un desenlace negativo y en qué pacientes los beneficios son mayores que los potenciales eventos adversos.
En conclusión podríamos pensar, haciendo un balance de los diversos estudios conocidos hasta la fecha, que el perfil cardiovascular de los coxib parece ser más un efecto de clase y menos probablemente de molécula como se planteó cuando aparecieron los primeros eventos adversos con rofecoxib, de tal forma que en cada paciente necesitamos hacer un análisis completo de los beneficios potenciales y los riesgos que enfrentaría el paciente al momento de utilizar un coxib.