Evaluar la eficacia y la seguridad a corto plazo del tratamiento de pacientes con artritis reumatoide (AR) con rituximab (RTX) comparado con un anti-TNF (2TNF) tras retirada de un primer anti-TNF.
MétodosEstudio multicéntrico prospectivo, observacional, de práctica clínica de pacientes con AR grave refractaria a anti-TNF que recibieron RTX comparados con los que recibieron un 2TNF. Comparación de las variables de eficacia y respuesta EULAR buena/moderada a los 6 meses.
ResultadosCiento tres pacientes incluidos; 82 alcanzan seguimiento a 6 meses, 73,7% mujeres. Datos basales grupo RTX y 2TNF, respectivamente: 8,6 y 6,6 NAD, 8,8 y 7,5 NAI, 5,45 ± 1,28 y 5,18 ± 1,21 en DAS28 (p=0,048), 41 y 38,7mmHg de VSG, y 1,2 y 1,0 en HAQ. Mejoría en todos los parámetros en ambos grupos sin diferencias significativas (excepto mayor reducción de VSG con RTX). Ausencia de efectos adversos graves.
ConclusionesEl uso de RTX en segunda línea de terapia biológica tras fallo a un primer anti-TNF en práctica clínica muestra mejoría en las variables de eficacia y funcionalidad a los 6 meses, sin presentar efectos adversos graves. Estos resultados no difieren de los observados tras el uso de un segundo anti-TNF en el mismo escenario clínico.
to compare the short-term efficacy and safety of rituximab (RTX) therapy versus anti-TNF in rheumatoid arthritis (RA) patients after discontinuation of a first anti-TNF agent.
Methodsprospective observational multicenter study in the clinical practice setting, involving patients with severe RA refractory to a first anti-TNF agent, who received either RTX or a second anti-TNF (2TNF), comparing the efficacy endpoints, EULAR response (Good/Moderate) and safety at 6 months.
Results103 patients enrolled, 82 completed 6-month follow-up, 73.7% women. Baseline data for RTX and 2TNF groups, respectively: TJC, 8.6 and 6.6; SJC, 8.8 and 7.5; DAS28 score, 5.45 (±1.28) and 5.18 (±1.21) (p=0.048), ESR, 41 and 38.7mmHg; and HAQ, 1.2 and 1.0. Improvement was observed in all parameters, with no significant differences (except for a more marked reduction in ESR with RTX). There were no serious adverse events.
ConclusionsRTX use as second-line therapy after anti-TNF failure led to improvements in the efficacy and functional variables at 6 months, with no serious adverse events. These results were comparable to those observed in patients who used a second anti-TNF agent in the same clinical scenario.
La artritis reumatoide (AR) es una enfermedad inflamatoria, autoinmune, que afecta a la población española con una prevalencia estimada de 0,5% siendo superior en mujeres que en hombres. Es una enfermedad crónica incapacitante con unos costes sociales y económicos y unas repercusiones psicológicas considerables, además de la disminución importante en la calidad de vida relacionada con la salud de estos pacientes1. El tratamiento de la AR, desde la aparición de los fármacos modificadores de la enfermedad biológicos, ha avanzado en el control de la enfermedad, la mejoría de los síntomas y la progresión del daño articular, con un buen perfil de seguridad2.
Dada la primera aparición de los anti-TNF como tratamiento biológico (TB), estos han sido los más ampliamente utilizados. Las recomendaciones de la Sociedad Española de Reumatología3 avalan tanto el posible cambio de diana terapéutica como la sustitución de un anti-TNF por otro. Es posible que haya pacientes en los que sea más interesante cambiar de diana terapéutica en lugar de cambiar de inhibidor del TNF alfa en las sucesivas líneas terapéuticas.
Existen datos en la literatura científica que apoyan tanto el cambio (switching) de un anti-TNF por otro, de forma consecutiva, como el cambio de diana terapéutica, como rituximab, entre otros, señalando incluso una posible preferencia por este último en pacientes seropositivos4-8. Algunos de estos resultados proceden de grandes registros observacionales, pero no de trabajos prospectivos.
El objetivo de nuestro trabajo es evaluar la eficacia clínica y seguridad a los 6 meses del inicio del tratamiento con rituximab, comparado con un segundo anti-TNF en segunda línea de TB en pacientes diagnosticados de AR, en práctica clínica.
Pacientes, material y métodosEstudio observacional, prospectivo, en práctica clínica habitual, postautorización en práctica clínica en pacientes con AR (criterios ACR 879) grave en tratamiento de segunda línea de TB, tras presentar respuesta inadecuada o intolerancia a un primer anti-TNF. El estudio fue aprobado por el comité ético de cada centro participante y los pacientes entregaron su consentimiento informado. Un total de 9 centros a nivel nacional y 14 reumatólogos participaron en el estudio, comprendiendo el periodo junio del 2009-septiembre del 2011.
Los pacientes fueron reclutados consecutivamente y recibieron o bien un segundo anti-TNF (2TNF), o bien rituximab (RTX) a juicio de cada investigador y de acuerdo con las recomendaciones de la Guía de uso de terapias biológicas de la Sociedad Española de Reumatología3.
Variables basales y a los 6 meses (previa a la nueva infusión del segundo ciclo de RTX):
- –
Edad, género, años de evolución de la enfermedad, causa de retirada de primer anti-TNF (fallo primario o secundario, intolerancia/efecto adverso).
- –
Número de articulaciones dolorosas, número de articulaciones inflamadas.
- –
Velocidad de sedimentación globular (VSG) en mmHg, proteína C reactiva (PCR) en mg/dl, factor reumatoide IgM (FR) positivo, si título > 15 U/mI) y título mediante nefelometría, anticuerpos anticitrulina positivo si > 20 U/ml, mediante técnica de enzimo-inmunoanálisis.
- –
Disease Activity Index 28 joints (DAS28) de 3 variables incluyendo VSG10.
- –
Efecto adverso leve: no requiere ingreso hospitalario, resuelve con retirada del fármaco; efecto adverso grave: requiere ingreso hospitalario y tratamiento específico.
- –
Cuestionario validado al castellano del Health Assessment Questionnaire (HAQ)11.
Se pretende comparar la respuesta clínica de RTX y de un 2TNF como segunda línea de TB en pacientes con AR a los 6 meses mediante respuesta EULAR buena/moderada12, y mediante la mejoría en los parámetros VSG, PCR, FR y HAQ. Se evalúa el porcentaje de pacientes que presentan retirada del fármaco por efecto adverso.
Análisis estadísticoEl análisis estadístico será realizado a partir de los datos introducidos en una base de datos, realizando análisis descriptivos de todas las variables cualitativas y cuantitativas.
Para realizar comparaciones a lo largo del periodo de estudio, en el caso de variables continuas se utilizará el test F de Snedecor (ANOVA) si las variables se distribuyen normalmente, o el test de Friedman si no cumplen los criterios paramétricos. En el caso de variables dicotómicas, se utilizará el test de Cochran.
El valor de significación estadística se establece en p<0,05. Todos los análisis se realizan con el programa estadístico SPSS 19.0.
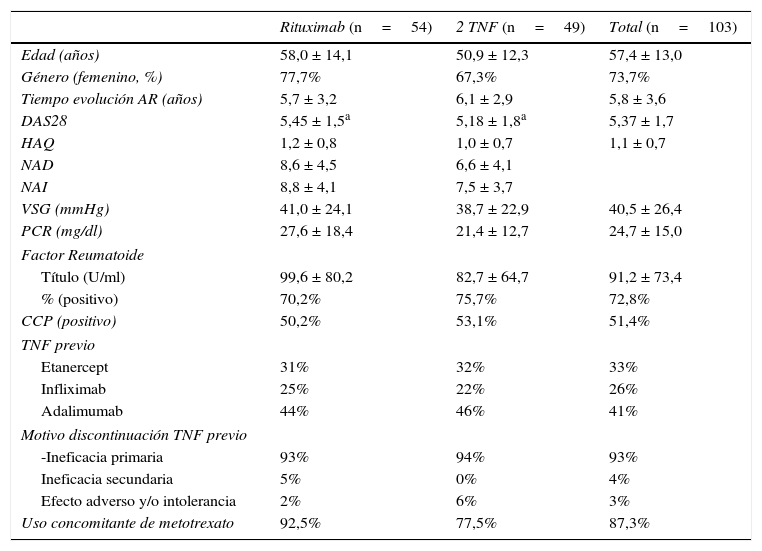
ResultadosSe incluyó a un total de 103 pacientes, 54 en el grupo RTX y 49 en el grupo 2TNF (23 etanercept [47%], 16 adalimumab [32%] y 10 infliximab [20%]), las variables sociodemográficas y clínicas principales de los cuales se muestran en la tabla 1.
Variables sociodemográficas y clínicas basales
| Rituximab (n=54) | 2 TNF (n=49) | Total (n=103) | |
|---|---|---|---|
| Edad (años) | 58,0 ± 14,1 | 50,9 ± 12,3 | 57,4 ± 13,0 |
| Género (femenino, %) | 77,7% | 67,3% | 73,7% |
| Tiempo evolución AR (años) | 5,7 ± 3,2 | 6,1 ± 2,9 | 5,8 ± 3,6 |
| DAS28 | 5,45 ± 1,5a | 5,18 ± 1,8a | 5,37 ± 1,7 |
| HAQ | 1,2 ± 0,8 | 1,0 ± 0,7 | 1,1 ± 0,7 |
| NAD | 8,6 ± 4,5 | 6,6 ± 4,1 | |
| NAI | 8,8 ± 4,1 | 7,5 ± 3,7 | |
| VSG (mmHg) | 41,0 ± 24,1 | 38,7 ± 22,9 | 40,5 ± 26,4 |
| PCR (mg/dl) | 27,6 ± 18,4 | 21,4 ± 12,7 | 24,7 ± 15,0 |
| Factor Reumatoide | |||
| Título (U/ml) | 99,6 ± 80,2 | 82,7 ± 64,7 | 91,2 ± 73,4 |
| % (positivo) | 70,2% | 75,7% | 72,8% |
| CCP (positivo) | 50,2% | 53,1% | 51,4% |
| TNF previo | |||
| Etanercept | 31% | 32% | 33% |
| Infliximab | 25% | 22% | 26% |
| Adalimumab | 44% | 46% | 41% |
| Motivo discontinuación TNF previo | |||
| -Ineficacia primaria | 93% | 94% | 93% |
| Ineficacia secundaria | 5% | 0% | 4% |
| Efecto adverso y/o intolerancia | 2% | 6% | 3% |
| Uso concomitante de metotrexato | 92,5% | 77,5% | 87,3% |
Resultados expresados en media ± desviación estándar) y en porcentajes.
AR: artritis reumatoide; CCP: anticuerpos anticitrulina; DAS28: Disease Activity Score 28 joints; HAQ: Health Assessment Questionnaire; NAD: número articulaciones dolorosas; NAI: número articulaciones inflamadas; PCR: proteína C reactiva; TNF: anti-TNF alfa; VSG: velocidad de sedimentación globular.
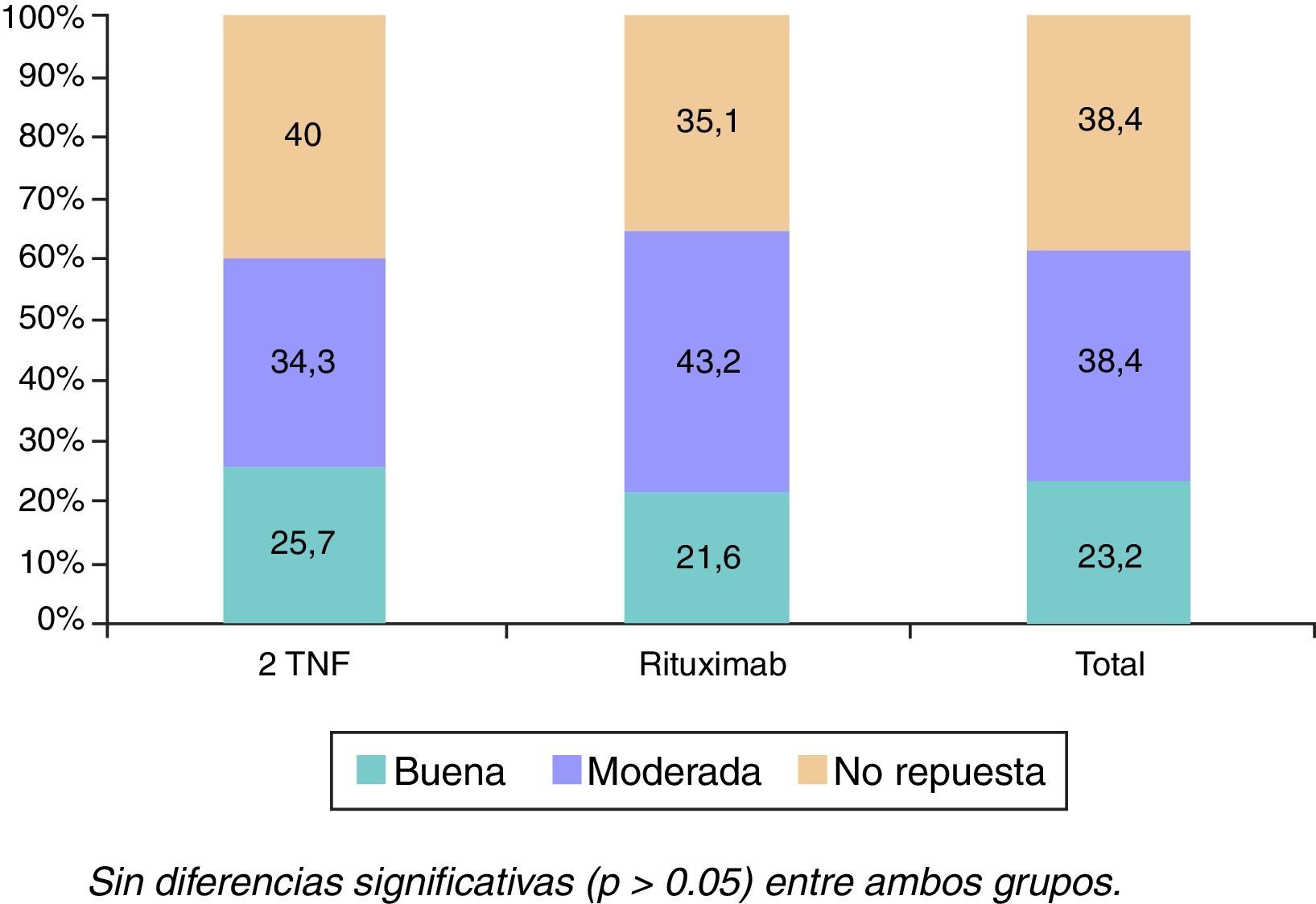
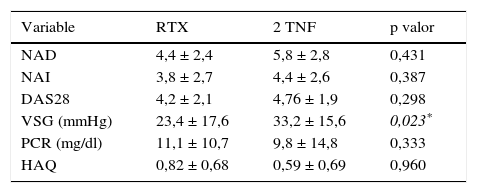
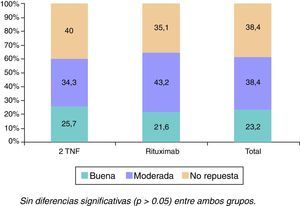
La evolución de los parámetros clínicos, serológicos y funcionales se representa en la tabla 2. Hubo una reducción significativa de todas las variables clínicas, serológicas y funcionales a los 6 meses porcentualmente mayores en el grupo RTX. Estas diferencias no fueron significativas, excepto en cuanto a la reducción de los niveles de VSG (mayor en el grupo RTX [p=0,023]). Las tasas de repuesta EULAR se muestran en la figura 1.
Evolución de los parámetros clínicos y serológicos a los 6 meses
| Variable | RTX | 2 TNF | p valor |
|---|---|---|---|
| NAD | 4,4 ± 2,4 | 5,8 ± 2,8 | 0,431 |
| NAI | 3,8 ± 2,7 | 4,4 ± 2,6 | 0,387 |
| DAS28 | 4,2 ± 2,1 | 4,76 ± 1,9 | 0,298 |
| VSG (mmHg) | 23,4 ± 17,6 | 33,2 ± 15,6 | 0,023* |
| PCR (mg/dl) | 11,1 ± 10,7 | 9,8 ± 14,8 | 0,333 |
| HAQ | 0,82 ± 0,68 | 0,59 ± 0,69 | 0,960 |
Resultados expresados en media ± desviación estándar y en porcentajes.
DAS28: Disease Activity Score 28 joints; HAQ: Health Assessment Questionnaire; NAD: número articulaciones dolorosas; NAI: número articulaciones inflamadas; PCR: proteína C reactiva; VSG: velocidad de sedimentación globular.
* p < 0,05.
Un total de 21 pacientes precisaron retirada de tratamiento (11 grupo RTX y 10 grupo 2TNF). En el grupo RTX un total de 3 (27%) pacientes no completaron la evaluación a los 6 meses por presentar un efecto adverso leve y también 3 (30%) en el grupo de 2TNF, sin evidenciarse diferencias estadísticamente significativas (p=0,457). No se registraron efectos adversos graves en ningún grupo. El resto de los pacientes que fueron retirados del estudio debido a la presencia de un empeoramiento o persistencia de síntomas que motivó un cambio de estrategia terapéutica por parte de su reumatólogo/a, el 73% en el grupo RTX y el 70% en el grupo 2TNF.
DiscusiónEste es un estudio en práctica clínica, prospectivo, que compara la eficacia a corto plazo de RTX con un anti-TNF en segunda línea de TB tras fallo a anti-TNF en pacientes con AR.
Globalmente, la eficacia de RTX fue buena, con elevada proporción de pacientes en respuesta EULAR buena/moderada (64%), comparable con la de un 2TNF (59%), incluso tras haber únicamente recibido un solo ciclo de RTX, ya que la valoración de la eficacia clínica fue realizada antes de la primera infusión del segundo ciclo correspondiente a los 6 meses. Además, la población que recibió RTX presentaba una elevada actividad medida por la puntuación DAS28, incluso mayor que la del grupo comparativo (5,45 vs. 5,18, respectivamente). Es importante señalar que la mayoría de estos pacientes discontinuaron su anti-TNF previo debido a ineficacia primaria, algo que ya se sugiere en observaciones previas13.
A pesar de no haber encontrado diferencias significativas clínicas y funcionales, sí podemos resaltar que RTX se muestra, por lo menos, igual de eficaz que un 2TNF en práctica clínica en un periodo corto de seguimiento (6 meses). A nivel biológico, sí encontramos una reducción mayor de los niveles de VSG en el grupo RTX, muy similar a lo ya publicado por Finckh et al.5. Este grupo encontró mayores diferencias de eficacia en los pacientes tratados con RTX en segunda línea de TB que en los tratados con 2TNF, con un tamaño de muestra muy similar al de nuestro trabajo, algo también comunicado en subsiguientes exploraciones13. Estas observaciones fueron también exploradas en nuestra población por Gomez-Reino et al.14, en un estudio observacional a 6, 9 y 12 meses en pacientes con fallo a uno o más anti-TNF, sin encontrar diferencias significativas entre ambas estrategias terapéuticas. De todas formas, este último estudio sí encontró diferencias en la reducción del DAS28 en los que habían sido previamente tratados con infliximab y adalimumab. En otro trabajo posterior, se evaluó la respuesta a nivel radiográfico, sin encontrar diferencias entre el uso de RTX o un 2TNF tras fallo a anti-TNF15.
Las limitaciones de nuestro estudio son, principalmente, el tamaño de la muestra (que limita el análisis por subgrupos), la mayor actividad basal en grupo RTX, el diseño en práctica clínica, el periodo de seguimiento y la ausencia de evaluaciones radiológicas, pero por otro lado, el carácter prospectivo le otorga mayor valor que el de otros trabajos publicados en esta misma línea.
En conclusión, nuestro datos demuestran que RTX en segunda línea de TB a fallo de un primer anti-TNF utilizado en práctica clínica puede ser, al menos, tan útil como un segundo anti-TNF.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que los procedimientos seguidos se conformaron a las normas éticas del comité de experimentación humana responsable y de acuerdo con la Asociación Médica Mundial y la Declaración de Helsinki.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener conflicto de intereses en la realización de este estudio.
Los autores quieren agradecer la inestimable ayuda de la Srta. Montserrat Sospedra.