La artritis reumatoide es clínicamente muy heterogénea y variable en su evolución, lo que ocasiona que no se pueda detallar un mismo tratamiento para todos los pacientes, ya que éste va a depender del curso clínico y de situaciones concretas que se van a presentar a lo largo del mismo.
ObjetivoRealizar una descripción del tratamiento con fármacos modificadores de la enfermedad (FAME) que se instauran por primera vez en pacientes con artritis reumatoide (AR) o artritis persistente (AP) en la práctica clínica habitual en España.
Material y métodosEstudio epidemiológico, transversal, no controlado, multicéntrico realizado en 15 comunidades autónomas de España durante un período de 5 meses (julio a noviembre del 2006). Se incluyeron pacientes de ambos sexos, mayores de 18 años y diagnosticados de AR según los criterios de la ACR o bien de AP definida como toda artritis (oligoartritis o poliartritis) ≥12 semanas de duración, a los que se les iba a administrar el primer FAME para tratar su enfermedad.
ResultadosSe reclutaron 1.079 pacientes, pero finalmente, 915 (33% ♂/67% ♀) cumplieron todos los criterios exigidos para ser evaluados en el estudio. La edad media de los pacientes fue de 54,6 (DE=15,4) años. El tiempo medio desde la aparición de los síntomas hasta la 1.a visita con el reumatólogo fue de 6,3 (11,3) meses y el tiempo desde la 1.a visita con el reumatólogo y el inicio del tratamiento fue de 4 (13,5) meses. Del total de pacientes evaluados, al 96,7% se les instauró tratamiento con al menos un FAME, al 62,1% se les administraron AINE, al 59,2% corticoesteroides y al 3,8% una terapia biológica. En los pacientes que recibieron FAME, el 90,3% recibió tratamiento con un solo FAME, el 9,5% con 2 FAME y el 0,2% con 3 FAME. En politerapia, los FAME que más a menudo se administraron conjuntamente fueron MTX+Hidroxicloroquina (4,8%), MTX+Leflunomida (2,0%) y MTX+Sulfasalazina (1,5%). El FAME más frecuentemente utilizado en monoterapia fue el MTX (81,3%), seguido de la leflunomida (4,1%) y la hidroxicloroquina (3,2%) En el 89,6%, el tratamiento de primera elección fue el adecuado según las recomendaciones de la SER.
ConclusiónLa pauta de tratamiento de inicio de la AR más frecuente es el MTX en monoterapia. El tratamiento de la AR por los reumatólogos se ha homogeneizado en los últimos años.
Rheumatoid arthritis is clinically very heterogeneous and variable in its progression, and no one treatment works the same for all patients, as this will depend on the clinical course and specific situations.
ObjectiveTo describe the treatment with DMARDs established for the first time in patients with rheumatoid arthritis (RA) or persistent arthritis (PA) in routine clinical practice in Spain.
Material and methodsEpidemiological, cross-sectional, uncontrolled, multicenter study in 15 regions of Spain during a period of five months (July to November 2006). We included patients of both genders, aged 18 years and diagnosed with RA according to ACR criteria or PA defined as any arthritis (oligoarthritis or polyarthritis) lasting ≥12 weeks, which would be given DMARD to treat their disease.
Results1079 patients were recruited, 915 analyzed (33% ♂/♀ 67%) meeting all the criteria required to be evaluated in the study. Mean age of patients was 54.6 (SD=15.4) years. The mean time from onset of symptoms until the 1st visit with the rheumatologist was 6.3 (11.3) months and the time from the 1st visit with the rheumatologist and the start of treatment was 4 (13.5) months. Of the patients tested, 96.7% was treated with at least one DMARD, 62.1% were given NSAIDs, corticosteroids to 59.2% and 3.8% biological therapy. In patients who received DMARDs, 90.3% received treatment with a single DMARD, 9.5% with 2 DMARDs and 0.2% with three DMARDs. In polytherapy, the DMARDs that are most often administered together were MTX + hydroxychloroquine (4.8%), MTX + leflunomide (2.0%) and MTX + sulfasalazine (1.5%). The most frequently used DMARD in monotherapy was MTX (81.3%), followed by leflunomide (4.1%) and hydroxychloroquine (3.2%). In 89.6%, the treatment of first choice was adequate according to the SER.
ConclusionThe most common pattern of initial treatment of RA is MTX monotherapy. Treatment of RA by rheumatologists has been homogenized in recent years.
La artritis reumatoide (AR) es una enfermedad inflamatoria crónica de origen desconocido, caracterizada por una poliartritis simétrica que afecta a pequeñas y grandes articulaciones, con tendencia a la cronicidad y evolución hacia la deformación y destrucción articular. La etiología es multifactorial, y requiere la interacción entre factores genéticos y estímulos antigénicos, probablemente exógenos, todavía desconocidos1. Su distribución es universal y se estima que la prevalencia mundial está en torno al 0,8%, siendo su incidencia de aproximadamente 0,5/1.000 habitantes al año2,3.
La AR es clínicamente muy heterogénea con importantes diferencias no solo entre pacientes, sino también en el mismo paciente en distintas fases de la evolución. Este fenómeno pone de manifiesto la dificultad de describir el curso natural de la enfermedad y, por tanto, la dificultad de predecir su evolución a priori, aspecto de gran importancia si se quiere alterar de una forma eficaz el curso de la enfermedad4. En los últimos años, la información obtenida de los estudios de cohortes con enfermos que fueron incluidos en las recientemente creadas consultas para la detección precoz de la AR (artritis de reciente comienzo) ha mejorado notablemente nuestro conocimiento sobre el curso de la enfermedad, y también ha dado lugar a la definición de la artritis persistente5.
La finalidad del tratamiento de la AR es conseguir la remisión completa o curación. Sin embargo este objetivo todavía no es posible y por lo tanto el planteamiento terapéutico se centra en disminuir la actividad de la enfermedad, para minimizar la posibilidad de lesión articular, aliviar el dolor, mantener el mejor grado funcional y de calidad de vida posibles6. Desgraciadamente, este último objetivo raramente se consigue, ya que, actualmente, la AR no tiene tratamiento curativo. Como otras enfermedades crónicas, la AR exige una evaluación frecuente e integral del paciente, para establecer su situación clínica en cada momento de la evolución. Estas evaluaciones periódicas nos van a permitir valorar qué grado de progresión presenta la enfermedad, predecir un pronóstico, y en consecuencia, indicar el programa terapéutico más acorde; adicionalmente, nos ayudarán a evaluar el grado de cumplimiento del tratamiento y la eficacia de este y sus posibles efectos adversos6,7.
Dada la heterogeneidad y variabilidad de su evolución, no se puede detallar un mismo tratamiento para todos los pacientes, ya que este va a depender del curso clínico y de situaciones concretas que se van a presentar a lo largo del mismo. Hasta hace unos 20 años, el tratamiento de la AR se ha basado en un modelo «piramidal», que consiste en la utilización inicial de antiinflamatorios no esteroideos (AINE), el empleo juicioso de los corticoides y, tras un año de observación de la evolución de la enfermedad, la inclusión de un fármaco modificador de la enfermedad (FAME), que se mantenía en espera de su eficacia o reacción adversa para cambiarlo por otro8,9. Esta actitud se ha modificado en los últimos años ante la evidencia de que la AR no es una enfermedad benigna y de que las lesiones radiológicas se pueden observar en los dos primeros años de evolución. De ahí, que el empleo de FAME (metrotexato, leflunomida, salazopirina, hidroxicloroquina o los fármacos denominados «terapia biológica») que modifican la evolución de la enfermedad, se realice de forma más temprana y que se propugnen terapias combinadas de los mismos, más agresivas, en un intento de alcanzar la remisión de la enfermedad, o la mínima actividad posible, objetivo actual del tratamiento de la AR10.
Sin embargo, el uso de estos fármacos es empírico y aunque todos han mostrado su eficacia en el tratamiento de la AR, no existe un criterio unánime acerca de qué régimen de tratamiento emplear ni de qué fármaco o combinación de fármacos elegir. A la hora de prescribir un fármaco de este tipo se debe tener en cuenta, además del grado de actividad de la enfermedad, los posibles resultados que esperamos obtener y los potenciales efectos tóxicos del mismo. Se han elaborado, y se siguen elaborando, guías y protocolos que pretenden estandarizar y/o protocolizar de alguna forma el tratamiento de los pacientes con AR. En este sentido, la Sociedad Española de Reumatología ha elaborado la GUIPCAR, la guía práctica más completa sobre el manejo de la artritis reumatoide (AR) en España11. La GUIPCAR está dividida en capítulos en los que se aborda desde la sospecha y detección de la enfermedad hasta el diagnóstico, su evaluación, la comorbilidad en AR, su tratamiento farmacológico, el tratamiento de la patología en situaciones especiales, monitorización, seguridad y recomendaciones de los fármacos modificadores de la enfermedad o el tratamiento no farmacológico de la AR. El grado de utilización de esta guía por los reumatólogos españoles no es conocido.
El auge actual de las consultas destinadas a atender las artritis de reciente comienzo ha proporcionado importante información sobre el pronóstico de la AR. Por ejemplo, hoy sabemos que algunas estrategias de tratamiento, más agresivas, mejoran el pronóstico de la AR cuando se utilizan de forma precoz en pacientes con un riesgo elevado de enfermedad grave, entendida en términos de incapacidad funcional, lesión estructural y/o mortalidad. Así, diversos estudios, como el de Houssien et al12, han demostrado que la derivación de los pacientes a una consulta de reumatología durante el primer año desde el inicio de la sintomatología mejora su capacidad funcional (medida mediante el cuestionario Nottingham Health Profile, NHP), comparada con la de los pacientes que fueron remitidos más tardíamente.
Basándonos en toda esa información, decidimos desarrollar un estudio cuyo objetivo principal fue realizar una descripción del tratamiento con FAME que se instaura por primera vez en pacientes con artritis reumatoide (AR) o artritis persistente (AP) en la práctica clínica habitual en España. Los objetivos secundarios fueron: 1) Evaluar el tiempo transcurrido desde el inicio de los síntomas hasta la instauración del tratamiento farmacológico. 2) Describir las características clínicas de los pacientes con AR activa o AP. 3) Evaluar el grado de adecuación del tratamiento farmacológico instaurado a las recomendaciones de la SER (GUIPCAR-2001).
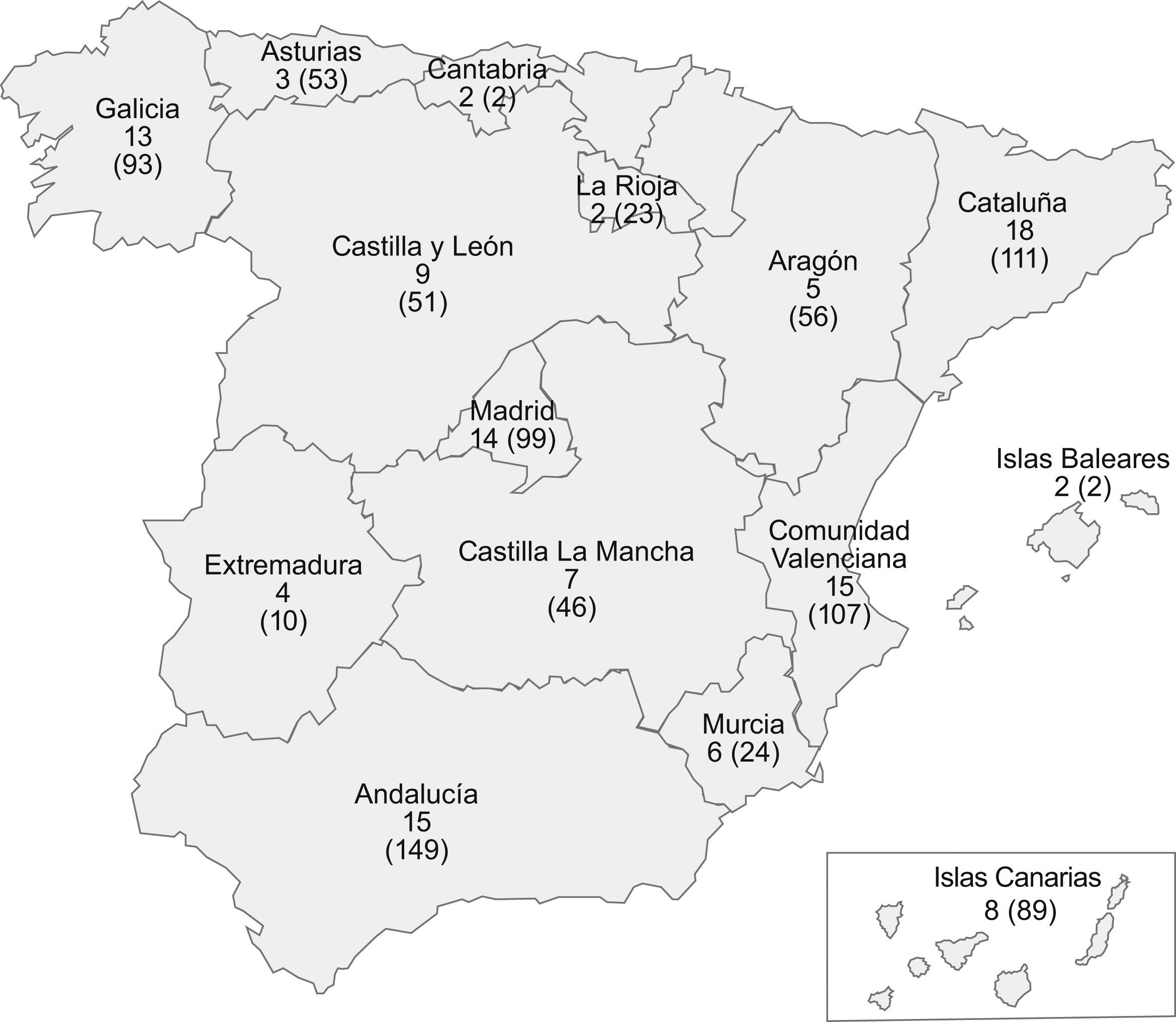
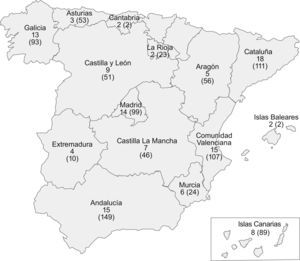
Pacientes y métodosEstudio epidemiológico, transversal, no controlado, multicéntrico realizado en España durante un período de 5 meses (julio–noviembre del 2006). Participaron un total de 127 médicos especialistas en reumatología de centros de especialidades u hospitales de 15 comunidades autónomas (fig. 1). Se incluyeron aquellos pacientes de ambos sexos mayores de 18 años y diagnosticados de AR según los criterios de la ACR o bien de AP definida como toda artritis (oligoartritis o poliartritis) ≥12 semanas de duración, a los que se les iba a administrar el primer FAME para tratar su enfermedad. En el registro de datos además de los datos demográficos y antropométricos (edad, sexo, talla y peso) se recogió información sobre los antecedentes de la artritis: fecha de inicio de los síntomas, fecha de diagnóstico, tiempo desde el inicio de los síntomas hasta la atención por el médico y tiempo desde el inicio del tratamiento. Las variables que se recogieron sobre la evaluación clínica y radiológica del paciente fueron el número de articulaciones tumefactas y dolorosas, la duración de la rigidez matutina, la evaluación global de la salud efectuada por el paciente y el médico en una escala analógica visual, el dolor evaluado por el paciente y la presencia de erosiones radiológicas. Así mismo se registraron datos en relación al fármaco utilizado, posología y el tiempo transcurrido desde la aparición de la sintomatología hasta la instauración del primer tratamiento farmacológico. Se utilizó la guía GUIPCAR del 2001 para valorar la concordancia de los tratamientos con las recomendaciones de la SER.
Se utilizó la prueba t-test de 2 muestras para comparar el número de articulaciones inflamadas y dolorosas, la duración de la rigidez matutina y el índice DAS28 entre los pacientes tratados con Metotrexato inyectable y los tratados con Metotrexato oral. Para comparar las erosiones radiológicas se utilizó el test chi-cuadrado. Los resultados se consideraron significativos para un valor de p≤0,05.
El protocolo de estudio fue aprobado por los comités éticos locales correspondientes siguiendo las directrices de la declaración de Helsinki.
ResultadosDescripción de la poblaciónSe reclutaron 1.079 pacientes de los cuales 164 fueron excluidos por no cumplir alguno o varios de los criterios de selección del estudio, como no presentar un diagnóstico de AR ni cumplir la definición de AP (1 paciente), por ser pacientes que no iniciaban su primer tratamiento con FAMES (161 pacientes) o bien porque no se disponía del consentimiento informado (79 pacientes). Finalmente, 915 (33%♂/67%♀) cumplieron todos los criterios exigidos para ser evaluados en el estudio (tabla 1). La edad media de los pacientes fue 54,6 (DE=15,4) años.
Datos demográficos e historia clínica
| Sexo (femenino/masculino) (%) | 67/33 |
| Edad (años) (media±DE) | 54,6±15,4 |
| Peso (kg) (media±DE) | 70,3±12,1 |
| Talla (cm) (media±DE) | 163,9±8,7 |
| IMC (kg/m)a (media±DE) | 26,2±4,0 |
| N.o articulaciones tumefactas (media±DE) | 8,3±6,1 |
| N.o articulaciones dolorosas (media±DE) | 6,4±4,9 |
| VSG (mm/h)b (media±DE) | 38,1±23,7 |
| PCR (mg/dL)a (media±DE) | 15,8±53,4 |
| Factor reumatoide positivo (%) | 60,1 |
| Erosiones radiológicas (%) | 31,0 |
| DAS28 (media±DE) | 5,3±1,4 |
| Tiempo desde inicio de los síntomas hasta la 1.a visita con el reumatólogo (meses) (media±DE) | 6,3±11,3 |
| Tiempo desde la 1.a visita con el reumatólogo hasta el inicio del tratamiento (meses) (media±DE) | 4,0±13,5 |
| Tiempo desde el diagnóstico hasta el inicio del tratamiento (meses) (media±DE) | 2,3±10,2 |
En una subpoblación de pacientes (n=161) en los que se pudieron recoger variables adicionales sobre la historia de la artritis se advirtió que el tiempo medio desde la aparición de los síntomas hasta la 1.a visita con el reumatólogo fue de 6,3 (11,3) meses y que el tiempo desde la 1.a visita con el reumatólogo y el inicio del tratamiento fue de 4 (13,5) meses.
En el momento de iniciar el tratamiento, los pacientes presentaban una media de 8,3 (6,1) articulaciones tumefactas y 6,44,9 articulaciones dolorosas. Así mismo el 36,2% y el 50,5% de los pacientes tenían < de 6 articulaciones tumefactas y dolorosas respectivamente. El 83,6% de los pacientes referían rigidez matutina con una duración media de 69,0 (51,6)min. En este momento, la valoración de la enfermedad por el paciente y el médico, utilizando una escala analógica visual (EVA) fue similar, 58,3 (23,6) y 53,7 (22,1)mm respectivamente. La VSG media fue de 38,1 (23,7)mm/h y la PCR 15,8 (53,4)mg/dl. El 60,1% de los pacientes eran factor reumatoide (FR) positivo y el 31,0% tenía erosiones radiológicas. El DAS28 medio en el momento de iniciar el tratamiento fue 5,31,4.
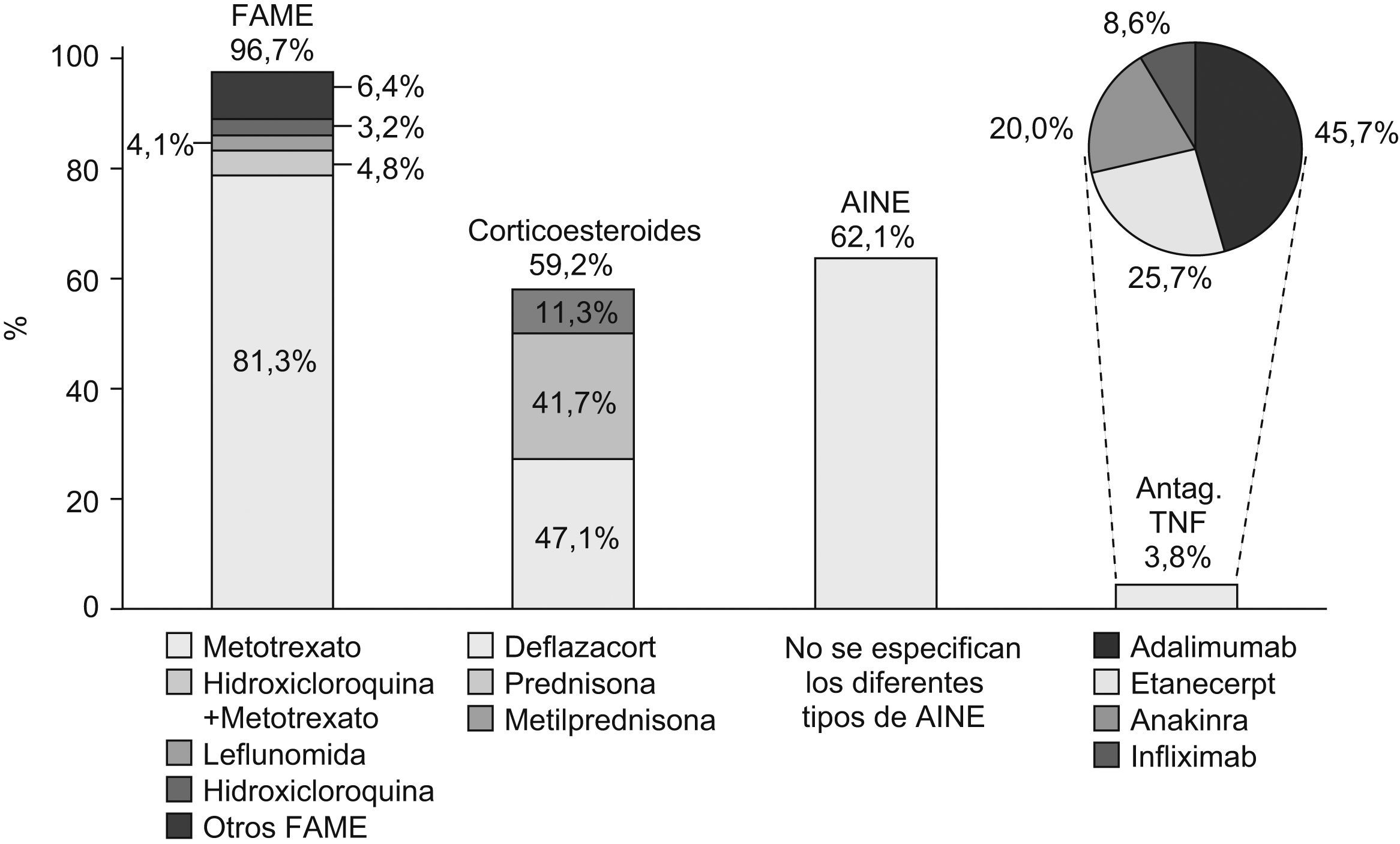
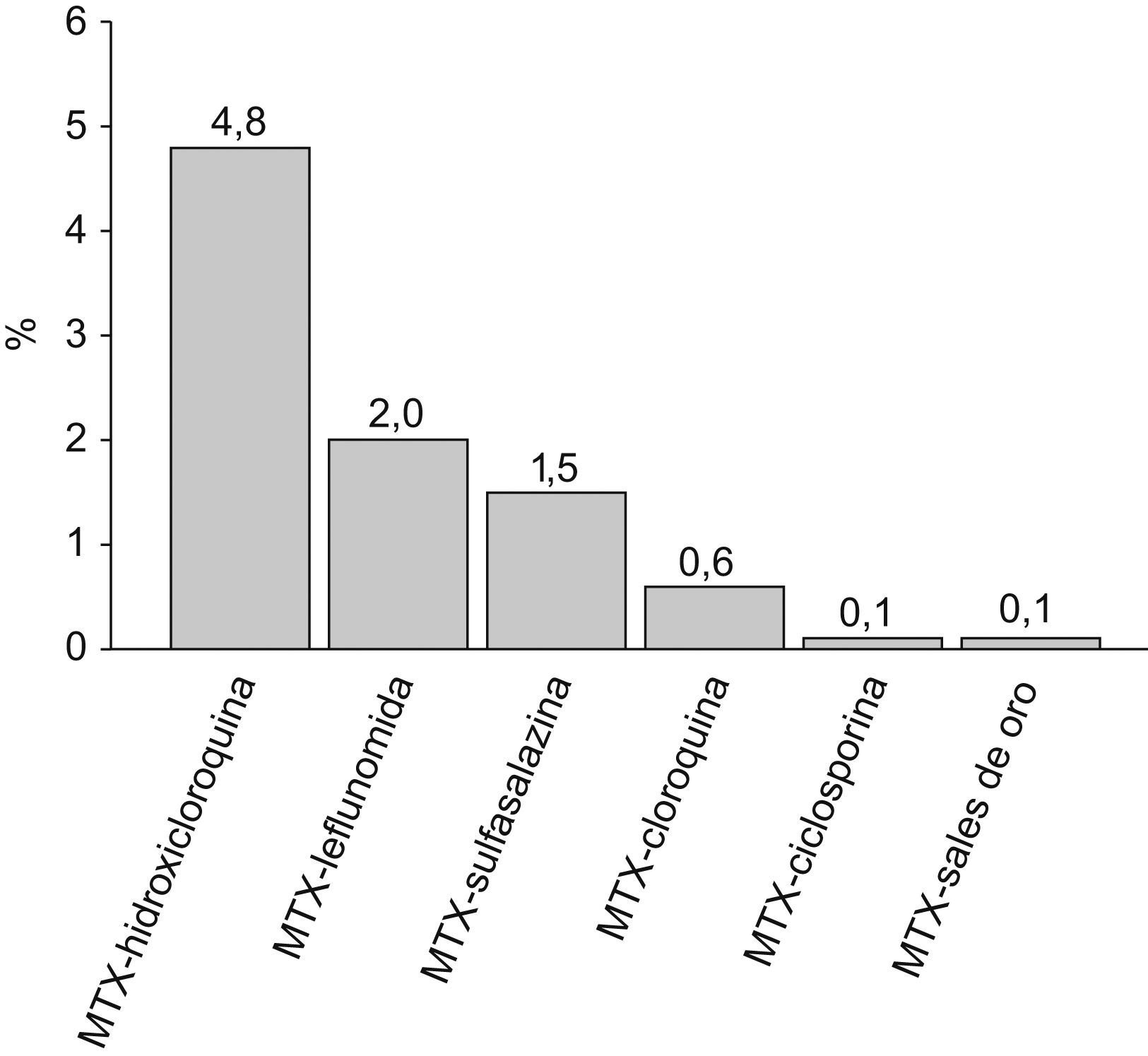
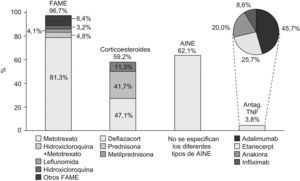
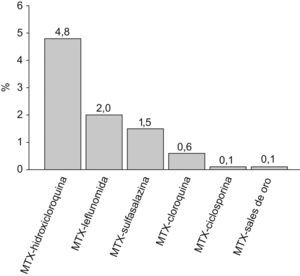
Descripción de la terapia utilizadaDel total de pacientes evaluados, al 96,7% se les instauró tratamiento con al menos un FAME, al 62,1% se les administraron AINEs, al 59,2% corticoesteroides (47,1% deflazacort y 41,7% prednisona) y al 3,8% una terapia biológica (fig. 2). En los pacientes que recibieron FAME, el 90,3% recibió tratamiento con un solo FAME, el 9,5% con 2 FAME y el 0,2% con 3 FAME. En politerapia, los FAME que más a menudo se administraron conjuntamente fueron MTX+Hidroxicloroquina (4,8%), MTX+Leflunomida (2,0%) y MTX+Sulfasalazina (1,5%) (fig. 3).
El FAME más frecuentemente utilizado en monoterapia fue el MTX (81,3%), seguido de la leflunomida (4,1%) y la hidroxicloroquina (3,2%) (fig. 2). La dosis media utilizada de MTX fue de 11,27 (3,5)mg/semana, siendo en este estudio el inyectable en jeringas precargadas la vía mayoritaria de administración de MTX (77,1%), seguido de la administración oral en comprimidos (21,6%). Del total de los pacientes que tomaban MTX, el 19,5% lo combinaban con AINE, el 16,5% con corticoesteroides y el 34,7% con corticoesteroides+AINE. De las terapias coadyuvantes, las más frecuentes fueron el ácido fólico (77,2% de los pacientes con MTX) y antiulcerosos (55,2% en combinación con MTX).
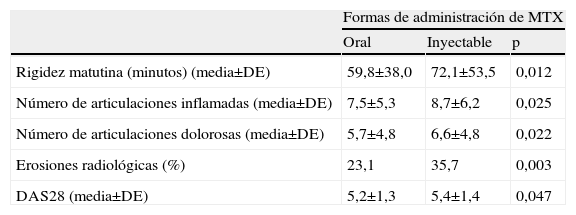
En el momento de instaurar el tratamiento farmacológico de primera línea, los pacientes que el médico decidió tratar con MTX inyectable mostraron mayor tiempo de rigidez matutina [72,1 (53,5) vs 59,8 (38,0) min, p=0,012], mayor porcentaje de erosiones radiológicas (35,7% vs 23,1%, p=0,003), mayor número de articulaciones tumefactas [8,7 (6,2) vs 7,5 (5,3), p=0,025] y dolorosas [6,6 (4,8) vs 5,7 (4,8), p=0,022] y un índice DAS28 mayor [5,4 (1,4) vs 5,2 (1,3), p=0,047] que aquellos que fueron tratados con MTX oral (tabla 2).
Datos clínicos de los pacientes tratados con MTX inyectable y oral
| Formas de administración de MTX | |||
| Oral | Inyectable | p | |
| Rigidez matutina (minutos) (media±DE) | 59,8±38,0 | 72,1±53,5 | 0,012 |
| Número de articulaciones inflamadas (media±DE) | 7,5±5,3 | 8,7±6,2 | 0,025 |
| Número de articulaciones dolorosas (media±DE) | 5,7±4,8 | 6,6±4,8 | 0,022 |
| Erosiones radiológicas (%) | 23,1 | 35,7 | 0,003 |
| DAS28 (media±DE) | 5,2±1,3 | 5,4±1,4 | 0,047 |
Los pacientes a los que se les administró terapia biológica (3,8% del total) tenían un tiempo medio desde el diagnóstico de 5 años, el 81,8% eran FR positivos, el 66,7% tenían más de 6 articulaciones dolorosas, el 72,7% más de 6 articulaciones tumefactas y el 51,5% presentaban erosiones radiológicas.
En el 89,6%, el tratamiento de primera elección fue el adecuado según las recomendaciones de la SER. Comparando los pacientes con artritis erosiva o no erosiva se observó un porcentaje mayor de no concordancia con las recomendaciones en la artritis no erosiva (12,5%) que en los pacientes con artritis erosiva (4,7%) (p=0,0009).
DiscusiónEn este estudio descriptivo de la AR se han incluido alrededor de 1.000 pacientes con AR o AP de toda la geografía española. Esta muestra representa un grupo de pacientes con características clínicas típicas y serológicas de la patología articular inflamatoria: más frecuente en mujeres, con una edad media de aproximadamente 50 años, el 60% de los pacientes son FR positivo, con reactantes de fase aguda como la VSG y PCR elevados y entre 6–8 articulaciones inflamadas y dolorosas.
Llama la atención que los pacientes con AR o AP son atendidos por los reumatólogos en sus consultas en un plazo medio de unos 6 meses desde el inicio de los síntomas. Este periodo representa un corto plazo de tiempo y parece lógico pensar que en esta reducción del tiempo que el paciente tarda en ser atendido por el reumatólogo influyen varios elementos entre los que se puede mencionar la existencia de consultas para la detección precoz de la AR que se han promovido desde la SER en los últimos años. Pero debemos mencionar que en el diseño de este estudio se descartó la inclusión de pacientes que se habían enviado a estas consultas. El motivo fue que, generalmente, estas consultas suelen utilizar protocolos establecidos de actuación y suelen formar parte de proyectos de investigación. Por el contrario, el objetivo de este trabajo fue describir de una forma lo más objetiva posible la situación de la AR en la práctica clínica habitual. Otros factores que han podido influir en esta reducción del tiempo para ser atendido por el reumatólogo son las campañas de divulgación y sensibilización de la población que se han realizado desde múltiples ámbitos con la finalidad de transmitir la idea de que las enfermedades reumáticas deben ser atendidas lo antes posible por el reumatólogo.
Otro dato interesante de este estudio es que los tratamientos con FAME se instauran de forma precoz. Esta decisión terapéutica está justificada por lo que actualmente conocemos, que el daño articular irreversible se produce en las primeras etapas de la enfermedad, y se estima que el momento óptimo para iniciar el tratamiento es en torno a los 3 primeros meses desde que se perciben los primeros síntomas. De esta forma, si la AR es tratada adecuadamente y de forma precoz se puede evitar la discapacidad que la artritis reumatoide puede conllevar con los años.
Prácticamente la totalidad de los pacientes de este estudio (96,7%) recibieron FAME como tratamiento de primera línea de su AR-AP. Este cambio en la utilización de los FAME desde el inicio de la enfermedad ha dejado definitivamente en el olvido la famosa pirámide del tratamiento de la AR. La monoterapia con FAME representa la opción más frecuentemente utilizada, y el MTX claramente es el fármaco seleccionado por prácticamente la totalidad de los reumatólogos para iniciar el tratamiento. El estudio muestra que el MTX inyectable en jeringas precargadas fue el FAME mas utilizado. Sin embargo este dato debe ser analizado con cuidado ya que el diseño del estudio facilitaba su uso. Otro dato interesante que se ha observado es que los pacientes tratados con MTX inyectable presentaban en el momento de iniciar el tratamiento, un peor estado de su patología, con mayor actividad inflamatoria y erosiones radiológicas que aquellos que fueron tratados con MTX oral. Esta práctica terapéutica está en la línea de las recomendaciones del EULAR para el uso del MTX en la AR13. Este mismo planteamiento fue hecho por los reumatólogos en el momento de prescribir una terapia biológica.
Finalmente, el estudio refleja que la gran mayoría de los reumatólogos españoles utilizan las recomendaciones de la SER para iniciar el tratamiento de la AR o AP. Esto demuestra que la práctica clínica reumatológica española está consiguiendo un grado alto de homogeneización en el tratamiento de la AR. Estos resultados también son concordantes con los obtenidos en el estudio EMECAR (Estudio de la Morbilidad y Expresión Clínica de la Artritis Reumatoide), en el cual se confirma la existencia de un importante cambio en el tratamiento de la AR en los últimos 5 años.
Conflicto de interesesJordi Galván es Director Médico de Gebro Pharma, S.A.-Barcelona-España; Esta empresa financió el proyecto.