Determinar la prevalencia y correlación clínica de los anticuerpos antirribosomal P en lupus eritematoso sistémico (LES) juvenil y compararlos con LES del adulto.
MétodosSe incluyeron en el estudio 30 pacientes con LES juvenil y 92 pacientes con LES del adulto. Consideramos LES de comienzo juvenil a todos aquellos pacientes que comenzaron su enfermedad antes de los 16 años. Se consideraron las manifestaciones clínicas y serológicas que presentaron los pacientes desde el diagnóstico hasta el momento de inclusión en el estudio (manifestaciones acumuladas). El anticuerpo antirribosomal P fue evaluado mediante la técnica de enzimo-inmunoensayo (ELISA).
ResultadosLa presencia de antirribosomal P fue significativamente mayor en el grupo de pacientes con LES juvenil comparado con LES del adulto (26,7% vs. 6,5%; OR=5,21 [IC95%=1,6-16,5], p=0,003). La alopecía (OR=10,11; IC95%=1,25-97) y rash cutáneo (no discoide) (OR=4,1; IC95%=1,25-13,89) fueron las únicas manifestaciones clínicas que se asociaron en forma estadísticamente significativa con la presencia del anticuerpo antirribosomal P.
ConclusiónEste estudio confirma una mayor prevalencia de anticuerpos antirribosomal P en pacientes con LES juvenil. La alopecia y el rash cutáneo fueros las únicas manifestaciones clínicas asociadas a la presencia de antirribosomal P.
To investigate the prevalence and associations with clinical manifestations of anti- P ribosomal antibodies in patients with juvenile-onset and adult-onset systemic lupus erythematosus (SLE).
MethodsClinical and serological data of 30 patients with juvenile-onset SLE (age at onset younger than 16 years old) were compared with data of 92 patients with adult-onset SLE. Symptoms occurring during the entire disease course were considered. Anti- P ribosomal antibodies were tested by ELISA.
ResultsAnti- P ribosomal antibodies were found significantly more often in pediatric-onset SLE patients (26.7% vs. 6.5%; OR=5.21 [CI95%=1.6-16.5], p=0.003). Alopecia (OR=10.11, CI 95%=1.25-97) and skin rash (non discoid) (OR=4.1, CI 95%=1.25-13.89) were significantly associated with anti- P ribosomal antibodies.
ConclusionAnti-ribosomal P antibodies are more often found in patients with juvenile SLE. Alopecia and skin rash were the only clinical manifestations associated to anti-ribosomal P antibodies.
El lupus eritematoso sistémico (LES) es una enfermedad autoinmune que puede afectar virtualmente cualquier órgano o sistema, clínicamente evoluciona con exacerbaciones y remisiones y serológicamente se caracteriza por la presencia de anticuerpos antinucleares (AAN), anti-DNA nativo y anti-Sm. Si bien es más común en adultos, un 15-20% de los pacientes con LES se diagnostican por primera vez antes de los 16 años1–3. En los pacientes con LES juvenil la edad de mayor incidencia es entre los 12 y 14 años, siendo infrecuente antes de los 5 años4.
El anticuerpo antirribosomal P es un anticuerpo dirigido contra una familia de fosfoproteínas asociadas a la subunidad ribosomal 60s. Los anticuerpos están dirigidos contra tres fosfoproteínas P0 (38kD), P1 (19kD), y P2 (17kD). Varios estudios clínicos han observado diferencias clínicas y serológicas entre pacientes con LES juvenil y del adulto. La enfermedad en los pacientes con LES juvenil es más grave, los tratamientos utilizados son más agresivos y acumulan mayor daño durante su evolución3,5. Esto se debe a una mayor incidencia de compromiso renal y del sistema nervioso central observado en pacientes menores de 16 años1,6–9.
Se ha reportado en la literatura una elevada prevalencia de anticuerpos antirribosomal P en algunas series de pacientes con LES juvenil10,11, mientras que otros grupos han encontrado una mayor prevalencia de anti-ADN nativo, anti-nRNP y anti-Sm12,13. La prevalencia de anticuerpos antirribosomal P en pacientes con LES varía del 6 al 36% dependiendo de la etnia, la edad y las variables clínicas analizadas14–16.
Los anticuerpos antirribosomal P se han asociado con la presencia de nefritis17–21, hepatitis autoimmune22,23 y compromiso neurológico24–27. Tres estudios evaluaron la prevalencia y asociación con manifestaciones clínicas del antirribosomal P en población juvenil, los hallazgos de estos estudios difieren entre sí7,11,28.
No hay datos en la literatura sobre la prevalencia de antirribosomal P y su asociación con manifestaciones clínicas en pacientes argentinos.
El objetivo de nuestro estudio fue determinar la prevalencia y correlación clínica en pacientes argentinos, de los anticuerpos antirribosomal P en LES juvenil y compararlos con los LES del adulto. Se plantea como objetivo secundario comparar las manifestaciones clínicas acumuladas del LES juvenil y del adulto.
Pacientes y métodosPacientesTodos los pacientes incluidos en el presente estudio cumplieron con cuatro o más criterios clasificatorios de LES del Colegio Americano de Reumatología revisados en 199729,30. Consideramos LES juvenil a todos aquellos pacientes que comenzaron su enfermedad antes de los 16 años. Se incluyeron en el estudio 30 pacientes con LES juvenil y 92 pacientes con LES del adulto, provenientes de siete centros de referencia de Argentina: Centro de Educación Médica y de Investigaciones Clínicas Norberto Quirno (CEMIC), Hospital Italiano de Buenos Aires, Hospital General de Agudos José Penna, Hospital de Clínicas José de San Martín, Hospital General de Agudos Juan Antonio Fernández, Hospital San Martín de La Plata, Hospital Británico de Buenos Aires y Hospital de Pediatría Prof. Dr. Juan P. Garrahan.
Datos clínicosSe diseñó un cuestionario específico para el estudio, donde se recogieron los datos clínicos sobre la base del interrogatorio y la revisión de la historia clínica del paciente. Se detallaron las manifestaciones clínicas que presentaron los pacientes desde el diagnóstico hasta el momento de inclusión en el estudio (manifestaciones acumuladas). Se consideraron las siguientes manifestaciones: rash discoide, úlceras orales, fotosensibilidad, alopecia, eritema malar, fenómeno de Raynaud, leucopenia, anemia hemolítica, plaquetopenia, serositis, artritis, psicosis, convulsiones, neuropatía, mielitis transversa, estado confusional agudo, glomerulonefritis, vasculitis, boca seca, ojo seco. Se obtuvo información sobre el tratamiento recibido desde el diagnóstico de la enfermedad hasta la inclusión en el estudio. Se calculó score de actividad utilizando el score Systemic Lupus Erythematosus disease activity index (SLEDAI) en el momento de recolección de la muestra.Se registraron además los resultados de anticuerpos presentes durante la historia del paciente (AAN, anti-DNA, anti-Ro/SSA, anti-La/SSB, anti-Sm y anti-nRNP).
Todos los participantes firmaron el consentimiento informado; el estudio fue realizado después de ser aprobado por los respectivos comités de ética de cada institución.
Recolección de muestras y determinaciones de laboratorioLas muestras de sangre para la determinación de los anticuerpos fueron tomadas en los centros participantes, y fueron analizadas de forma centralizada en el laboratorio de Inmunología y Reumatología del CEMIC. La medición de anticuerpos anti-Ro/SSA, anti-La/SSB, anti-Sm y anti-nRNP se realizó por técnica de doble-difusión. El anticuerpo antirribosomal P fue evaluado mediante la técnica de enzimo-inmunoensayo (ELISA) utilizando como antígeno, proteína purificada a partir de timo bovino y/o conejo (ImmunoVision, Inc.) absorbida a razón de 0,5 ug por well (placa de poliestireno Maxisorb; Nunc). Las muestras fueron consideradas positivas con valores ≥11 U. La medición de anti-Ro/SSA, anti-La/SSB, anti-Sm y anti-nRNP y antirribosomal P se realizó al mismo tiempo en todas las muestras.
Análisis estadísticoLas variables cualitativas se presentan como número y porcentaje y las cuantitativas como media/mediana y sus desvíos estándar/valores mínimos y máximos. Para determinar asociación se utilizaron la prueba de chi-cuadrado (χ2) o test exacto de Fisher. Para cuantificar fuerza de asociación se determinaron los odds ratios (OR) y sus intervalos de confianza 95% (IC95%). Para el análisis del SLEDAI en pacientes antirribosomal P positivos y negativo y en adultos vs. juveniles se utilizaron las pruebas de Wilcoxon y Mann-Whitney. Se consideró como significativa una p<0,05. El análisis estadístico fue realizado utilizando el paquete estadístico Epi Info™ 7 (Centers for Disease Control and Prevention [CDC]).
ResultadosDatos demográficosVeinticuatro pacientes (80%) en el grupo juvenil y 81 (88%) en los adultos eran de etnia caucásica. Dos (6,7%) de los pacientes con LES juvenil y 6 (6,5%) pacientes en el grupo de LES del adulto fueron de sexo masculino. La media de edad al diagnóstico en los pacientes con LES juvenil fue de 12,67±3,56 y en los adultos de 30±11,46 años. La media de edad de los pacientes en el momento de la inclusión en el estudio fue de 22,9±8,4 y 39,76±12,37 años para el grupo de LES juvenil y del adulto respectivamente; la media de tiempo de evolución de la enfermedad en el momento de la inclusión en el estudio fue de 10,63±7,16 años en los juveniles y de 9,36±7,75 años en los adultos.
Manifestaciones clínicas y tratamientos recibidos:
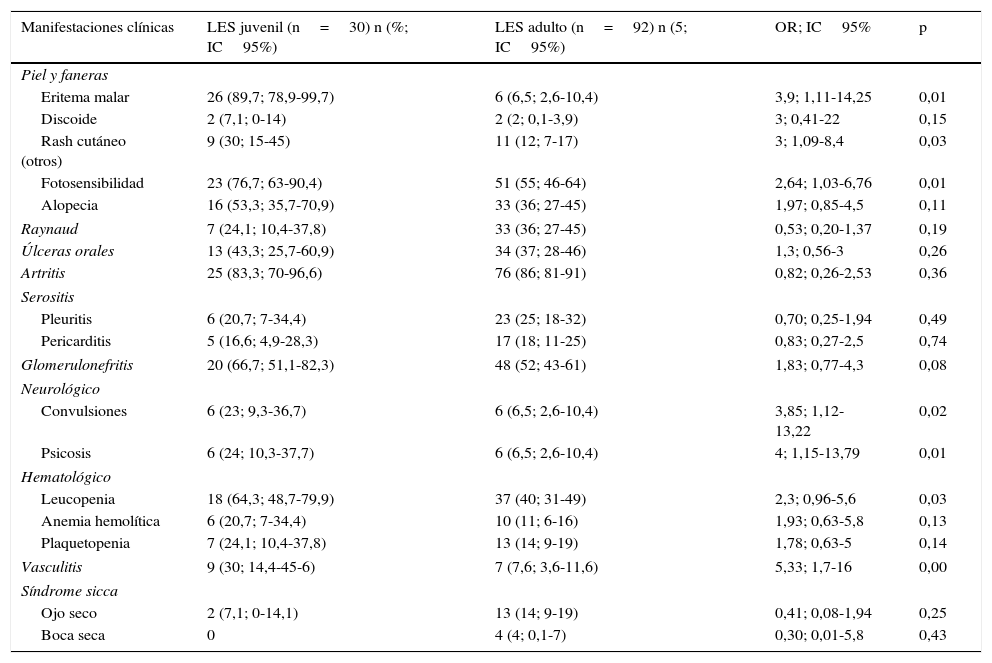
La prevalencia de las diferentes manifestaciones clínicas en los dos grupos (adultos y juveniles) se detalla en la tabla 1. El eritema malar (OR=3,9; IC95%=1,11-14,25), la fotosensibilidad (OR=2,64; IC95%=1,03-6,76), la presencia de vasculitis (OR=5,33; IC95%=1,7-16,0), rash cutáneo no discoide (OR=3,0; IC95%=1,09-8,4) y compromiso neurológico: convulsiones OR=3,85; (IC95%=1,12-13,22) y psicosis OR=4; (IC95%=1,15-13,79) se encontraron con mayor frecuencia en el grupo de LES juvenil. Cinco pacientes adultas desarrollaron manifestaciones neurológicas (no criterio ACR): deterioro cognitivo en 3 pacientes, polineuropatía periférica sensitiva de miembros inferiores una paciente y estado confusional agudo una paciente. Ninguna paciente presentó mielitis transversa, o mononeuritis múltiple.
Prevalencia de manifestaciones clínicas: LES juvenil comparado con LES del adulto
| Manifestaciones clínicas | LES juvenil (n=30) n (%; IC95%) | LES adulto (n=92) n (5; IC95%) | OR; IC95% | p |
|---|---|---|---|---|
| Piel y faneras | ||||
| Eritema malar | 26 (89,7; 78,9-99,7) | 6 (6,5; 2,6-10,4) | 3,9; 1,11-14,25 | 0,01 |
| Discoide | 2 (7,1; 0-14) | 2 (2; 0,1-3,9) | 3; 0,41-22 | 0,15 |
| Rash cutáneo (otros) | 9 (30; 15-45) | 11 (12; 7-17) | 3; 1,09-8,4 | 0,03 |
| Fotosensibilidad | 23 (76,7; 63-90,4) | 51 (55; 46-64) | 2,64; 1,03-6,76 | 0,01 |
| Alopecia | 16 (53,3; 35,7-70,9) | 33 (36; 27-45) | 1,97; 0,85-4,5 | 0,11 |
| Raynaud | 7 (24,1; 10,4-37,8) | 33 (36; 27-45) | 0,53; 0,20-1,37 | 0,19 |
| Úlceras orales | 13 (43,3; 25,7-60,9) | 34 (37; 28-46) | 1,3; 0,56-3 | 0,26 |
| Artritis | 25 (83,3; 70-96,6) | 76 (86; 81-91) | 0,82; 0,26-2,53 | 0,36 |
| Serositis | ||||
| Pleuritis | 6 (20,7; 7-34,4) | 23 (25; 18-32) | 0,70; 0,25-1,94 | 0,49 |
| Pericarditis | 5 (16,6; 4,9-28,3) | 17 (18; 11-25) | 0,83; 0,27-2,5 | 0,74 |
| Glomerulonefritis | 20 (66,7; 51,1-82,3) | 48 (52; 43-61) | 1,83; 0,77-4,3 | 0,08 |
| Neurológico | ||||
| Convulsiones | 6 (23; 9,3-36,7) | 6 (6,5; 2,6-10,4) | 3,85; 1,12-13,22 | 0,02 |
| Psicosis | 6 (24; 10,3-37,7) | 6 (6,5; 2,6-10,4) | 4; 1,15-13,79 | 0,01 |
| Hematológico | ||||
| Leucopenia | 18 (64,3; 48,7-79,9) | 37 (40; 31-49) | 2,3; 0,96-5,6 | 0,03 |
| Anemia hemolítica | 6 (20,7; 7-34,4) | 10 (11; 6-16) | 1,93; 0,63-5,8 | 0,13 |
| Plaquetopenia | 7 (24,1; 10,4-37,8) | 13 (14; 9-19) | 1,78; 0,63-5 | 0,14 |
| Vasculitis | 9 (30; 14,4-45-6) | 7 (7,6; 3,6-11,6) | 5,33; 1,7-16 | 0,00 |
| Síndrome sicca | ||||
| Ojo seco | 2 (7,1; 0-14,1) | 13 (14; 9-19) | 0,41; 0,08-1,94 | 0,25 |
| Boca seca | 0 | 4 (4; 0,1-7) | 0,30; 0,01-5,8 | 0,43 |
Los pacientes utilizaron los siguientes tratamientos inmunosupresores: metotrexato (MTX), micofenolato mofetil (MMF), azatioprina (AZA), ciclofosfamida (CF), glucocorticoides (prednisona o equivalente) >20mg no hubo diferencias estadísticamente significativas entre pacientes adultos y juveniles ni entre los pacientes antirribosomal P positivos o negativos (datos no mostrados). Los pacientes adultos recibieron con mayor frecuencia que los juveniles hidroxicloroquina (95,6%; vs. 83,3% p=0,025).
El score SLEDAI en la población total (adultos y juveniles) fue media 3,89 (DS 4,68), en los pacientes con LES juvenil media 5,11 (DS 5,33) y en adultos media 3,56 (DS 4,44) p=0,09
Prevalencia de autoanticuerposLa prevalencia de anticuerpos se detalla en la tabla 2. De los anticuerpos determinados la presencia de antirribosomal P (OR=5,21; IC95%=1,6-16,5) fue significativamente mayor en el grupo de pacientes con LES juvenil.
Prevalencia de autoanticuerpos en pacientes con LES juvenil comparado con LES del adulto
| Autoanticuerpo | LES juvenil n=30 | LES adulto n=92 | OR; 95%IC | p |
|---|---|---|---|---|
| Antirribosomal P; n (%) | 8 (26,7) | 6 (6,5) | 5,21; 1,6-16,5 | 0,003 |
| Anti-La/SSB; n (%) | 0 | 6 (6,5) | 0,23; 0,01-4.3 | 0,33 |
| Anti-Ro/SSA; n (%) | 5 (16,6) | 29 (31,5) | 0,47; 0,16-1,38 | 0,17 |
| Anti-Sm; n (%) | 3 (10) | 5 (5,4) | 2,1;0,47-9,5 | 0,32 |
| Anti-nRNP; n (%) | 7 (23,3) | 20 (21,7) | 1,22; 0,45-3,3 | 0,68 |
En tabla 3 se detalla la prevalencia de otros autoanticuerpos en pacientes con LES juvenil y del adulto, según sean estos antirribosomal P positivos o negativos. La prevalencia de todos los otros autoanticuerpos fue similar en ambos grupos.
Prevalencia de otros autoanticuerpos en pacientes con antirribosomal P positivo y negativo
| Autoanticuerpo | Antirribosomal P (+) n=14 | Antirribosomal P (-) n=108 | OR (95% IC) | p |
|---|---|---|---|---|
| Anti-La/SSB; n (%) | 0 | 6 (5,5) | 0,61; 0,03-11,6 | 0,74 |
| Anti-Ro/SSA; n (%) | 3 (21) | 31 (29) | 0,80; 0,20-3,1 | 0,75 |
| Anti-Sm; n (%) | 2 (14) | 6 (5,5) | 3,33; 0,59-18,7 | 0,17 |
| Anti-nRNP; n (%) | 3 (21) | 24 (22) | 1,13; 0,28-4,54 | 0,85 |
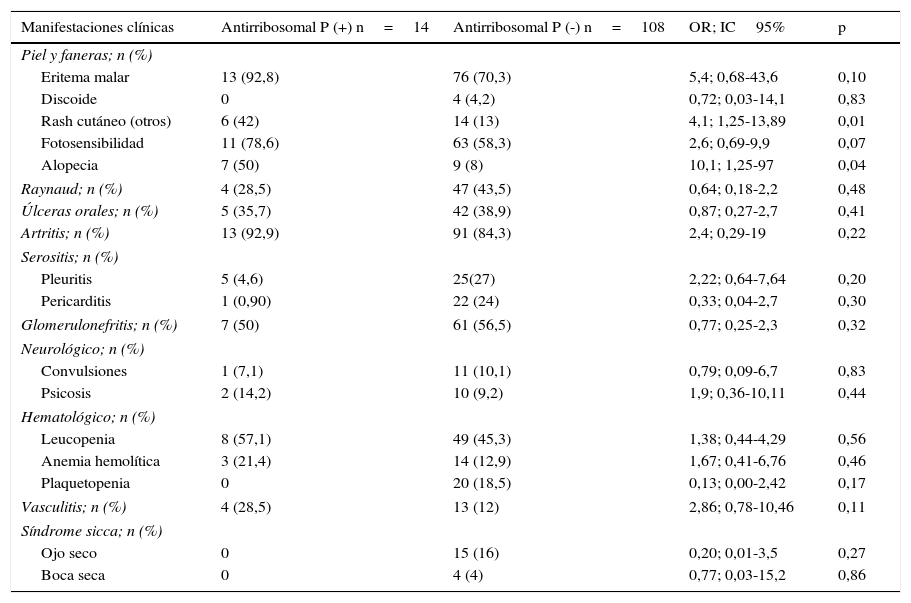
En la tabla 4 se detalla la prevalencia del anticuerpo antirribosomal P según las manifestaciones clínicas. La alopecía (OR=10,11; IC95%=1,25-97) y rash cutáneo (no discoide) (OR=4,1; IC95%=1,25-13,89) fueron las únicas manifestaciones clínicas que se asociaron en forma estadísticamente significativa con la presencia del anticuerpo antirribosomal P.
Diferencias en las manifestaciones clínicas entre pacientes antirribosomal P positivos y negativos
| Manifestaciones clínicas | Antirribosomal P (+) n=14 | Antirribosomal P (-) n=108 | OR; IC95% | p |
|---|---|---|---|---|
| Piel y faneras; n (%) | ||||
| Eritema malar | 13 (92,8) | 76 (70,3) | 5,4; 0,68-43,6 | 0,10 |
| Discoide | 0 | 4 (4,2) | 0,72; 0,03-14,1 | 0,83 |
| Rash cutáneo (otros) | 6 (42) | 14 (13) | 4,1; 1,25-13,89 | 0,01 |
| Fotosensibilidad | 11 (78,6) | 63 (58,3) | 2,6; 0,69-9,9 | 0,07 |
| Alopecia | 7 (50) | 9 (8) | 10,1; 1,25-97 | 0,04 |
| Raynaud; n (%) | 4 (28,5) | 47 (43,5) | 0,64; 0,18-2,2 | 0,48 |
| Úlceras orales; n (%) | 5 (35,7) | 42 (38,9) | 0,87; 0,27-2,7 | 0,41 |
| Artritis; n (%) | 13 (92,9) | 91 (84,3) | 2,4; 0,29-19 | 0,22 |
| Serositis; n (%) | ||||
| Pleuritis | 5 (4,6) | 25(27) | 2,22; 0,64-7,64 | 0,20 |
| Pericarditis | 1 (0,90) | 22 (24) | 0,33; 0,04-2,7 | 0,30 |
| Glomerulonefritis; n (%) | 7 (50) | 61 (56,5) | 0,77; 0,25-2,3 | 0,32 |
| Neurológico; n (%) | ||||
| Convulsiones | 1 (7,1) | 11 (10,1) | 0,79; 0,09-6,7 | 0,83 |
| Psicosis | 2 (14,2) | 10 (9,2) | 1,9; 0,36-10,11 | 0,44 |
| Hematológico; n (%) | ||||
| Leucopenia | 8 (57,1) | 49 (45,3) | 1,38; 0,44-4,29 | 0,56 |
| Anemia hemolítica | 3 (21,4) | 14 (12,9) | 1,67; 0,41-6,76 | 0,46 |
| Plaquetopenia | 0 | 20 (18,5) | 0,13; 0,00-2,42 | 0,17 |
| Vasculitis; n (%) | 4 (28,5) | 13 (12) | 2,86; 0,78-10,46 | 0,11 |
| Síndrome sicca; n (%) | ||||
| Ojo seco | 0 | 15 (16) | 0,20; 0,01-3,5 | 0,27 |
| Boca seca | 0 | 4 (4) | 0,77; 0,03-15,2 | 0,86 |
El score SLEDAI en la población con antirribosomal P negativo fue media: 3,93 (DS 4,76) y en los pacientes con antirribosomal P positivo media: 3,58 (DS 4,12) p=0,97.
DiscusiónEn nuestro estudio hemos analizado las características clínicas y de laboratorio de pacientes con LES que comenzaron su enfermedad antes de los 16 años (juvenil) y los comparamos con pacientes con LES del adulto. La presencia de eritema malar, fotosensibilidad, vasculitis, rash cutáneo y compromiso neurológico (convulsiones y psicosis) fue más frecuente en los pacientes con LES juvenil. Cuando comparamos el perfil de los autoanticuerpos entre ambos grupos de pacientes, encontramos que el anticuerpo antirribosomal P fue significativamente más prevalente en los LES juvenil (27% vs. 5,62%). No encontramos asociación del anticuerpo antirribosomal P con otros autoanticuerpos. La alopecia y rash cutáneo (no discoide) fueron las únicas manifestaciones clínicas que se asociaron en forma estadísticamente significativa con la presencia del anticuerpo antirribosomal P.
La mayoría de los estudios reportados con anterioridad, coinciden en que hay una mayor prevalencia de anticuerpos antirribosmal P en los LES juveniles; nuestro estudio confirmó estos hallazgos. Es conocido que ciertas características de la población en estudio, como la etnia, el estado de la enfermedad (mayor prevalencia de anticuerpos antirribosomal P en LES activo) y la intensidad del tratamiento hacen que la prevalencia de este autoanticuerpo sea variable, y difiera entre los distintos estudios. Reichlin et al.11 reportaron una prevalencia del anticuerpo antirribosomal P de 42% en pacientes con LES juvenil donde un gran porcentaje de ellos presentaba LES activo. Hoffmann et al.7, a diferencia de los autores anteriores, encontraron una prevalencia del 25%, y Press et al.31 en su estudio publicado previamente reportaron una prevalencia del 20%. En estos dos últimos trabajos no hubo detalles sobre la actividad de la enfermedad y mostraron una prevalencia de antirribosomal P similar a nuestro estudio. Existe gran discrepancia en la literatura respecto a la asociación entre el anticuerpo antirribosomal P y las diferentes manifestaciones clínicas en los LES juveniles. Reichlin et al.11 hallaron que el antirribosomal P se asoció al compromiso renal. Todo lo contrario fue reportado por Hoffman et al.7, quienes describieron que la presencia del antirribosomal P en ausencia de anti-DNA se comportaba como protector del compromiso renal. En la población de LES del adulto, otros autores encontraron asociación entre antirribosomal P y la presencia de nefropatía membranosa20. Al igual que nosotros, Press et al.31 no encontraron ninguna asociación entre este autoanticuerpo y el compromiso renal.
La asociación del anticuerpo antirribosomal P con las manifestaciones neurológicas en pacientes con LES juvenil también es controvertida. Aldar et al.28 observaron mayor frecuencia del autoanticuerpo en pacientes con LES juvenil y ansiedad, pero no con otras manifestaciones clínicas más graves del sistema nervioso central. Reichlin et al.11 y Hoffman et al.7 no mencionaron en sus trabajos la asociación entre el antirribosomal P y el compromiso neurológico. En nuestro estudio, si bien encontramos una mayor prevalencia de manifestaciones clínicas neurológicas (psicosis y convulsiones) en LES juvenil, no hallamos una asociación estadísticamente significativa entre el anticuerpo antirribosomal P y dichas manifestaciones, ya sea en el análisis de la población total de pacientes estudiados como en la de LES juvenil en particular.
Se ha reportado la correlación del antirribosomal P con actividad de la enfermedad medida por SLEDAI y con la presencia de anti-DNA. En nuestro estudio no se encontró relación entre la actividad de la enfermedad medida por SLEDAI y la presencia de antirribosomal P31.
Una de las limitaciones más importantes de nuestro estudio es el número reducido de pacientes con LES juvenil debido a dificultades en el reclutamiento. El anticuerpo antirribosomal P fue medido en una única oportunidad, por lo tanto podríamos no haber detectado el anticuerpo en pacientes que estén inactivos en el momento de la toma de la muestra. Por otro lado, en la muestra hay solo 14 pacientes con antirribosomal P positivo, esto puede haber limitado la posibilidad de encontrar asociaciones estadísticamente significativas entre el anticuerpo y las manifestaciones clínicas.
A pesar de las limitaciones, este estudio confirma la prevalencia aumentada de anticuerpos antirribosomal P en pacientes con LES juvenil y no encuentra asociación del anticuerpo con manifestaciones renales y del SNC. La alopecia y rash cutáneo (no discoide) fueron las únicas manifestaciones clínicas que se asociaron en forma estadísticamente significativa con la presencia del anticuerpo antirribosomal P.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.