El tratamiento con agentes contra el factor de necrosis tumoral (TNF) alfa se ha asociado a la reactivación de la infección crónica por el virus de la hepatitis B. Algunos casos publicados indican la necesidad de tratamiento crónico con lamivudina cuando se utilizan los agents anti-TNFa. Describimos el caso de un paciente con espondilitis anquilosante y antígeno de superficie positivo tratado con infliximab y lamivudina. La respuesta clínica fue excelente, pero cuando el paciente interrumpió el tratamiento con lamivudina, se observó reactivación de la replicación viral. Una vez reinstaurado dicho tratamiento, se controló nuevamente la replicación viral y se normalizaron las concentraciones de transaminasas. Esta observación indica que en pacientes con infección crónica por VHB que necesitan tratamiento anti-TNFa, se requiere un tratamiento preventivo a largo plazo con lamivudina.
Anti-tumor necrosis factor-a (TNF) therapy has been associated with reactivation of hepatitis B virus infection. Case reports have suggested the concomitant need of lamivudine treatment in patients with HBV infection treated with antiTNFa agents. We describe a case of ankylosing spondylitis with positive HBV surface antigen (HBsAg) treated with infliximab and lamivudine. Clinical response was excellent but when lamivudine therapy was stopped, reactivation of replication viral occurred. After the reintroduction of lamivudine, viral replication was controlled and liver function tests were normalized. Preventive long-term lamivudine therapy is mandatory when anti-TNFa therapy is maintained in patients with chronic HBV infection.
El infliximab, un anticuerpo monoclonal quimérico contra el factor de necrosis tumoral (TNF) alfa, es un tratamiento de amplio uso en espondiloartritis, artritis reumatoide y enfermedad de Crohn. Desde la aprobación de su uso se siguen planteando cuestiones sobre su seguridad. Aunque se mantiene el debate sobre la seguridad del tratamiento antagonista del TNFα en la infección crónica por el virus de la hepatitis C, los datos publicados indican que su uso es relativamente seguro1,2. Por el contrario, en la infección crónica por el virus de la hepatitis B (VHB) parece cada vez más evidente por los casos publicados que se produce una reactivación del virus cuando se instaura tratamiento con agentes anti-TNFα3–10. La infección por el VHB es una de las infecciones virales crónicas más frecuentes en el mundo y afecta aproximadamente a 400 millones de personas11. Describimos el caso de un paciente con espondilitis anquilosante (EA) e infección crónica por el VHB tratado con lamivudina e infliximab.
Caso clínicoSe trata de un varón de 32 años de raza blanca, diagnosticado de EA en 1996, que cumplía criterios modificados de New York. El perfil serológico para el VHB era HBsAg positivo, anticuerpos anti-HBe y HBc positivos, antígeno HBe y anticuerpos anti-HBs negativos. Las determinaciones de ALT y AST se habían mantenido siempre dentro de los límites normales. Desde 1996 había recibido tratamiento con sulfasalazina y diferentes antiinflamatorios no esteroideos (AINE), a pesar de lo cual la EA se mantenía persistentemente activa, con BASDAI de 6 (0–10), BASFI de 50 (0–100), dolor nocturno de 7 (0–10) y proteína C reactiva (PCR) de 16,3mg/dl, por lo que se planteó al paciente tratamiento con infliximab.
En abril de 2004 la determinación de la carga de ADN del VHB era de 237 copias/ml. Antes de recibir infliximab se inició tratamiento con lamivudina, 100mg diarios. En noviembre de 2004 la carga viral era menor de 200 copias/ml (tabla 1). El paciente firmó consentimiento informado y comenzó el tratamiento con infliximab, en abril de 2005, a dosis de 5mg/kg en semanas 0, 2, 6 y posteriormente cada 8 semanas. En la semana 12 alcanzó una mejoría del BASDAI del 70% y se normalizó la PCR. Durante el seguimiento, a partir de junio de 2005, tras haber recibido 4 infusiones de infliximab, se detectó un aumento de la replicación viral, con elevación coincidente de las transaminasas. El paciente reconoció haber abandonado la lamivudina 4 meses antes. Se decidió reinstaurar el tratamiento con lamivudina suspendiendo temporalmente el infliximab y controlando periódicamente la replicación viral y las concentraciones de transaminasas. El paciente continuó recibiendo tratamiento con infliximab y lamivudina, con buen control de los síntomas de la EA (BASDAI < 2) y valores normales de transaminasas con control de la replicación viral (tabla 1).
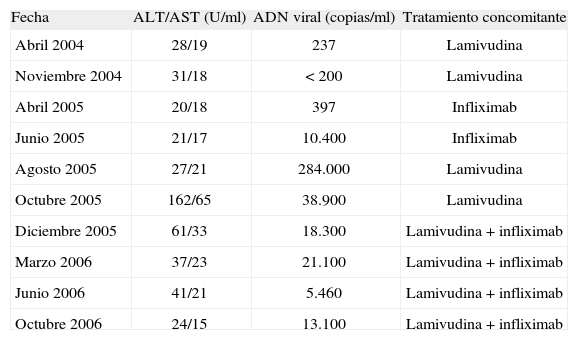
Concentraciones de transaminasas y de ADN viral durante el tratamiento con infliximab y lamivudina
| Fecha | ALT/AST (U/ml) | ADN viral (copias/ml) | Tratamiento concomitante |
| Abril 2004 | 28/19 | 237 | Lamivudina |
| Noviembre 2004 | 31/18 | < 200 | Lamivudina |
| Abril 2005 | 20/18 | 397 | Infliximab |
| Junio 2005 | 21/17 | 10.400 | Infliximab |
| Agosto 2005 | 27/21 | 284.000 | Lamivudina |
| Octubre 2005 | 162/65 | 38.900 | Lamivudina |
| Diciembre 2005 | 61/33 | 18.300 | Lamivudina + infliximab |
| Marzo 2006 | 37/23 | 21.100 | Lamivudina + infliximab |
| Junio 2006 | 41/21 | 5.460 | Lamivudina + infliximab |
| Octubre 2006 | 24/15 | 13.100 | Lamivudina + infliximab |
Los datos publicados indican que la administración de infliximab en pacientes con infección crónica por el VHB condiciona un mayor riesgo de reactivación del virus, pero que es factible controlar este riesgo con el tratamiento concomitante con lamivudina.
La lamivudina es un antirretroviral inhibidor de la transcriptasa inversa que ha demostrado eficacia en el control de la reactivación viral en pacientes con infección crónica por el VHB que reciben quimioterapia por neoplasias oncohematológicas y por trasplantes de órganos12–14. Aunque los mecanismos patogénicos no están completamente claros, en estudios experimentales in vitro y en modelos animales se ha observado que el TNF inhibe la replicación del VHB y estimula una respuesta celular T-específica que implicaría la eliminación del virus de los hepatocitos infectados15–17. Según estos hallazgos cabe pensar que la administración de antagonistas del TNFα incrementaría la expresión de los antígenos virales y la reactivación de la replicación viral.
Se han comunicado varios casos de infección crónica por VHB y tratamiento con infliximab en enfermedad de Crohn, espondiloartritis y artritis reumatoide. Ya que en la enfermedad de Crohn el uso de infliximab se limita, en muchos casos, a 3 dosis, se discutirá fundamentalmente la enfermedad reumática que requiere de una administración continuada de infliximab.
Oniankitan et al9 comunicaron un caso de EA con infección crónica por VHB tratado con infliximab y metotrexato durante 1 año sin deterioro de la función hepática. En este caso, 1 año antes de recibir infliximab, había estado en tratamiento con lamivudina y la replicación viral se mantenía estable. Wendling et al8 publicaron otro caso de EA con infección crónica por VHB que recibió metotrexato e infliximab con buena respuesta terapéutica. Durante el seguimiento, las transaminasas comenzaron a aumentar, así como la replicación viral. Cuatro meses después se inició tratamiento con lamivudina, las transaminasas volvieron a límites normales y la carga viral se hizo indetectable. Ostuni et al3 comunicaron un caso de artritis reumatoide e infección por VHB tratado con metotrexato e infliximab que desarrolló una hepatitis aguda y que al suspender el tratamiento e iniciar lamivudina se normalizaron las transaminasas y se controló la replicación viral. Nuestro caso confirma estos hallazgos. Además nuestro caso ejemplifica que mientras se mantiene el tratamiento con lamivudina la replicación se controla, se incrementa rápidamente al suspenderla y al reinstaurarlo se consigue el efecto inicial. Un problema adicional es la posible aparición de resistencias que ocurren durante el uso prolongado de lamivudina, ya observada en los tratamientos prolongados en pacientes trasplantados18,19. Todas estas cuestiones requieren estudios controlados y cohortes más numerosas de pacientes para ser contestadas.
Hasta que dispongamos de más datos, parece razonable recomendar que: a) en todos los pacientes con enfermedades reumáticas, que potencialmente pueden recibir tratamientos inmunosupresores en general y antiTNFα en particular, se debe investigar el perfil serológico del VHB y, en el caso de no estar inmunizados, recomendar vacunación; b) si el paciente es HBsAg positivo, se debe instaurar tratamiento con lamivudina y confirmar que la replicación viral esté controlada antes de utilizar tratamiento anti-TNFα; c) si el paciente es HBsAg negativo y anticuerpo anti-HBc positivo, se debería monitorizar mensualmente el HBsAg y, si se positivizara, instaurar tratamiento con lamivudina20; d) una vez instaurado el tratamiento, se debe mantener un control estrecho de la ALT y del ADN del VHB (cada 4–8 semanas) hasta por lo menos 3 meses después de la última dosis de dicho tratamiento, y e) si ocurriera una reactivación viral, se debe pensar en la aparición de resistencias y plantear la posibilidad de utilizar otro agente antiviral, como el adenofir.