A pesar de la mejora en el manejo y el tratamiento de los pacientes con artritis reumatoide (AR), la necesidad de cirugía ortopédica correctora sigue siendo una situación que se plantea con relativa frecuencia en la práctica clínica diaria. El peso de la decisión sobre el manejo de los fármacos que recibe el paciente con AR sigue recayendo sobre el reumatólogo y esta decisión no siempre está respaldada por información científica de calidad adecuada.
Even though clinical management and treatment of rheumatoid arthritis patients has improved, orthopedic surgery is now a common situation in daily clinical practice. Usually, the rheumatologist is who manages the anti-rheumatic treatment in the perioperative period and decisions are not always supported by scientific information of suitable quality.
A pesar de que está demostrado que el tratamiento precoz e intensivo de los pacientes con artritis reumatoide (AR) mejora su evolución a medio y largo plazo1, algunos presentan un deterioro progresivo de las articulaciones que requiere algún tipo de corrección quirúrgica. En el estudio EmAR, promovido por la Sociedad Española de Reumatología y que finalizó en el año 2001, se estimó que un 26% de los pacientes con AR sufre una intervención de cirugía ortopédica durante la evolución de su enfermedad2. Esta cifra es intermedia si se compara con los datos publicados en la literatura médica sobre países del entorno: el 37% de los pacientes en Estados Unidos3,4, el 27% en Holanda, el 38% en Alemania5 y el 16% en Gran Bretaña6. Muy recientemente se ha publicado un estudio que se llevó a cabo en Suecia con cifras muy superiores a las publicadas previamente (58%)7. Las razones que argumentan los autores de estos estudios para explicar las diferencias encontradas son variadas: los cambios en los tiempos de actuación y el momento de la indicación, la disponibilidad de los cirujanos ortopédicos, las diferencias en los sistemas sanitarios, etc.
También se ha descrito una disminución en el tiempo de las tasas de procedimientos quirúrgicos ortopédicos llevados a cabo en pacientes con AR, lo que puede ser el reflejo de un cambio en la gravedad de la enfermedad o, más probablemente, en el manejo de ésta. El estudio de Weiss8 describe descensos continuos en el número de procedimientos de cirugía ortopédica en pacientes con AR en el período estudiado, de 1987 a 2001. Da Silva3 et al describen la evolución de la cirugía ortopédica en sujetos con AR de 1955 a 1995, con un menor riesgo para ésta en los pacientes diagnosticados durante los períodos de 1955 a 1964 (por una menor disponibilidad de la técnica) y de 1985 a 1994 que en los períodos de 1965 a 1974 y de 1975 a 1984. Esto puede reflejar mejoras en el tratamiento de la enfermedad, tanto desde el punto de vista diagnóstico como terapéutico, los regímenes de tratamiento nuevos y más efectivos y los avances en los patrones de actuación reumatológicos y traumatológicos. En cualquier caso, estos datos son anteriores al empleo de los agentes biológicos y aún se tardará al menos 10 años en detectar los efectos de éstos en el porcentaje de pacientes con AR a los que se les realiza cirugía ortopédica.
Pero además de la importancia por el volumen que representa, la necesidad de cirugía ortopédica, sobre todo de artroplastia de grandes articulaciones, es un indicador de gravedad de la AR9, de fallo en el manejo médico10 y de mal pronóstico. Se puede afirmar que los pacientes con AR que requieren cirugía ortopédica durante la evolución de su enfermedad tienen un peor pronóstico relacionado con una mayor discapacidad y con una peor calidad de vida (que conlleva una mayor demanda de recursos y de servicios sociales), lo que tiene consecuencias socioeconómicas importantes.
Por otro lado, los procedimientos quirúrgicos suponen un riesgo adicional para el paciente con AR. Se ha estimado que el riesgo de complicaciones infecciosas tras un procedimiento de cirugía ortopédica en general es 2,6 veces mayor en pacientes con AR que en aquellos en los que el motivo de la intervención es artrosis11.
Se ha descrito una gran variedad de factores de riesgo para la aparición de complicaciones en el contexto de cualquier procedimiento quirúrgico. Hay factores relacionados con el propio enfermo, la enfermedad que ha provocado la necesidad del procedimiento quirúrgico y la misma intervención en sí. Si se tienen en cuenta todos estos factores, los pacientes con AR reúnen varios de ellos. La enfermedad que presentan es inflamatoria. Además, muchos de ellos tienen osteoporosis y están inmunodeprimidos, tanto por la propia enfermedad como por el tratamiento que reciben. Asimismo, pueden presentar desnutrición (sobre todo en las fases de actividad de la enfermedad) y la gran mayoría de ellos recibe tratamiento con distintos fármacos para su AR así como tratamiento para otras enfermedades concomitantes.
El manejo de los fármacos que el sujeto recibe como tratamiento de su AR es un problema que se plantea con cierta frecuencia en la práctica clínica diaria y por el que otros especialistas consultan al reumatólogo, al que se considera el más preparado para la toma de decisiones sobre esta cuestión.
Manejo de los fármacos empleados habitualmente en los pacientes con artritis reumatoide durante el período perioperatorioHay una serie de consideraciones muy generales a tener en cuenta a la hora de decidir qué actitud se toma con el tratamiento habitual que recibe un paciente con AR en el momento de planear un procedimiento quirúrgico electivo12.
En primer lugar, se debe disponer de un listado exhaustivo de las medicaciones que recibe todo paciente que se vaya a intervenir; este listado debe incluir todo tipo de suplementos y de medicaciones alternativas. En segundo lugar, deben mantenerse durante todo el período perioperatorio aquellas medicaciones cuya suspensión abrupta pueda suponer un aumento de la morbilidad. En tercer lugar, deben suspenderse aquellas medicaciones que supongan un riesgo quirúrgico y no sean esenciales para la calidad de vida del paciente a corto plazo. Los fármacos que no cumplan ninguna de las condiciones anteriores deben mantenerse o suspenderse en función de la opinión del médico que sigue habitualmente al paciente.
En el caso de la AR, en un platillo de la balanza se situaría el riesgo de la suspensión del tratamiento que recibe el sujeto como tratamiento de su enfermedad, que en este caso implica la posible reaparición de la actividad inflamatoria, lo que llevaría a recomendar el mantenimiento del tratamiento. La reactivación de la AR supone una mayor dificultad en la recuperación, la rehabilitación postoperatoria y la necesidad de control de la AR, que suele requerir, a su vez, el empleo de más fármacos. En el otro platillo de la balanza se situaría el riesgo que se supone que tiene el paciente por el hecho de recibir tratamiento con medicaciones inmunorreguladoras.
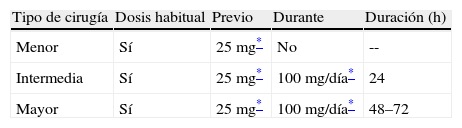
CorticoidesIndependientemente de que el tratamiento con esteroides puede empeorar el proceso de cicatrización y aumentar tanto la fragilidad de la piel y de los vasos como el riesgo de infección, la preocupación más inmediata en el manejo durante el período perioperatorio es el riesgo derivado de la supresión del eje hipotalamohipofisario debido al tratamiento esteroideo prolongado. Esta supresión puede resultar en una falta de respuesta de cortisol endógeno al estrés que supone la intervención quirúrgica. No hay riesgo de supresión del eje hipotalamohipofisario cuando el tratamiento esteroideo ha tenido una duración inferior a 3 semanas, cuando la dosis administrada es inferior a 5mg/día de prednisona (o su equivalente) o cuando se emplean dosis en días alternos. El eje hipotalamohipofisario se suprime cuando la dosis de prednisona es superior a 20mg/día y se ha empleado durante más de 3 semanas o cuando el paciente tiene un síndrome de Cushing yatrogénico. Está claro que en el primer caso no es necesario suplementar con esteroides exógenos y en el segundo caso sí. El problema se plantea en situaciones intermedias, cuando la duración del tratamiento es superior a 3 semanas y con dosis intermedias de 5mg/día a 20mg/día. En este caso lo indicado es hacer un test de respuesta suprarrenal, indicación poco práctica por lo que, en caso de no poder realizarse, lo indicado es suplementar. En cuanto a las pautas de suplementación en el período perioperatorio, hay varias descritas, una de éstas se muestra en la tabla 113. Como norma general, se debe administar una dosis única previa al procedimiento quirúrgico y posteriormente un suplemento diario total con una duración máxima que no sea superior a 72h, siempre en caso de que no surjan complicaciones postoperatorias.
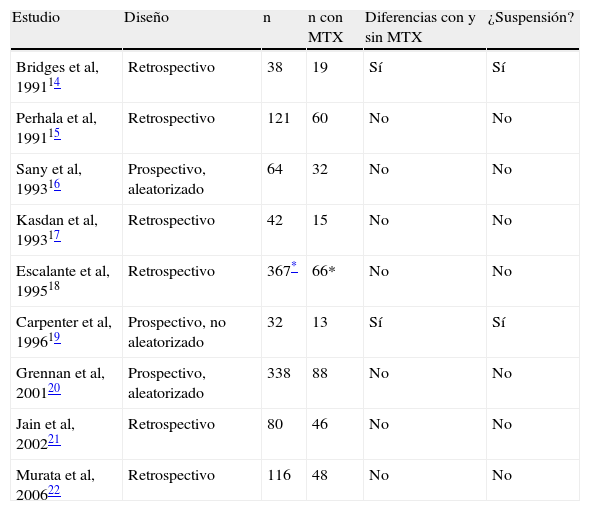
MetotrexatoDesde el año 1991 se han publicado distintos estudios en los que se analiza el empleo de metotrexato durante el período perioperatorio y sus posibles complicaciones (tabla 2)14–22. Solamente en dos de estos estudios14,19 el resultado fue desfavorable para el metotrexato; en todos los demás, el perfil de seguridad fue favorable al fármaco, sin que se encontraran diferencias en el número de complicaciones locales entre aquellos sujetos a los que se suspendía y aquellos sujetos en los que se mantenía el metotrexato. De todos estos estudios, el que marcó la diferencia fue el estudio prospectivo y aleatorizado de Grennan et al20, en el que se incluyeron 388 pacientes que se aleatorizaron prospectivamente en 3 grupos: el primer grupo continuó el tratamiento con metotrexato, el segundo grupo suspendió el tratamiento con metotrexato dos semanas antes y dos semanas después de la cirugía y el tercer grupo, que sirvió como grupo control, incluyó a pacientes en tratamiento con otros fármacos modificadores de la enfermedad distintos a metotrexato. Estos autores describen un menor número de complicaciones posquirúrgicas en el primer grupo de sujetos y, además, los sujetos de este grupo no presentan empeoramiento de la actividad de la enfermedad. Recientemente Loza et al llevaron a cabo una revisión sistemática en la que concluyen que se puede utilizar metotrexato de forma segura durante todo el período perioperatorio en pacientes con AR a los que se les va a realizar una cirugía ortopédica electiva con evidencia tipo 1b y grado de recomendación B (Véase Loza et al. Clin Exp Rheumatol: "sometido"). Sin embargo, hay dos excepciones a esta recomendación general: pacientes con insuficiencia renal y pacientes ancianos en los que está elevado el riesgo de toxicidad sobre la médula ósea, exacerbado debido a las condiciones especiales que concurren en el período perioperatorio. En este caso, la recomendación de algunos autores es la suspensión de metotrexato una semana antes de la cirugía y la reintroducción una o dos semanas tras la intervención, en función de la evolución.
Estudios sobre la influencia del metotrexato en la aparición de complicaciones en el período perioperatorio
| Estudio | Diseño | n | n con MTX | Diferencias con y sin MTX | ¿Suspensión? |
| Bridges et al, 199114 | Retrospectivo | 38 | 19 | Sí | Sí |
| Perhala et al, 199115 | Retrospectivo | 121 | 60 | No | No |
| Sany et al, 199316 | Prospectivo, aleatorizado | 64 | 32 | No | No |
| Kasdan et al, 199317 | Retrospectivo | 42 | 15 | No | No |
| Escalante et al, 199518 | Retrospectivo | 367* | 66* | No | No |
| Carpenter et al, 199619 | Prospectivo, no aleatorizado | 32 | 13 | Sí | Sí |
| Grennan et al, 200120 | Prospectivo, aleatorizado | 338 | 88 | No | No |
| Jain et al, 200221 | Retrospectivo | 80 | 46 | No | No |
| Murata et al, 200622 | Retrospectivo | 116 | 48 | No | No |
MTX: metotrexato.
Se han publicado dos estudios sobre el empleo de la leflunomida durante el período perioperatorio23,24. Ambos adolecen de importantes errores de diseño y los resultados son contradictorios. Sin embargo, el perfil de seguridad del fármaco y la perspectiva sobre éste, dados por el tiempo que se lleva utilizando, permite afirmar que no hay razones para suspender la leflunomida en el período perioperatorio.
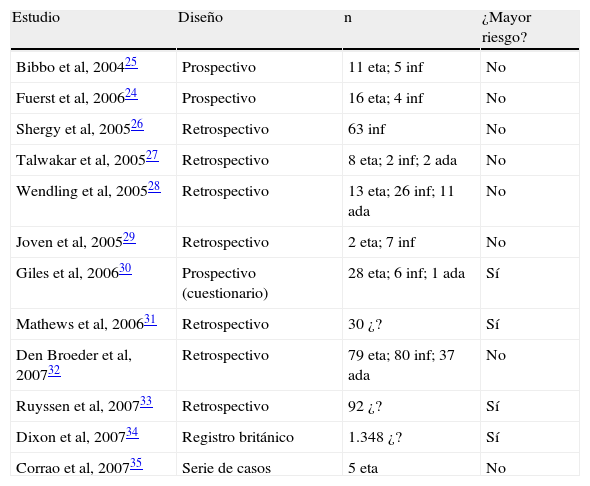
Agentes TNFUna gran cantidad de estudios han analizado el hecho de que la exposición durante el período perioperatorio a agentes (anti-TNF) puede estar asociada a complicaciones postoperatorias24–35. En total hay 12 estudios (tabla 3); ninguno de éstos tiene una validez adecuada y la mayoría incluye un número escaso de pacientes. Al analizarlos en profundidad, se aprecia una gran variabilidad en cuanto al tipo (la mayoría retrospectivos), al tipo de cirugía ortopédica incluida a las complicaciones analizadas y a los grupos de sujetos que se incluyen en el análisis. En concreto, los dos estudios prospectivos disponibles incluyen un escaso número de sujetos, tienen importantes errores de diseño y sus conclusiones son contradictorias.
Estudios sobre la influencia de los agentes anti-factor de necrosis tumoral en la aparición de complicaciones en el período perioperatorio
| Estudio | Diseño | n | ¿Mayor riesgo? |
| Bibbo et al, 200425 | Prospectivo | 11 eta; 5 inf | No |
| Fuerst et al, 200624 | Prospectivo | 16 eta; 4 inf | No |
| Shergy et al, 200526 | Retrospectivo | 63 inf | No |
| Talwakar et al, 200527 | Retrospectivo | 8 eta; 2 inf; 2 ada | No |
| Wendling et al, 200528 | Retrospectivo | 13 eta; 26 inf; 11 ada | No |
| Joven et al, 200529 | Retrospectivo | 2 eta; 7 inf | No |
| Giles et al, 200630 | Prospectivo (cuestionario) | 28 eta; 6 inf; 1 ada | Sí |
| Mathews et al, 200631 | Retrospectivo | 30 ¿? | Sí |
| Den Broeder et al, 200732 | Retrospectivo | 79 eta; 80 inf; 37 ada | No |
| Ruyssen et al, 200733 | Retrospectivo | 92 ¿? | Sí |
| Dixon et al, 200734 | Registro británico | 1.348 ¿? | Sí |
| Corrao et al, 200735 | Serie de casos | 5 eta | No |
ada: adalimumab; eta: etanercept; inf: infliximab.
Si se profundiza en la información que aporta el laboratorio que produce los distintos fármacos, en el caso del infliximab y del adalimumab aparece una alusión en la ficha técnica, pero sólo hace referencia a la larga vida media de ambos productos (término farmacológico y escasamente práctico). En el caso de los prospectos, este punto aparece referido en los tres agentes anti-TNF disponibles pero se remite al paciente al médico que prescribe el tratamiento, mayoritariamente el reumatólogo.
Hoy en día, el empleo de estos fármacos está guiado por consensos sobre su uso en distintos países. Las indicaciones sobre el manejo de estos fármacos durante el período perioperatorio en estos consensos son variadas: el consenso italiano36 no hace referencia y los consensos español y británico recomiendan la suspensión del fármaco entre dos y cuatro semanas antes y después de la cirugía37,38. Las recomendaciones más exhaustivas sobre el manejo de los agentes anti-TNF en el período perioperatorio se especifican en el consenso de la Sociedad Francesa de Reumatología39, aunque, como indican sus autores, siempre se basan en opiniones de expertos.
Otros fármacos biológicosRituximabRespecto al rituximab, no hay evidencia científica sobre el empleo del fármaco en el período perioperatorio ni sobre las consecuencias de la continuación del tratamiento durante éste en pacientes con AR. Dado que el rituximab se emplea en los trasplantes de órganos sólidos, para evitar los fenómenos mediados por células B (el rechazo o los fenómenos derivados de la incompatibilidad de grupos sanguíneos ABO40), se ha comunicado el empleo del rituximab durante los 4 meses previos a la cirugía de trasplante sin que se reporten complicaciones distintas a las habituales en estos procedimientos ni atribuibles al fármaco. Por tanto, y aunque ésta es una situación que nada tiene que ver con los pacientes con AR, parece que el rituximab es un fármaco seguro en el período perioperatorio. Ni en la ficha técnica ni en el prospecto del fármaco se hace alusión a las recomendaciones en caso de cirugía electiva.
AbataceptEn cuanto al abatacept, no hay datos publicados al respecto. Al consultar la ficha técnica y el prospecto del producto, no hacen ninguna referencia ni a un posible efecto del fármaco sobre la evolución tras la cirugía ni a las recomendaciones en caso de necesidad de intervenir a un sujeto en tratamiento con el fármaco. En los ensayos clínicos no se han hecho subanálisis de los grupos de sujetos a los que se les realiza cirugía durante el desarrollo del fármaco. En el contexto de una presentación oral el Dr. Westhovens (de Leuven, Bélgica) señaló que en su serie de 38 sujetos tratados se intervino a 10, en 8 se había suspendido una infusión y ninguno había presentado complicación durante el período perioperatorio.
ConclusionesSe puede concluir que la cirugía ortopédica supone hoy en día un problema frecuente en los pacientes con AR (uno de cada 4 de ellos tiene una intervención quirúrgica ortopédica durante la evolución de su enfermedad). En cuanto al manejo de los fármacos con los que se trata a estos sujetos, está muy clara la actitud respecto a los corticoides y al metotrexato. En cuanto al manejo de la leflunomida y de los agentes biológicos, dado que los datos disponibles en la literatura médica no son concluyentes, la decisión debe ser individualizada y, en ésta, el reumatólogo es una pieza clave.