El tejido óseo es una estructura fuertemente regulada, que desempeña un papel esencial en diferentes funciones fisiológicas. A través de acciones autocrinas y paracrinas participa en la hematopoyesis, influyendo en el destino de las células madre hematopoyéticas. Existe además una serie de moléculas compartidas y también múltiples conexiones entre el sistema inmune y el tejido óseo. Con el objetivo de agrupar los conocimientos que relacionan ambos sistemas, se ha desarrollado una nueva disciplina conocida con el término «osteoinmunología». Su progresión en los últimos años ha sido exponencial y nos ha permitido relacionar e incrementar el conocimiento en temas aparentemente alejados como la erosión reumatoide, la osteoporosis posmenopáusica, las metástasis óseas o la enfermedad periodontal. En la presente revisión hemos tratado de resumir los avances más relevantes que se han producido en la última década, sobre todo en aquellos aspectos que interesan de manera preferente a la reumatología.
Bone tissue is a highly regulated structure, which plays an essential role in various physiological functions. Through autocrine and paracrine mechanisms, bone tissue is involved in hematopoiesis, influencing the fate of hematopoietic stem cells. There are a number of molecules shared by bone cells and immune system cells indicating that there are multiple connections between the immune system and bone tissue. In order to pool all the knowledge concerning both systems, a new discipline known under the term «osteoimmunology» has been developed. Their progress in recent years has been exponential and allowed us to connect and increase our knowledge in areas not seemingly related such as rheumatoid erosion, postmenopausal osteoporosis, bone metastases or periodontal disease. In this review, we have tried to summarize the most important advances that have occurred in the last decade, especially in those areas of interest related to rheumatology.
El esqueleto humano adulto está compuesto por 213 huesos, excluyendo los sesamoideos, y constituye el 20% de la masa corporal1. Sus funciones son múltiples (tabla 1) y, hasta cierto punto, antagónicas, ya que debe poseer fortaleza y resistencia para proteger adecuadamente las estructuras vitales que alberga y, de forma simultánea, mantener la suficiente ligereza que permita el movimiento sin demasiado esfuerzo muscular2. Además, el tejido óseo es fuente de una gran actividad secretora, a través de la cual participa tanto en procesos locales como a distancia, mediante la producción de diversas proteínas con actividad hormonal que intervienen en procesos tan variados como la homeostasis del calcio, la función renal o el metabolismo energético.
Propiedades y funciones del tejido óseo
| Propiedades del tejido óseo | Funciones principales |
| Rigidez | Soporte de estructuras |
| Resistencia | Soporte de cargasPropulsión contra gravedad |
| Ligereza | Locomoción |
| Flexibilidad | Absorción de energía/recuperación |
| Capacidad de autorreparación | Formación de callo en las fracturasManejo de la fatiga y del microdaño |
| Metabolismo muy activo | Homeostasis del calcio/otros ionesReservorio factores de crecimiento y citocinasAcción endocrina (función renal, metabolismo energético)Hematopoyesis |
Considerado durante mucho tiempo como una estructura estática, el tejido óseo se comporta realmente como un órgano muy activo, que se relaciona durante todo el ciclo vital con otros órganos y sistemas, con una actividad celular permanente. Para conseguir realizar con éxito las complejas funciones citadas, el esqueleto utiliza un sistema biológico único, denominado remodelado óseo (RO), mediante el cual se renueva en su totalidad cada 10 años, a lo largo de toda la vida adulta. Este proceso, que comienza antes del nacimiento, es crucial en la adolescencia, etapa en la que la formación ósea supera a la resorción, lo que permite la adquisición del 40% de la masa ósea total y llegar al pico de masa ósea3. En los años posteriores se alcanza el equilibrio y la masa ósea permanece estable, hasta que, unos años antes de la menopausia en mujeres y a edades más avanzadas en hombres, el RO se invierte, con un resultado final de predominio de la resorción sobre la formación, lo que provoca la disminución paulatina de la masa ósea alcanzada al final de la maduración ósea. Esta aceleración del remodelado, cuando es excesiva, constituye la causa principal de la osteoporosis involutiva4.
El RO es un proceso imprescindible y fuertemente regulado, en el que intervienen factores mecánicos y un delicado cortejo de células y moléculas, que proceden de la médula ósea local y de regiones distantes del propio tejido óseo. En la última década se han sentado las bases fisiopatológicas que nos han permitido incrementar el conocimiento de los mecanismos que controlan las relaciones entre las células y moléculas protagonistas de la respuesta inmune y las células óseas, y hemos aprendido que estas complejas interacciones son fundamentales para comprender el mecanismo íntimo que caracteriza a enfermedades tan diferentes en su expresión clínica, como la artritis, la osteoporosis o el cáncer. Con la intención de agrupar todos estos conocimientos, se ha desarrollado una nueva disciplina científica, denominada «osteoinmunología», término acuñado por vez primera por Arron y Choi en el año 20005.
La osteoinmunología se encarga del estudio de las conexiones entre los sistemas inmune y esquelético (sistema osteoinmune), analizando su interdependencia a nivel anatómico, vascular, celular y molecular, con especial énfasis en el desarrollo del conocimiento de los ligandos, receptores y moléculas de señalización intracelular que gobiernan estos procesos. Su campo de interés clínico es muy amplio y alcanza un protagonismo esencial en procesos como la artritis, enfermedad inflamatoria intestinal, osteoporosis, cáncer y enfermedad periodontal, entre otras6. En la presente revisión hemos tratado de resumir los avances más relevantes que se han producido en la última década, sobre todo en aquellos aspectos que interesan de manera preferente a la reumatología.
Conexiones anatomofuncionales entre el sistema immune y el tejido óseoExisten múltiples contactos anatómicos y vasculares, así como diferentes mecanismos moleculares y celulares, que permiten la interacción permanente entre el tejido óseo y el sistema inmune, de tal forma que podemos considerarlos como un conjunto funcional integrado7 (sistema osteoinmune). El hueso, en virtud de su estructura, se relaciona interiormente con la médula ósea, participando en la hematopoyesis y permitiendo la cooperación local de células óseas e inmunes, tanto a nivel local como a distancia a través de vasos nutricios y periósticos, mientras que, a través de las entesis y el esqueleto yuxtaarticular, se conecta con estructuras decisivas en el proceso de destrucción articular que caracteriza a las enfermedades inflamatorias articulares crónicas.
Las células de ambos sistemas comparten orígenes comunes, ya que los osteoclastos (OC) proceden de células madre hematopoyéticas y comparten su linaje con los monocitos y los macrófagos, mientras que las células madre mesenquimales son las precursoras de los osteoblastos (OB), que, a su vez, desempeñan un papel central en la diferenciación de las células madre hematopoyéticas en los nichos adyacentes a la superficie endóstica8. Algunas vías moleculares que participan en el remodelado, como la parathormona (PTH), las proteínas morfogenéticas del hueso y la vía Wnt, lo hacen también en la regulación de la hematopoyesis. Por otro lado, múltiples citocinas procedentes de linfocitos, células dendríticas y macrófagos, actúan sobre las células del RO, tanto en su vertiente resortiva, generalmente a través de la vía RANK/RANKL/OPG, como en su vertiente osteoformadora, directa o indirectamente a través de la señal Wnt9.
Una de las cuestiones relevantes, aun sin resolver, es el papel del sistema inmune en el desarrollo esquelético normal. Desde un punto de vista ontogénico, el esqueleto precede al desarrollo del sistema inmune, por lo que es improbable que exista intervención relevante de este, al menos, en las fases tempranas de la formación y adquisición de las funciones del tejido óseo. Sin embargo, es sobradamente conocido que modelado y remodelado ocurren durante toda la vida adulta y que se producen en espacios concretos que comparten cierto parecido con los compartimentos cerrados donde se desarrolla la hematopoyesis, otro proceso que se mantiene activo hasta la muerte. Estos espacios medulares, denominados «nichos de células madre» (NCM), cuyo soporte estructural y mantenimiento es fuertemente dependiente de las células óseas, son imprescindibles para el desarrollo del sistema inmune y permiten la interacción de las células inmunes y óseas, de manera bidireccional.
La homeostasis ósea, en gran parte dependiente de los sitios de remodelado, está regulada por respuestas inmunes, sobre todo si estas están provocadas por situaciones patológicas. Con el envejecimiento se produce una acumulación de linfocitos T de memoria en la médula ósea, que han sido activados a lo largo de una vida de exposición antigénica continua, que expresan RANKL en su superficie y que podrían facilitar la activación del RO que se observa en ciertas situaciones asociadas a la edad avanzada.
Remodelado óseoEl RO se produce en lugares concretos llamados compartimentos de remodelado óseo, que están compuestos por una cohorte funcional de células que actúan de forma coordinada, denominada unidad multicelular básica y que contiene OC, OB, osteocitos (OS), células de la superficie ósea («linning») y células de los capilares de soporte10. El ciclo se estructura en 4 fases consecutivas, pero no simétricas ni de la misma duración, iniciándose con el reclutamiento de precursores de OC hacia un lugar de las superficies quiescentes, en la superficie trabecular o endóstica o en la profundidad de una osteona. Los OC maduros activan su maquinaria resortiva y labran una laguna (laguna de Howship), que en la siguiente fase (fase de inversión) es «allanada» por la colaboración de células de estirpe macrofágica con las células del linning, lo que permite acudir a los OB maduros que rellenan la cavidad de osteoide. Finalmente, se produce la mineralización y la formación de hueso maduro.
En ausencia de enfermedad, la diferencia entre el corto periodo de resorción y el largo periodo de formación (espacio de remodelado) no provoca consecuencias estructurales relevantes. Sin embargo, cuando existe un desequilibrio entre ambos procesos y se incrementa la frecuencia de activación de unidades de remodelado, como ocurre en la menopausia, el espacio de remodelado alcanza unas dimensiones considerables y puede provocar aumento de la fragilidad ósea (muchas lagunas abiertas, sin que haya finalizado el proceso de relleno osteoblástico).
En el esqueleto adulto normal hay unos 2 millones de sitios de remodelado que trabajan a una velocidad de 25μm por día y reemplazan un volumen óseo en cada micrositio de 0,025mm3. El intervalo entre ciclos en la misma localización oscila entre 2 y 5 años y la tasa de remodelado del esqueleto completo es del 10% anual (3% en hueso cortical y 30% en el trabecular). La vida media de los OC es de 2 semanas y su destino final, en condiciones normales, es la apoptosis, mientras que la vida media de los OB activos es de 3 meses y su destino es triple, pues pueden sufrir apoptosis o quedar inactivos como células del linning o enterrados en la profundidad de la matriz mineralizada por ellos mismos fabricada, transformándose en OS11.
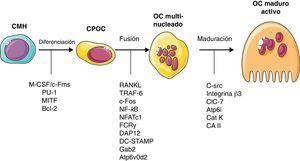
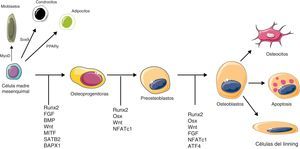
Las células óseasOsteoclastosLos OC comprenden solamente el 1-2% de las células óseas. Su morfología es característica cuando se activan y se reconocen fácilmente en las muestras sin decalcificar, como estructuras multinucleadas fuertemente polarizadas, con una región basal de intercambio de señales externas y una zona unida al tejido óseo calcificado, que posee una estructura específica denominada ribete en cepillo. Pertenecen a la estirpe monocito-macrofágica (fig. 1), aunque, a diferencia de otros miembros de la familia, en su estado maduro tienen la capacidad de unión al hueso a través de las integrinas αvβ3 que se expresan en la superficie de los podosomas y que tienen la propiedad de interactuar con proteínas de la matriz, como osteopontina y vitronectina. Tras la señal de activación primaria, se produce el anillo de actina y el sellado hermético de la zona, que va permitir el intercambio de iones y proteasas necesario para la resorción ósea.
Control molecular de la diferenciación osteoclástica. CMH: célula madre hematopoyética: CPOC: célula precursora de osteoclastos; OC: osteoclasto. Resto de abreviaturas: ver glosario de términos en el anexo 1. Modificada de Arron y Choi5.
En el citoplasma osteoclástico, la anhidrasa carbónica ii va a disociar el ácido carbónico citosólico en protones (H+) y bicarbonato (HCO3−), siendo este último intercambiado por cloro (Cl−) mediante un canal específico, lo que permite la conservación del estado isoeléctrico intracelular. El protón se dirige al ribete en cepillo, donde es captado por una bomba de protones dependiente de una ATPasa específica (H+-ATPasa) que lo transporta a la laguna osteoclástica. En la vecindad de esta bomba se sitúa un canal iónico: canal de cloro 7 o ClC7. En concreto, este canal, intercambia 2 Cl− por un H+ y está considerado como fundamental en los procesos de acidificación lisosómica en general y en la resorción ósea en particular12. Su pérdida de función es una de las causas más frecuentes de osteopetrosis13 y constituye, junto a la bomba de protones, una interesante diana terapéutica14 por el momento limitada por sus acciones extraesqueléticas derivadas, sobre todo, del riesgo de producción de enfermedades lisosómicas15.
En la laguna osteoclástica, mediante la unión de estos 2 iones, se forma ácido clorhídrico que va a acidificar el medio y provocar la disolución de la hidroxiapatita y la liberación de calcio y fosfato, manteniendo a la vez la carga iónica citoplasmática en equilibrio. Por último, a través de lisosomas, se segrega una cisteinproteasa, la catepsina K, y una serie de metaloproteasas que, finalmente, van a provocar la disolución de la matriz orgánica. Los productos de degradación resultantes entran en el OC por endocitosis y son transportados a la región basolateral en vesículas ricas en fosfatasa ácida resistente al tartrato y liberados al exterior por exocitosis.
En el momento actual se conocen una serie de moléculas de señal que participan en la diferenciación y activación osteoclásticas16, que se resumen en la figura 1. En su diferenciación, es necesaria la intervención inicial del M-CSF. En una segunda fase, la expresión de RANK en la membrana caracteriza definitivamente a la población que va a diferenciarse en OC. Cuando este receptor se une a su ligando (RANKL), la célula precursora comienza su maduración, convirtiéndose en una célula multinucleada y polarizada, capaz de activar toda su maquinaria resortiva. La activación de RANK desencadena una señal intracelular a través del factor adaptador TRAF6 y también, mediante varias cascadas de señal paralelas en las que, finalmente, se va a provocar activación de NF-κB, c-Fos, fosfolipasa C y NFATc1.
Aunque el origen clásico del RANKL se sitúa en el OB, recientes estudios han mostrado que es realmente el OS quien aporta una mayor cantidad de esta citocina, lo que, por otra parte es más lógico, debido al papel conocido de estas células en la detección de señales tanto mecánicas como hormonales, que indican que los OS podrían ser los verdaderos reguladores del RO, al menos en condiciones fisiológicas. Los linfocitos T y B también producen RANKL, aunque es muy probable que su papel sea relevante únicamente en situaciones patológicas. En condiciones fisiológicas, el IFN-γ segregado por linfocitos T inactiva TRAF6, el factor adaptador principal de la señal intracelular de RANK, lo que constituye un factor regulador de particular relevancia para impedir una sobreactivación osteoclástica provocada por el RANKL linfocitario. Este hallazgo es también importante por su dimensión histórica, pues la publicación de las evidencias experimentales de este mecanismo dio lugar a un editorial acompañante en el que Arron y Choi utilizaron por primera vez el término osteoinmunología5. Existe además una serie de vías coestimuladoras, como la que utiliza el osteoclast-associated receptor17 y el triggering receptor expressed in myeloid cells-218, cuyos ligandos y control de activación se desconocen, pero que podrían ser necesarias en estados inflamatorios, aunque su análisis excede el alcance de esta revisión.
OsteoblastosLa formación ósea es dependiente del reclutamiento de un número suficiente de OB a las superficies que han sido sometidas al ataque de los OC. Proceden de un subgrupo de células madre mesenquimales con capacidad de diferenciación osteogénica. Aunque la localización exacta de estas células in vivo no se conoce, recientes estudios sugieren que podrían situarse en la superficie externa de los sinusoides medulares y que alcanzarían las superficies óseas a través de canales vasculares en respuesta a señales procedentes de los sitios de remodelado, bien de la matriz reabsorbida o de los propios OC activos. Una vez situados en la superficie ósea, los OB producen la matriz orgánica (osteoide) y finalmente mueren por apoptosis o son «enterrados» en la matriz calcificada, transformándose en OS19.
El regulador máster de la diferenciación osteoblástica es Runx2, marcador que se expresa precozmente en este linaje celular20. Es un factor necesario, pero no suficiente, para que una célula progenitora se diferencie (fig. 2). Además es imprescindible para que se produzca tanto la osificación encondral como la intramembranosa, ya que los ratones nulicigóticos para Runx2 no forman hueso mineralizado en ninguna región del esqueleto y carecen de OB así como de fosfatasa alcalina, osteopontina y osteocalcina. En un estadio más avanzado de diferenciación intervienen otros factores, aunque los más relevantes son PTH/PTHrp, GH/IGF-1 (que desempeña un papel muy destacado en el mantenimiento de la masa muscular y ósea, y en el envejecimiento), la gran familia de las BMP21 (que pertenecen a la superfamilia del TGF-β y son los factores osteogénicos más potentes que se conocen en la actualidad) y la vía Wnt (ver más adelante). En clínica, la BMP2 y la BMP7 se utilizan, a nivel local, en fusión espinal y en defectos de unión de los huesos largos, respectivamente22
Señales moleculares que desempeñan un papel clave en la diferenciación y activación osteoblástica. MyoD: myogenic differentiation 1 protein; PPARγ: peroxisome proliferator-activated receptor gamma; Sox9: sex determining region Y-box 9. Resto de abreviaturas: ver glosario de términos en el anexo 1.
Los OS son las células óseas más abundantes (90-95%) y las más longevas, pues pueden alcanzar los 25 años de supervivencia23. Cada OS posee un elevado número (hasta 50) de prolongaciones de morfología dendrítica que se distribuyen por el tejido circundante y alcanzan la superficie, utilizando canalículos por los que circulan pequeñas moléculas, como óxido nítrico y prostaglandinas, que participan en una extensa red de señalización que empieza a ser reconocida como una parte fundamental del control del remodelado. Estas dendritas sirven de unión con otros OS cercanos y también con los OB, células endoteliales y OC superficiales, para lo que se sirven de estructuras nodales especializadas24 que contienen integrinas y conexinas (principalmente la conexina 43).
Es obvio que esta red osteocito-canalicular funciona como un sincitio situado y distribuido idealmente para detectar cambios mecánicos o lesiones en la profundidad del hueso y establecer un sistema de comunicación necesario para atraer a la zona las células precisas para adaptar la forma del hueso a la carga (modelado) o iniciar una nueva unidad de remodelado que repare el daño ocasionado, proporcione hueso nuevo al organismo o responda a necesidades hormonales sistémicas como la homeostasis del calcio o la función renal25.
La actividad secretora del OS es muy intensa, habiéndose detectado una gran cantidad de moléculas en los canalículos, entre las que destacan RANKL y OPG (señalización de inicio de activación de un sitio de remodelado en respuesta al estímulo mecánico), ATP (modulación del Ca2+ intracelular), PGE2 (promueve la osteoformación), óxido nítrico (promueve la osteoformación e inhibe la resorción), FGF23 (modula la proliferación y diferenciación celular, con acciones sistémicas de naturaleza hormonal) y la DMP-1 (que inhibe la mineralización ósea)23.
Recientemente se ha puesto de manifiesto el protagonismo del RANKL osteocítico en la activación osteoclástica. Además, la vía Wnt/β-catenina desempeña un destacado papel en la osteoformación, constituyendo una atractiva diana terapéutica. Esta ruta, también conocida como vía Wnt canónica, es fundamental para el desarrollo normal del hueso y el cartílago. También posee un papel relevante en el esqueleto del adulto, aun mal conocido, pero de importancia indiscutible en el RO26,27.
Las Wnt son una serie de ligandos naturales (actualmente se conocen al menos 19 diferentes) que se unen a receptores de la membrana celular y desencadenan acciones intracelulares que conducen a la liberación de la β-catenina y su translocación al núcleo celular. El receptor de membrana consiste en un complejo dual formado por la Lrp 5/6 y el frizzled, un receptor que contiene 7 dominios transmembrana, cuya estructura tridimensional ha sido recientemente caracterizada28. Cuando el ligando Wnt se une a esta estructura se produce una cascada de señales que conduce a la inhibición de la GSK3 β citoplasmática, la cual libera β-catenina, el mediador clave de la vía Wnt canónica, que, en ausencia de esta señal, permanece anclada en una estructura que provoca su destrucción proteosómica y evita su acumulación. Cuando la β-catenina llega al núcleo va a interaccionar con miembros de la familia de factores de transcripción TCF/Lef y a provocar la síntesis de proteínas que intervienen principalmente en la osteoformación. En esta vía, el OS interviene mediante la secreción de esclerostina, un potente inhibidor de la vía Wnt, el cual representa una atractiva diana terapéutica.
Células inmunes y fisiopatología óseaEl enorme progreso en el conocimiento de las funciones de RANKL y sus receptores, observado en la última década, ha sido el factor más decisivo para el desarrollo de la osteoinmunología. El RANKL es esencial para la diferenciación, activación, polarización y supervivencia del OC, en condiciones fisiológicas. Su papel en las enfermedades caracterizadas por una destrucción ósea acelerada, como la osteoporosis, artritis o metástasis óseas, es también muy importante, aunque se han observado algunas peculiaridades que van a tener una enorme relevancia clínica.
Cuando se estudian modelos animales de artritis, los ratones deficientes en RANKL o c-fms (ambas progenies carecen de OC, ya que no responden a los ligandos RANK o M-CSF, respectivamente), no sufren destrucción ósea, incluso cuando son cruzados con ratones transgénicos para TNF, que desarrollan artritis erosiva espontáneamente. Sin embargo, en ambos casos se observa un nivel similar de inflamación, que indica que OC y RANKL son imprescindibles para la destrucción ósea pero no para la inflamación, la cual está regulada por vías patogénicas diferentes29,30. Esta observación experimental ha sido corroborada en la clínica, ya que las terapias antiosteoclásticas reducen la pérdida ósea pero no la inflamación.
Cuando se silencia el gen Tnfsf11, que codifica la citocina RANKL, además de desarrollarse una osteopetrosis por carencia de OC, se producen alteraciones en el desarrollo de los linfocitos y en la organogénesis de los ganglios linfáticos. La deleción dirigida de otras moléculas también provoca efectos en ambos sistemas. Por ejemplo, los ratones que carecen de PU.1, un factor de transcripción que regula la función de las células B, muestran un fallo en la diferenciación de los macrófagos y una inhibición de la osteoclastogénesis31. La deficiencia de adaptadores de señal transmembrana que contengan motivos ITAM, como DAP12, o de FcR-γ, provoca fallos en la activación de OC, y cuando el defecto implica a ambas moléculas se produce una osteopetrosis grave32.
Existe, además, una serie de moléculas coestimuladoras, cuyo papel no se conoce con claridad, pero que podría ser importante sobre todo en estados patológicos de activación osteoclástica. Una de estas moléculas, denominada osteoclast-associated receptor, un receptor IgG-like cuyo ligando se desconoce, transmite una señal intracelular complementaria a la de RANK, a través de NFATc1, y también modula la activación y maduración de las células de la estirpe monocito-macrofágica. Este receptor podría ser relevante en la patogénesis y gravedad de las enfermedades osteoinmunes y la identificación de su ligando, aun desconocido, es un campo de enorme interés17. En resumen, existen múltiples evidencias experimentales que indican que el esqueleto y el sistema inmune emplean los mismos sistemas de señalización.
La infiltración de linfocitos T es una de las características principales de la sinovial reumatoide, aunque su papel en la osteoclastogénesis (y por consiguiente, en la erosión yuxtaarticular) ha sido motivo de larga controversia. Estas células, cuando son activadas, expresan RANKL, pero, dependiendo de su perfil también segregan otras citocinas como IFN-γ en el caso de los linfocitos Th133, que posee una acción antiosteoclastogénica, incluso a concentraciones muy bajas, a través de la degradación de TRAF6 mediada por el sistema ubiquitina-proteasoma34. Además, la expresión de IFN-γ en la sinovial reumatoide es baja, lo que sumado a lo anterior, convierte a la célula Th1 en un candidato muy improbable de activación de OC, en este escenario.
En este punto, queremos destacar los trabajos realizados en laboratorio de Takayanagi35, uno de los pioneros de la osteoinmunología, en los que se muestra la relevancia de la subpoblación Th17 como principal reguladora de la activación osteoclástica local en la artritis reumatoide (AR). Estas células, que cronológicamente podemos definir como el tercer brazo efector (tras el descubrimiento inicial de las Th1 y Th2) de la población de células T helper CD4+, son muy relevantes en la defensa frente a infecciones bacterianas y fúngicas, pero su desequilibrio puede promover la aparición de enfermedades autoinmunes. Su desarrollo se produce en respuesta a IL-6 y TGF-β, mientras que IL-23 promueve su expansión. La deficiencia transgénica de IL-17 en modelos murinos o el bloqueo terapéutico mediante anticuerpos reduce marcadamente el desarrollo de AR, hechos que sugieren que estas células tienen un papel patogénico muy relevante en la patogenia de esta enfermedad, que se analizará en otro apartado.
Papel del sistema inmune en la osteoporosis posmenopáusicaLas células óseas poseen receptores estrogénicos y se ha observado que estas hormonas pueden actuar directamente sobre el esqueleto, mediante funciones protectoras mal conocidas, cuya disfunción sería determinante en la patogenia de la osteoporosis posmenopáusica (PM). Además de esta acción, los estrógenos ejercen acciones indirectas regulando la producción de citocinas por las propias células óseas y también por los linfocitos T y B, que finalmente van a interaccionar, provocando cambios en el perfil de remodelado. Hace una década se observó un incremento en los niveles de TNF-α en el microambiente esquelético provocado por la expansión de células T asociada al déficit estrogénico, postulándose esta citocina como actor principal de la pérdida ósea climatérica36,37. Sin embargo, el estudio de modelos murinos deficitarios en TNF-α mostró resultados contradictorios38,39 y situó el interés en la búsqueda de otras citocinas protagonistas de la resorción acelerada que caracteriza al periodo PM.
Existen evidencias que muestran una sobrerregulación de RANKL tras la ovariectomía, tanto en células de la médula ósea PM como en células sinoviales de ratones con artritis experimental40–42. La expresión de RANKL en mujeres con menopausia reciente se triplica en células mononucleares de la médula ósea, tanto en los preosteoblastos como en los linfocitos T y B, cuando se compara con mujeres premenopáusicas o con PM tratadas con estrógenos. Por otro lado, Yoneda et al. proporcionaron pruebas adicionales del relevante efecto de los estrógenos sobre RANKL al observar un marcado incremento de esta citocina en células sinoviales en un modelo murino de AR sometido a ovariectomía43.
Los estrógenos ejercen también acciones sobre RANK de membrana en precursores osetoclásticos y en OC maduros, aunque los resultados del análisis de la expresión de este receptor, en situaciones de déficit hormonal, han sido contradictorios. Existen pruebas de que los estrógenos intervienen en la señal RANKL-RANK intracelular por mecanismos que comienzan a ser actualmente desvelados. Mediante experimentos efectuados en monocitos murinos se ha observado que estas hormonas bloquean la transcripción de la señal dependiente de AP-1 al suprimir la expresión de c-Jun y su fosforilación por cinasas. Los estrógenos inhiben también la degradación de IkB, impidiendo la localización nuclear de NF-κB en los OC, probablemente a través de efectos no genómicos que promueven secuestro de TRAF644–46.
En resumen, son numerosas las pruebas que confirman la potente acción antirresortiva de los estrógenos y que, parte de estas acciones, están relacionadas con el sistema RANKL/OPG/RANK. Sin embargo, aun no ha sido suficientemente aclarado si estas acciones son directas o se producen de forma indirecta, implicando a otras citocinas. Es un hecho aceptado que la producción de RANKL por células osteoblásticas es estimulada en presencia de TNF-α, IL-1b, IL-11 y PGE247 e inhibida por TGF-β48. Además, la administración de etanercept o anakinra a mujeres con menopausia reciente reduce en un 50% los marcadores de resorción, mientras que diferentes modelos murinos han confirmado el relevante papel de estas citocinas en la osteopenia inducida por la ovariectomía49. La función de otras citocinas, como IL-6 o IL-7 no ha sido suficientemente aclarada, aunque es probable que desempeñen también un cierto papel prorresortivo.
Mecanismos de daño óseo en la artritis reumatoideLa membrana sinovial, compuesta por una población mixta de células con características fenotípicas de fibroblastos y macrófagos, es el sitio en el que se inicia el proceso inflamatorio articular. Este fenómeno se produce tras la infiltración sinovial por linfocitos T y B, células endoteliales y macrófagos activados, y conduce a una hiperplasia sinovial marcada y a la destrucción del hueso situado en las zonas de contacto osteosinoviales, que ocasiona las típicas erosiones y la invasión de los espacios medulares adyacentes por el tejido inflamatorio neoformado50.
Asimismo, se conocen otras 2 formas de pérdida ósea en la AR: la osteopenia periarticular que afecta al hueso trabecular y cortical situados en la vecindad del proceso inflamatorio, y la osteopenia generalizada que se produce en regiones alejadas del tejido articular51. En ambos casos se observa una disminución de la masa ósea, aunque por mecanismos diferentes. En la osteopenia sistémica el remodelado se acelera aunque permanece acoplado, con un balance final negativo, mientras que en la pérdida ósea periarticular existe un déficit osteoformador primario, probablemente asociado a un disbalance en el acoplamiento mediado, entre otros, por Dkk-1. En esta revisión nos centraremos en la lesión focal que da lugar a la erosión, como característica primordial de la enfermedad.
Las células efectoras de la erosión, situadas en la zona de contacto entre el pannus sinovial y el hueso marginal, expresan catepsina K, fosfatasa ácida resistente al tartrato, integrina β3 y mRNA del receptor de calcitonina, que son marcadores fenotípicos característicos de los OC maduros. En la sinovial reumatoide se producen múltiples citocinas con actividad osteoclastogénica (tabla 2), entre ellas RANKL, M-CSF, IL-1, IL-17 y TNF, aunque los mecanismos que conducen a la erosión todavía son mal conocidos. Es un hecho demostrado que la infiltración sinovial por células T es una de las principales características de la AR y que estas células activadas expresan RANKL, lo que las convierte en candidatas para la activación osteoclástica. Sin embargo, estas células segregan otras citocinas, algunas como IFN-γ (Th1) e IL-4 (Th2), que ejercen un potente efecto inhibidor de la diferenciación osteoclástica a partir de sus precursores de la línea monocito-macrofágica52.
Citocinas y factores locales potencialmente implicados en la erosión reumatoide
| Citocina | Población celular de origen en AR | Efecto inflamatorio | Efecto osteoactivo |
| TNF-α | Macrófagos y células dendríticas | CK proinflamatoria principal en AR | Activación osteoclástica indirecta a través de RANKL. Directa probable a través de receptor de TNF 1. Inhibe osteoformación |
| TGF-β | Células Treg y dendríticas | No | Activación osteoclástica indirectaInhibe diferenciación osteoblástica |
| GM-CSF | Células Th1 | Sí. Probable papel en activación local y reclutamiento de macrófagos y PMN | Inhibe osteoclastogénesis |
| IFN-у | Células Th1Células NK | Sí | Inhibe osteoclastogénesis |
| IL-1 | Macrófagos y células dendríticas | Sí | Estimulador potente de la osteoclastogénesis y activación |
| IL-2 | Células Th1 | Sí | |
| M-CSF/IL-3 | Células Th1 y Th2 | Sí | Inhibe osteoclastogénesis |
| IL-4 | Células Th2Mastocitos | Pro y antiinflamatoria | Inhibe osteoclastogénesis |
| IL-6 | Macrófagos, células dendríticas y fibroblastos sinoviales | CK proinflamatoria principal | Activación osteoclástica indirecta |
| RANKL | Fibroblastos sinoviales, osteoblastos y células Th17 | No | Activación osteoclástica directa a través de RANK |
| IL-10 | Macrófagos, células Th2, células Treg | Acción anti-inflamatoria | Acción antiosteoclástica |
| IL-15 | Monocitos, macrófagos, células dendríticas y fibroblastos | Acción pro-inflamatoria | Activación osteoclástica indirecta |
| IL-17A | Células Th17, células Tуδ, mastocitos | Citocina efectora principal de Th17 | Activación osteoclástica indirecta a través de RANKL y mediante la inhibición de IL-4, IFN-у e IL-12 |
| IL-17F | Células Th17, monocitos | Mediador débil de inflamación a través de Th17 | Probable acción osteoclastogénica |
| IL-21 | Células Th17 y células NK | Sí a través de amplificación autocrina de Th17 | Activación osteoclástica indirecta dependiente de RANKL |
| IL-22 | Células Th17, células NK, células dendríticas | Sí a través de inducción de TNF e IL-6 | Activación osteoclástica indirecta |
| IL-23 | Células dendríticas y macrófagos | Sí a través de Th17 | Activación osteoclástica indirecta |
| IL-27 | Células dendríticas y macrófagos | Función dual, dependiente del microambiente de citocinas | Inhibe formación de precursores osteoclásticos, bloqueando señales intracelulares dependientes de RANK |
| IL-32 | Células NK, fibroblastos sinoviales | Sí. Funciones de predominio intracelular. Dependencia mutua de TNF-α | Promueve diferenciación osteoclástica pero no activación directa |
| IL-33 | Fibroblastos sinoviales | Acciones mixtas no bien definidas | Inhibición de osteoclastogénesis |
| Dkk-1 | Osteocitos y osteoblastos | Inhibidor soluble y global de la vía Wnt. No claras acciones inflamatorias en AR | Inhibidor clave de la osteoformación en AR |
| sFRP | Fibroblastos y macrófagos sinoviales | Inhibidor soluble vía Wnt sin efecto sobre inflamación en AR | Inhibidor de la osteoformación |
| Esclerostina | Osteocitos, condrocitos | Inhibidor de la vía Wnt, con acciones más selectivas que Dkk-1 | Inhibidor de la osteoformación |
AR: artritis reumatoide; CK: citocina; Dkk-1: proteína Dickkopf-1; GM-CSF: factor estimulador de colonias de granulocitos y macrófagos; IFN-у: interferón gamma; IL: interleucina; M-CSF: factor estimulador de colonias de macrófagos; NK: natural killer; PMN: polimorfonucleares; RANK/RANKL: receptor activador del factor NF-κB /ligando del RANK; sFRP: secreted frizzled-related protein; TGF-β: transforming growth factor beta; TNF: factor de necrosis tumoral; Treg: células T reguladoras; Wnt: vía de señalización Wnt, término proveniente de la unión del nombre del gen Wg (wingless) de la Drosophila y su homólogo Int (Integration 1) de los mamíferos.
Otros hallazgos experimentales han añadido pruebas negativas sobre el papel de las células T, tanto Th1 como Th2, como efectoras directas de la activación osteoclástica, y en definitiva, de la producción de erosiones. Por ejemplo, en cocultivos de células T activadas con precursores de OC se observa un efecto de predominio inhibidor de las primeras sobre las segundas, mientras que en modelos murinos de artritis inducida por colágeno, la gravedad del daño óseo local podía estar incrementada en ausencia de señal IFN-γ o IL-4. Todos estos datos sugieren que tanto las células Th1 como las Th2 no intervienen directamente en la destrucción ósea local53,54.
Las células Th17, consideradas el tercer brazo efector de la población de células T CD4+ activadas55, cumplen una serie de características que las implican directamente en la activación osteoclástica local en la AR: no producen cantidades significativas de IFN-γ, provocan simultáneamente inflamación local y citocinas que inducen expresión de RANKL en los fibroblastos sinoviales y ellas mismas expresan RANKL con capacidad de activar directamente a los precursores osteoclásticos. Su diferenciación es desencadenada por la combinación de IL-6 y TGF-β, mientras que IL-23 es requerida para su desarrollo y funciones efectoras, pero no es imprescindible para el inicio de su diferenciación desde la célula naïve.
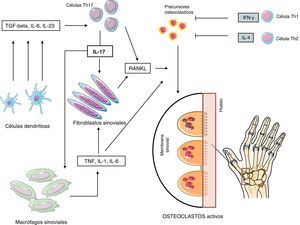
Las células Th17 maduras producen IL-17, IL-21 e IL-22, citocinas con actividad proinflamatoria y, en el momento actual, pueden considerarse el largamente buscado subtipo Th osteoclastogénico. Para ello, estas células producen IL-17 que induce expresión de RANKL en los fibroblastos sinoviales que, principalmente de forma directa, contacta con el RANK de los precursores provocando la diferenciación de OC que migran hacia la zona marginal donde inician la erosión ósea. Además, la IL-17 incrementa la inflamación local mediante la producción de citocinas inflamatorias, como TNF, IL-1 e IL-6. En definitiva, podemos concluir que las células Th17 tienen capacidad de provocar tanto inflamación como destrucción ósea local, y constituyen una interesante diana terapéutica, que actualmente, avanza en su desarrollo clínico56–61 (fig. 3).
Una de las características propias de la erosión reumatoide es la llamativa ausencia de reparación perilesional, en oposición a lo que se observa en otras enfermedades inflamatorias como la artritis psoriásica o la espondilitis anquilosante62. Tradicionalmente se ha relacionado con la actividad inflamatoria local que frenaría el trabajo osteoblástico en la proximidad de la erosión63. Sin embargo, la utilización de potentes fármacos antiinflamatorios, como los inhibidores del TNF o de la IL-6, aunque frene la evolución de la erosión, solamente provoca ligeros signos de reparación, en forma de aposición de hueso nuevo, situado en la base de la erosión, adyacente a la médula ósea yuxtaarticular64–67.
En modelos murinos se ha observado que la población de precursores osteoblásticos expresando Runx2 es elevada en las zonas inflamadas, pero muy escasa la presencia de OB maduros, con muy baja expresión de fosfatasa alcalina que indicaría mineralización activa68. Estas células inmaduras podrían producir osteoide pero no mineralizarlo, conservando, a su vez, la expresión normal de RANKL y, por consiguiente, su capacidad de activar OC.
En su conjunto, los resultados obtenidos sugieren que el proceso inflamatorio de la AR provoca un desequilibrio entre la resorción y formación óseas, con freno en la formación de OB maduros, pero no en la llegada de precursores Runx2 positivos. Estas células presentan un fenotipo que recuerda al observado en ratones con señalización de β-catenina deficiente, lo que ha disparado el interés de la vía Wnt como posible vía disfuncional implicada en la ausencia de reparación de la erosión reumatoide.
Hasta el momento, se conocen varias familias de inhibidores endógenos de la vía Wnt que, por su papel extraordinariamente relevante en múltiples funciones del desarrollo y de la activación de varios sistemas celulares, está fuertemente regulada. Entre ellos, esclerostina, Dkk-1 y sFRP, son los mejor conocidos69,70. En la AR se encuentran niveles séricos elevados de estas moléculas y el tratamiento con un anticuerpo monoclonal neutralizante de Dkk-1 mejora la erosión local en el ratón hTNF.Tg RA, invirtiendo el patrón «asténico» de la lesión típica que se convierte en una erosión proliferativa. Una hipótesis muy interesante sería considerar que estos inhibidores serían los responsables de la escasa reparación característica de la erosión reumatoide, pero el papel específico de cada uno, su procedencia y las consecuencias de su inhibición son aspectos aun mal conocidos que deberán ser analizados en profundidad por su enorme interés patogénico y terapéutico.
Funciones inmunomoduladoras de RANKLEl papel de RANKL en la activación osteoclástica ha quedado plenamente establecido en enfermedades como la osteoporosis PM o la AR. Su expresión final va a depender del perfil de citocinas existente en el microambiente circulante. En entornos con gran componente inflamatorio, como en la sinovial reumatoide, la expresión de RANKL está incrementada, con diferentes vías de estímulo. También puede ser inducido por señales dependientes de estímulos mecánicos o por déficits hormonales como en la osteoporosis por inmovilización o PM, respectivamente. De hecho, la demostración del papel protagonista de RANKL en estos procesos y su regulación por IFN-γ constituyó el punto de partida de la osteoinmunología.
El eje RANKL/RANK controla el desarrollo de las células lobuloalveolares de la mama durante la gestación, a través de Ikk-α, una proteincinasa necesaria para la renovación de células progenitoras y también relacionada con la progresión del cáncer de mama y las metástasis del cáncer de próstata71,72. El origen de RANKL en estas circunstancias no había sido aclarado, hasta que Tan et al., en un modelo murino de cáncer de mama, demostraron que su fuente principal en el estroma tumoral eran las células TREG CD4+ CD25+ FOXP3+, tradicionalmente asociadas a mal pronóstico, y que RANKL estaba implicado en la extensión local y capacidad metastásica de las células carcinomatosas que expresan RANK73. El papel paracrino de RANKL en la tumorogénesis mamaria ha sido confirmado en otros estudios con metodologías diferentes74,75.
En otras circunstancias, la relación de RANKL con las células TREG también parece evidente. Por ejemplo, en un modelo murino de diabetes76 se observó que la administración de estas células prevenía la destrucción de células beta en los islotes pancreáticos, mientras que la inhibición del eje RANKL/RANK inhibía la acumulación local de células TREG, lo que provocaba activación de células T citotóxicas y destrucción de células beta. Una acción similar fue observada en colitis, donde la inhibición de RANKL frenaba la expansión de células reguladoras, empeorando la inflamación intestinal77.
El estudio global de los fenotipos de mutantes murinos también ha sido una relevante fuente de información sobre el papel extraesquelético del eje RANKL/RANK/OPG. Los ratones RANKL KO, además de presentar osteopetrosis y ausencia de la erupción dental, muestran un cociente CD4+/CD8+ normal, pero, tanto la activación de las células T como el desarrollo de los linfocitos B están alterados. Además se observan defectos en los ganglios linfáticos periféricos y un reducido tamaño de las placas de Peyer, mientras que la arquitectura esplénica es normal. Obviamente, no hay OC y, por tanto, no se observan erosiones en este modelo de artritis inducida. Cuando se silencia el gen de RANK, los resultados son muy similares. En cuanto a los ratones OPG KO, las consecuencias no son simétricamente opuestas. Por un lado, sí presentan osteoporosis, con acusada fragilidad ósea, pero además padecen calcificación arterial e hipoacusia, no existiendo suficientes datos, por el momento, sobre las características de los efectores inmunes en este modelo78,79.
Finalmente, el RANKL expresado en las células T es necesario para la formación de las células epiteliales medulares del timo que son responsables de la selección negativa de células autorreactivas, un papel cuya relevancia en el desarrollo embrionario es indudable, aunque su importancia en la función del sistema inmune adulto es desconocida80.
En resumen, RANKL es una citocina que participa en el desarrollo del sistema inmune y de la glándula mamaria. Su papel en la extensión local y capacidad de diseminación a distancia en determinados cánceres es muy destacado y parece relacionado con la función negativa atribuida a la infiltración del estroma tumoral por las células TREG. En otros órganos y funciones, su papel es más confuso y podría desempeñar una función tejido-específica, actuando como molécula proinflamatoria o antiinflamatoria, en relación directa con las células reguladoras.
Células óseas como inmunomoduladorasUna de las funciones del esqueleto, enumeradas en la tabla 1, es el soporte de estructuras vitales, entre ellas, la médula ósea. Aunque, clásicamente, considerado como una simple estructura protectora, en el momento actual está plenamente demostrado que el tejido óseo participa de manera destacada en la fisiopatología medular, al formar parte de los NCM hematopoyéticas, donde interviene en las decisiones sobre el destino de estas, fuertemente dependiente del microambiente local.
En 1994 se demostró por primera que los OB mantenían la proliferación de progenitores hematopoyéticos primitivos in vitro, a través de G-CSF81, y, desde entonces, ha crecido significativamente el interés por conocer el papel de estas células en el determinismo de los progenitores hematopoyéticos, sobre todo en las líneas relacionadas con el sistema inmune82. Una subclase de OB, que por sus características morfológicas y de expresión génica son denominados spindle-shaped N-cadherin+ osteoblastic cells, tienen capacidad funcional para interaccionar con receptores de células madre hematopoyéticas y soportar estructuralmente su anclaje en el interior de los nichos situados en el endostio83.
Otras vías de señalización, como Notch84 y algunas moléculas segregadas por el OB, como angiopoyetina-185, han sido también implicadas tanto en la regulación del pool de CMH como en el equilibrio entre células en fase quiescente o en fase de desarrollo, aunque con resultados contradictorios. Podríamos concluir que los OB desempeñan un papel relevante en los nichos endósticos, aunque su función precisa aun no ha podido ser definida con claridad.
Los OC, con su función exclusiva de resorción, podrían ser los encargados de degradar la superficie endóstica proporcionando «sitios» estructuralmente adecuados en los que se situarían los NCM hematopoyética. De esta forma, RO y hematopoyesis estarían íntimamente conectados. No obstante, estudios más recientes no han podido demostrar la participación necesaria de los OC en el mantenimiento y movilización de las células madre, y su función sería puramente estructural86. Otras funciones como su posible papel en el mantenimiento de las células plasmáticas, tras la demostración in vitro de un aumento de la supervivencia de estas células en presencia de OC, acción que requiere contacto celular y mecanismos independientes de BAFF y APRIL87, así como sus funciones como célula presentadora de antígenos88 con capacidad de activar células T CD4+ y CD8+ indican la necesidad de ampliar estudios que determinen con exactitud el papel de los OC en la regulación del sistema inmune.
Perspectivas futurasEs evidente que la agrupación de los conocimientos que han ido surgiendo desde diferentes disciplinas científicas y que relacionan el sistema inmune con el esqueleto, ha sido muy beneficiosa para el desarrollo de nuevas dianas terapéuticas. Por ejemplo, la enorme capacidad secretora del OS indica que sus funciones transcienden el esqueleto y van mucho más allá de su papel en el RO. Es intrigante observar las consecuencias de la anulación del gen de la esclerostina, teniendo en cuenta que es una diana terapéutica en muy avanzado estado de investigación clínica. En un reciente estudio realizado en el modelo murino SOST (-/-), Cain et al. observaron que el desarrollo de la estirpe linfocitaria B estaba afectado en todas sus fases, a causa del aumento de la apoptosis de estas células89. El análisis de la expresión de este gen (cuyo producto es la esclerostina) confirmó su origen osteocitario y su ausencia en la línea hematopoyética. Además, la alteración descrita era independiente de Wnt. Podríamos decir que el OS, a través de la esclerostina, desempeña un papel en la maduración de la estirpe linfocitaria B, antes desconocido, cuyo estudio es de vital interés.
Otro aspecto relevante que extiende aun más si cabe el perímetro de la osteoinmunología ha sido puesto de manifiesto recientemente por Buchwald et al.90. Este grupo había demostrado previamente que los OC murinos pueden reclutar células CD8 naïves bajo condiciones no inflamatorias y activarlas para inducir linfocitos T CD8 FoxP3+ (TcREG) y también producir citocinas como IL-2, IL-6, IL-10 o IFN-γ91, cuyas acciones individuales sobre la osteoclastogénesis pueden ser positivas o negativas. En un estudio in vitro determinaron que el efecto neto de estas células es supresor y directo, inhibiendo la diferenciación de OC maduros, que pierden su capacidad resortiva, sin afectar a su supervivencia. Mientras que la inducción de linfocitos TcREG por OC es antígeno-dependiente, la supresión de OC por TcREG no requiere antígeno o reestimulación. El bloqueo de las citocinas citadas reducía parcialmente su efecto inhibidor. La confirmación de estos hallazgos indicaría que existe un feed-back regulador osteoinmunológico en la activación osteoclástica y que este subtipo de células T reguladoras participaría no solo en el sistema inmune y en la patogenia de la artritis, sino también en la homeostasis esquelética. Estos resultados muestran que existe un complejo equilibrio entre las acciones directas de los linfocitos TcREG y las indirectas a través de citocinas con funciones antagónicas a nivel individual92.
La comunicación intercelular es otro de los aspectos que están situándose como diana terapéutica de primer nivel93. Al papel ya conocido de la familia de efrinas, ligandos unidos a membrana y sus receptores Ephs en la transmisión de señales entre OC y OB se añade un nuevo grupo de moléculas de enorme interés. Se trata de las semaforinas, identificadas inicialmente como un sistema de guía axónica necesario para que las neuronas alcancen sus dianas y, posteriormente, implicadas en numerosas funciones orgánicas, entre ellas el sistema inmune y el esqueleto94. Hasta el momento, no se ha hallado ninguna molécula con acción «protectora» del esqueleto que actúe a nivel local sobre OC y OB, lo que impide romper el acoplamiento entre resorción y formación y condena de forma repetitiva a los diferentes fármacos a un techo terapéutico debido al freno en la actividad osteoblástica que sigue al uso de antirresortivos y, en el otro extremo de la balanza, al estímulo osteoclástico que sigue al tratamiento anabólico. La semaforina 3 A (Sema 3 A) se une a la neuropilina 1 (NRP-1) bloqueando la diferenciación osteoclástica inducida por RANKL al inhibir las vías de señal proximal ITAM y RhoA, mientras que simultáneamente estimula al OB a través de la vía Wnt canónica. Los ratones Sema 3A -/- tienen fenotipo osteopénico que puede ser reproducido alterando la señal Sema 3A/NRP-1, mientras que la infusión intravenosa de esta semaforina incrementa el volumen óseo y acelera la osteoregeneración95.
ConclusionesLa osteoinmunología es una nueva disciplina científica, de evolución vertiginosa, que estudia los efectos mutuos del esqueleto y el sistema immune a nivel celular y molecular, tanto en condiciones fisiológicas como en las enfermedades óseas. La osteoinmunología ha puesto de manifiesto que existe un amplio repertorio de moléculas e interacciones celulares, cuyo conocimiento detallado está proporcionando sólidas bases científicas para un cambio de paradigma en el campo de las enfermedades osteoinmunes, lo que permitirá el desarrollo de aproximaciones terapéuticas más eficaces y seguras en los próximos años.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses en relación con el presente trabajo.
Responsabilidades éticasProtección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
GLOSARIO DE TÉRMINOS
Apc (adenomatous polyposis coli): Proteína intracelular que, junto a axina y GSK3 β, forma parte del complejo que retiene a la β-catenina y promueve su degradación. Cuando se activa la via Wnt canónica, es atraída a la membrana celular con el resto de la estructura de retención, quedando libre la β-catenina.
Atp6v0d2 y Atp6i: Isoformas de la ATPasa vacuolar que desempeñan papeles destacados en el funcionamiento de la bomba de protones que permite la acidificación de la laguna osteoclástica. Su disfunción puede provocar formas graves de osteopetrosis.
ATF4 (activating transcription factor 4): Factor de transcripción que desempeña un papel relevante en las células del linaje osteoblástico más maduras.
BAFF (B cell activating factor belonging to the TNF family): Citocina implicada en la maduración y supervivencia de los linfocitos B periféricos y en la activación de los linfocitos B y T.
BAPX1 (bagpipe homeobox protein homologue 1): Factor de transcripción que estimula la osteoblastogénesis en esqueleto axial.
Bcl-2 (B-cell CLL/lymphoma 2): Molécula antiapoptótica por su acción inhibidora de la liberación de citocromo C mitocondrial, que promueve la diferenciación, activación y supervivencia de osteoclastos y osteoblastos.
β-Catenina: Proteína citoplasmática multifuncional que media en la señal Wnt.
BMP (bone morphogenic protein): Son un grupo de citocinas, originalmente descubiertas por su papel como potentes inductoras de la formación ósea. Actualmente su papel es muy amplio, estando relacionadas con señales morfogenéticas fundamentales en muchos tejidos.
c-Fos: Factor de transcripción implicado en la diferenciación osteoblástica. Dimeriza con la proteína c-Jun para formar el factor de transcripción AP-1, el cual activa la transcripción de numerosos y diversos genes implicados en procesos relacionados con la proliferación y diferenciación celular.
Caderinas: Familia de glucoproteínas transmembrana que median en la adhesión intercelular y también actúan como receptores de señal que afectan a la diferenciación y proliferación celular.
Catepsina K: Cisteína-proteasa que segrega el osteoclasto al ribete en cepillo y provoca la primera fase de la disolución del colágeno de la matriz ósea.
CK1 (casein kinase 1): Familia de cinasas que funcionan como reguladores de la transducción de la señal en múltiples vías, entre ellas la Wnt-β-catenina.
ClC7 (canal de cloro 7): Uno de los miembros más relevantes de la superfamilia de los canales de cloro, que participa en el intercambio de cloro por protones, un proceso fundamental para la resorción osteoclástica.
CREB (cAMP response element-binding): Factor de transcripción implicado en la activación osteoclástica.
DAP12 (DNAX-activating protein de 12 kDa): Proteína adaptadora que contiene ITAM (immunoreceptor tyrosine-based activation motifs) y que desempeña un papel esencial en la transducción de la señal RANK.
DC-STAMP (dendritic cell specific transmembrane protein): Proteina transmembrana fundamental para la fusión osteoclástica.
Dmp1 (Dentin matrix acidic phosphoprotein 1): Proteína de la matriz extracelular que desempeña un papel muy relevante en la mineralización del hueso y de la dentina.
Dsh (disheveled): Es una fosfoproteína citoplasmática que desempeña un papel relevante en la señal intracelular de los receptores frizzled.
Dkk (Dickkopf): Familia de proteínas compuesta por 4 miembros, que contienen entre 206 y 366 aa. Los denominados Dkk-1 y 4 inhiben las vías de señal Wnt, uniéndose al LRP 6 a través de su dominio CRD1, con lo que son antagonistas naturales de la vía Wnt canónica.
FcR-γ (receptores gamma para el Fc): Receptores que reconocen la porción Fc de la IgG y son importantes en la respuesta de los leucocitos a los inmunocomplejos, participando además en el desarrollo del linaje osteoclástico.
FGF (fibroblast growth factor): Familia de citocinas que desempeñan un papel clave en diversos procesos relacionados con la proliferación y diferenciación celular. Se han identificado 22 miembros en humanos y su acción se realiza a través de receptores con dominios extracelulares Ig-like y trasmisión de la señal intracelular a través de tirosina-cinasas.
Frizzled: Receptor de la superfamilia de receptores acoplados a proteínas G, de 7 dominios transmembrana, que transmite la señal intracelular de los ligandos Wnt. Se conocen 10 miembros, enumerados correlativamente del 1 al 10, con un tamaño variable que oscila entre los 500 y 700 aa. El dominio rico en cisteína de la región aminoterminal extracelular está altamente conservado entre especies y es imprescindible para la unión a Wnt.
Gab-2 (GRB2-associated binding protein 2): Proteína adaptadora que participa en la trasmisión intracelular de diversas señales en respuesta a estímulos procedentes de receptores de citocinas y factores de crecimiento.
GH/IGF-1(growth hormona/insulin-like growth factor 1): Eje endocrino que desempeña un papel relevante en la osteoformación. Existe una forma circulante de IGF-1, segregada por el hígado en respuesta a GH y una forma local que actúa en múltiples procesos celulares como factor autrocrino o paracrino.
GSK3 β (glycogen synthase kinase 3 beta): ver Apc.
H+-ATPasa: ATPasa del osteoclasto que provoca el paso de protones a través de la membrana para acidificar la laguna y disolver el material calcificado.
IFN-γ (interferón gamma): citocina producida principalmente por los linfocitos T y células NK, cuya función más importante es la activación de los macrófagos, tanto en las respuestas inmunitarias innatas como en las adquiridas. En el osteoclasto inactiva TRAF6, impidiendo la transducción de la señal RANK y, de esta forma, tiene acción antiosteoclástica.
Integrinas; Moléculas expresadas en la membrana del osteoclasto y que facilitan su adhesión al tejido mineralizado, mediante su interacción con proteínas de la matriz ósea. La integrina a2ß 1 se une al colágeno, mientras que la integrina avß3 lo hace con la vitronectina, osteopontina y sialoproteína ósea
ITAM (intracellular tyrosine-based activation motif): Motivos presentes en diferentes adaptadores, entre ellos TRAF6, de importancia en la transducción de la señal RANK.
Jnk (c-Jun N-terminal kinase): Pertenece a la família de cinasas activadas por mitógeno y desempeñan un papel relevante en la señalización de estímulos de estrés, entre ellos la respuesta inflamatoria.
Krm (kremen) Proteínas transmembrana implicadas en la señal Wnt/Dkk.
Lef1 (Lymphoid enhancer binding factor): Factor de transcripción implicado en la señal Wnt.
Lrp 5/6 (low-density lipoprotein receptor-related protein 5/6): Proteínas transmembrana, pertenecientes a la familia de LDLR, de 1.615 y 1.613 aa respectivamente. A diferencia de otros miembros de la familia, Lrp 5 y 6 actúan como correceptores de frizzled en la transmisión de la señal Wnt.
M-CSF (macrophage-colony stimulating factor): implicado en los estadios iniciales de la diferenciación osteoclástica.
MITF (microphthalmia-associated transcription factor): Factor de transcripción que participa, entre otros procesos celulares, en los estadios tempranos de la diferenciación osteoclástica.
NFATc1 (nuclear factor of activated T cells, cytoplasmatic): Factor de transcripción que actúa como regulador máster de la diferenciación y activación osteoclástica.
NIK (NF-κB inducing kinase): Cinasa que participa en la activación del NF-κB.
OPG (osteoprotegerin): También conocida como miembro 11B de la superfamilia del receptor de TNF, es una citocina que actúa como receptor señuelo para RANKL. Tras su unión a este, inhibe NF-κB y la activación de genes relacionados con la respuesta inmune y la activación del osteoclasto.
OSCAR (osteoclast-associated receptor): Receptor IgG-like, sin ligando conocido hasta el momento, expresado principalmente en osteoclastos, monocitos, granulocitos, macrófagos y células dendríticas. Participa en señales activadoras de osteoclastos de manera complementaria a RANKL/RANK.
Osx (osterix): Factor de transcripción principal que estimula la diferenciación osteoblástica, actuando en un nivel distal a Runx2.
PCP (planar cell polarity): Vía alternativa de transducción de la señal Wnt.
PU.1: Factor de transcripción que regula la función de las células B.
RANK (receptor cctivador del factor nuclear κB): Receptor de membrana de tipo i expresado en la superficie de los osteoclastos. Su ligando es RANKL.
Receptores señuelo: Son receptores que reconocen citocinas con elevada afinidad y especificidad, pero son estructuralmente incapaces de inducir señalización o de presentar el agonista a los complejos receptores de señal. La OPG (osteoprotegerina) es un receptor señuelo que regula el remodelado atrapando el RANKL y ejerciendo, por tanto, un papel «osteoprotector».
ROR 1 y 2 (tyrosine kinase orphan receptor): Pertenecen a la familia de receptores tirosina-cinasa (Trk).
Runx2 (runt-related transcription factor 2): Es el regulador máster y, también, el que aparece más precozmente en el proceso de diferenciación osteoblástica. Es necesario pero no suficiente para que una célula progenitora se diferencie.
SATB2 (special AT-rich sequence-binding 2): Proteína de la matriz nuclear que estimula la osteoblastogénesis a través de Runx2.
Scl (esclerostina): Hormona segregada por los osteocitos maduros que desempeña un papel de relevancia creciente en el remodelado óseo, tanto por su papel antagonistas de la vía Wnt como su más reciente función autocrina y paracrina sobre RANKL.
sFRP (secreted frizzled-related protein): Familia compuesta por 5 miembros de 286 a 325 aa, que son antagonistas de la vía Wnt, al unirse directamente al ligando, bloqueando su interacción con frizzled.
SQSTM1/p62 (sequestosome 1): Modulador de señal implicado en la transducción de señales mediadas por receptor. En el osteoclasto participa en la degradación autofágica del inhibidor de NF-κB, que permite la activación de esta célula.
SOST (gen de la esclerostina): Es el gen que codifica la esclerostina.
TCF/Lef (cell-specific transcription factor/lymphoid enhancer binding factor): Familia de factores de transcripción implicados en la señal Wnt.
TGF-β (transforming growth factor 1): Proteína multifuncional que desempeña un papel relevante en los procesos de proliferación y diferenciación de diversos tipos celulares.
TRAP (tartrate-resistant acid phosphatase): Marcador enzimático de los osteoclastos maduros.
TRAF6 (TNF receptor associated factor 6): Proteína adaptadora que tiene una función crítica en la transducción de la señal intracelular de los miembros de las superfamilias IL-1R/TLR y TNFR.
TREM2 (triggering receptor expressed in myeloid cells-2): Receptor sin ligando conocido, de estructura IgG-like, que participa, como también lo hace OSCAR, en la coestimulación osteoclástica
Unidad multicelular básica (UMB): Conjunto de células que participan de forma coordinada en el remodelado.
Wif (Wnt inhibitory factor): Antagonista natural de los ligandos Wnt.
Wise (Wnt modulator in surface ectoderm): Modulador de la señal Wnt.
Wnt: Familia de glucoproteínas segregadas y modificadas a nivel postranslacional mediante la adición de lípidos (palmitato). Actúan como ligandos naturales, desencadenando múltiples cascadas de señal que intervienen en procesos clave del desarrollo embrionario y la regeneración tisular. Son muy inestables y difíciles de aislar. Hasta el momento, se han descrito, en mamíferos, 19 proteínas Wnt distintas que actúan en 4 vías de señal diferentes. La vía Wnt-β-catenina es la más conocida y desempeña un papel clave en el desarrollo y función osteoblástica.