Se presenta el caso de un paciente con granulomatosis de Wegener asociada a anticuerpos antiproteinasa 3 que tuvo mejoría inicial con dosis altas de glucocorticoides y ciclofosfamida, pero que posteriormente a una recaída no respondió a los mismos medicamentos, ni a metotrexate ni azatioprina. Por tal motivo, recibió tratamiento con rituximab en 4 dosis, además de glucocorticoides obteniendo mejoría del cuadro tanto clínica como radiográficamente.
Male with diagnosis of Wegener's granulomatosis associated to anti-proteinase 3 antibodies that improved initially to the treatment with high dose glucocorticoids and ciclophosphamide, but in a relapse he did not have good response to glucocorticoid treatment, ciclophosphamide, methotrexate nor azathioprine. The patient received treatment with rituximab in 4 doses with clinical and radiographic improvement.
La granulomatosis de Wegener (GW) es una vasculitis sistémica granulomatosa que afecta principalmente al aparato respiratorio superior, al inferior y a los riñones. Tiene dos formas clínicas de presentación: generalizada y localizada1. El uso de la ciclofosfamida ha revolucionado el tratamiento de las vasculitis tipo GW y se considera el fármaco de elección para el control de esta enfermedad, sin embargo, la toxicidad de la ciclofosfamida limita su uso durante períodos prolongados2. La aparición de nuevos fármacos, incluida la terapia biológica, se ha convertido en una esperanza para los pacientes que no responden a la terapia convencional o que han desarrollado complicaciones por el tratamiento3.
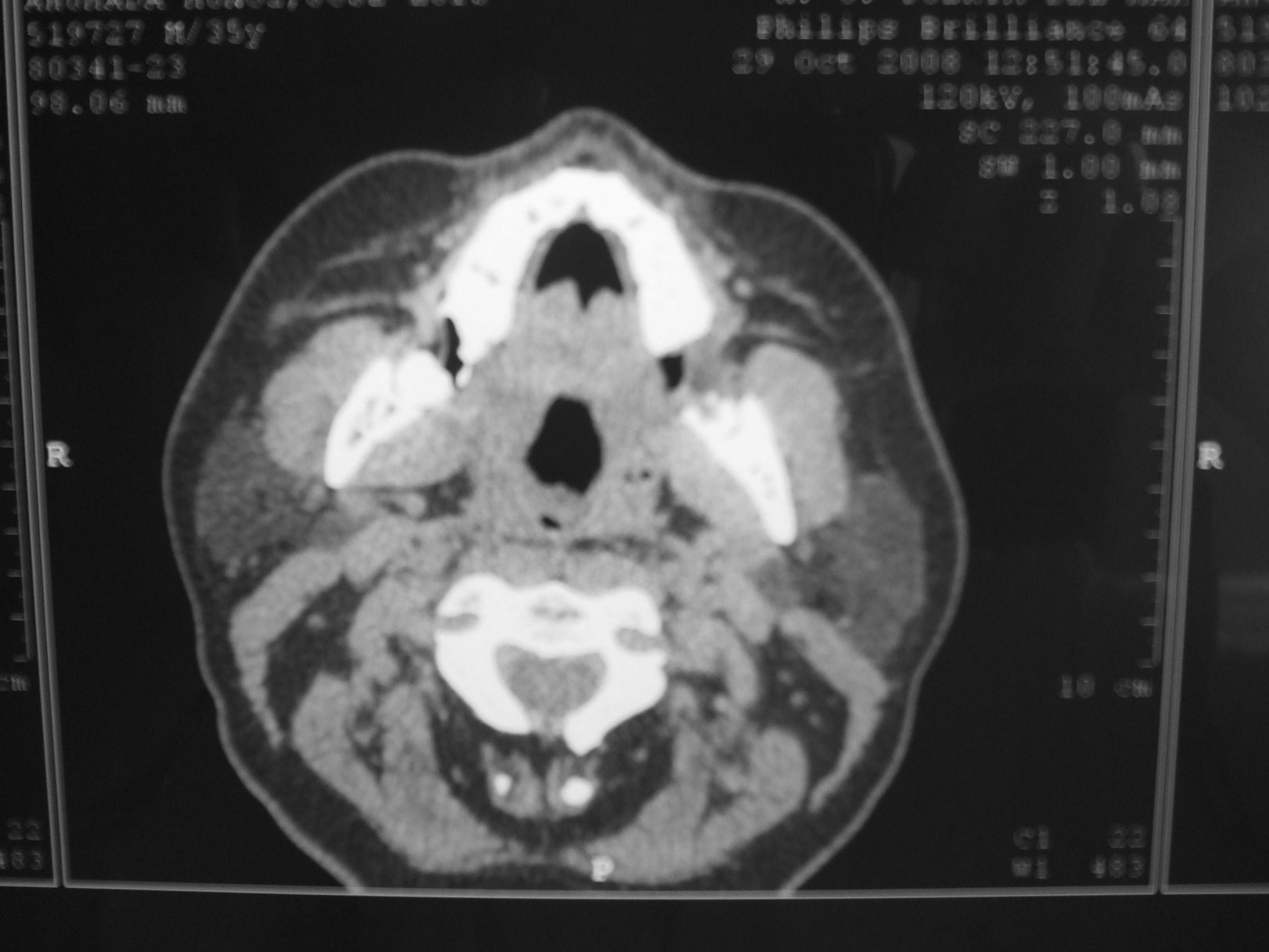
Caso clínicoVarón de 35 años con antecedentes personales de intolerancia a cotrimoxazol; hipertensión arterial en tratamiento con enalapril; sinusopatía crónica y pólipos nasosinusales intervenidos en varias ocasiones; hiperreactividad bronquial y GW diagnosticada en 1999 sobre la base de inflamación nasal; biopsia de mucosa nasal compatible con vasculitis necrosante granulomatosa; anemia hemolítica autoinmune; mononeuritis múltiple; proptosis del globo ocular derecho; seudotumor orbitario izquierdo, y anticuerpos contra el citoplasma de los neutrófilos (c-ANCA) positivos a título 1/640 con presencia de anticuerpos antiproteinasa 3 (72U/ml). Recibió tratamiento con ciclofosfamida oral (2mg/kg/día; aproximadamente 36 g de dosis acumulada de ciclofosfamida) y glucocorticoides orales (1mg/kg/día, en pauta descendente hasta alcanzar una dosis acumulada aproximada de 8,5 g) durante 1 año, logrando la remisión completa de las manifestaciones iniciales. En el año 2001 sufrió recidiva nasosinusal y seudotumor orbitario izquierdo, con índice Birmingham Vasculitis Activity Score de 28 sobre 63, y se inició tratamiento con glucocorticoides orales a dosis de 1mg/kg/día en pauta descendente (con dosis total acumulada de aproximadamente 5 g de prednisona) y metotrexate intramuscular a dosis de 20mg semanales. No se optó por reiniciar la ciclofosfamida oral por evitar secundarismos. El metotrexate hubo de ser retirado al año por hipertransaminasemia mantenida, por lo que, para mantener la remisión, se inició azatriopina (150mg/día), que se mantuvo durante 18 meses. En enero de 2008, encontrándose el paciente sin tratamiento inmunosupresor ni corticoideo y sin hacer revisiones periódicas al menos durante 2 años por problemas laborales de traslado a otra ciudad, se volvió a revisar al paciente, que refería clínica nasosinusal mantenida de al menos 6 meses de evolución. Se realizó una tomografía computarizada (TC) de senos y macizo facial, donde se objetivó ocupación en prácticamente la totalidad de las celdillas etmoidales, los senos esfenoidales, los frontales, los maxilares y las fosas nasales, con ausencia de visualización de los cornetes medios y destrucción de prácticamente la totalidad del septo nasal y de las paredes medias de los senos maxilares, con adelgazamiento marcado de las paredes inferiores de los senos maxilares y de las trabéculas óseas de las celdillas etmoidales (fig. 1), que no se conocía por estudios de imagen realizados con anterioridad al paciente. En esta ocasión se decidió el inicio de tratamiento con ciclofosfamida oral (2mg/kg/día, con dosis total acumulada de 18 g) y glucocorticoides (1mg/kg/día en dosis descendente, con dosis total de 5 g). A los 4 meses se valoró la respuesta al tratamiento y el paciente continuaba igual clínicamente. Se repitió la TC de senos y macizo facial, sin objetivar mejoría radiológica. Los estudios de laboratorio no mostraban datos clínicamente significativos. Los anticuerpos antinucleares fueron negativos y los ANCA (2.a determinación) positivos patrón C-ANCA a título 1/160 con positividad para proteinasa 3 (24U/ml). El Mantoux fue negativo y la radiografía de tórax, la ecografía abdominal y la exploración oftalmológica fueron normales. Se planteó con el Servicio de Otorrinolaringología el inicio de tratamiento biológico con rituximab intravenoso como uso compasivo a dosis de 375mg/m2 de superficie corporal/semana (cuatro dosis en total) con premedicación con glucocorticoides intravenososos (100mg de metilprednisolona), paracetamol y antihistamínicos. Se obtuvo mejoría clínica tanto sintomatológica como radiológica, tal como se objetivó en una TC de macizo facial realizada a los 3 meses de terminar el tratamiento con rituximab, donde se observó menor ocupación de las celdillas etmoidales y de los senos.
Ocupación de prácticamente la totalidad de las celdillas etmoidales, el seno esfenoidal y los frontales, los maxilares y las fosas nasales, con ausencia de visualización de los cornetes medios y destrucción de prácticamente la totalidad del septo nasal y de las paredes medias de los senos maxilares, con adelgazamiento marcado de las paredes inferiores de los senos maxilares y de las trabéculas óseas de las celdillas etmoidales.
La GW es una vasculitis necrosante sistémica que afecta a los tractos respiratorios superior e inferior y, en la mayoría de los casos, a los riñones. La enfermedad nasal se da hasta en un 80% de los casos e incluye inflamación de la mucosa con obstrucción nasal, ulceraciones y perforaciones del septo nasal, epistaxis y deformidad de la nariz “en silla de montar”4. El tratamiento se basa en los glucocorticoides a dosis altas y la asociación a inmunosupresores. El uso de la ciclofosfamida ha revolucionado el tratamiento de las vasculitis tipo GW y se considera el fármaco de elección para el control de esta enfermedad, sin embargo, se limita su uso durante períodos prolongados. La aparición de otros fármacos (como micofenolato-mofetilo, metotrexate, azatioprina, ciclosporina o inmunoglobulinas), radioterapia local y los tratamientos biológicos se ha convertido en una esperanza para los pacientes que no responden a la terapia convencional o que han desarrollado complicaciones por el tratamiento. La eliminación de células B con rituximab (4 dosis semanales de 375mg/m2 u, ocasionalmente, 2 dosis de 1g cada 2 semanas) ha inducido remisiones completas aunque temporales en pacientes con vasculitis asociadas a ANCA refractarias a terapias convencionales en pequeños estudios5,6 y mejora la enfermedad en pacientes con estenosis subglótica, granulomas retrobulbares y afectación de senos que no han respondido a la terapia convencional7,8. Sin embargo, hay casos en los que predominan las manifestaciones granulomatosas que parecen no responder a rituximab9. Su administración repetida se ha sugerido y probado con éxito aunque puede haber complicaciones y secundarismos, por lo que son necesarios más estudios y se están realizando ensayos controlados para aclarar los efectos y las nuevas indicaciones del rituximab10,11.