Evaluar si la seguridad y la eficacia de los tratamientos anti TNF en pacientes ancianos con enfermedades reumáticas inflamatorias es similar a la seguridad y eficacia en pacientes jóvenes.
MétodosRevisión sistemática. Se realizó una búsqueda bibliográfica en Medline (vía Pubmed), Embase (vía Ovid) y Cochrane Library Plus, abstracts publicados en los congresos americano y europeo de reumatología y artículos publicados en Reumatología Clínica.
ResultadosDiez estudios cumplían los criterios de inclusión. Los estudios coinciden en una eficacia similar en jóvenes y ancianos. Las diferencias en la reducción del DAS28 de antes y después entre jóvenes y ancianos son muy pequeñas: 0,04 en el estudio de Geneway et al y 0,0 en el de Mariette et al; así como en el HAQ de antes y después: 0,04 (Geneway et al), 0,18 (Schiff et al) y 0,06 (Mariette et al).
Los efectos adversos descritos en ancianos y jóvenes respectivamente son de 83,3% y 77,1% con etanercept, según Fleischmann; 27,2% vs 12,5%, p=0,19, según Chevillotte; y 57,8% vs 29,2% con infliximab, p=0,03, 36% vs 15% p=0,01 con adalimumab y de 10,3% vs 9,5% con etanercept, p no significativa, según Massara.
ConclusionesLa información para evaluar la eficacia y seguridad de los anti TNF en ancianos procede de subanálisis y por tanto se encuentra sujeta a sesgos. Podemos decir, con un nivel de evidencia bajo o moderado, que los ancianos presentan más acontecimientos adversos y similar eficacia que en los no ancianos cuando se tratan con agentes anti TNF.
To evaluate whether the safety and efficacy of anti-TNF treatments in elderly patients with rheumatic diseases is similar than the safety and efficacy of the same drugs in younger patients.
MethodsSystematic review. We performed a systematic search in MEDLINE (Pubmed), EMBASE (Ovid), and the Cochrane Library Plus. Abstracts published in the American and European rheumatology congresses and articles in Reumatología Clínica were also reviewed.
ResultsTen studies fulfilled the inclusion criteria. Studies show a similar efficacy in elderly and younger patients. The differences between the young and the elderly regarding DAS28 reductions before and after are very small: 0.04 in the Geneway et al study and 0.0 in the Mariette et al study, as well as in the before and after HAQ: 0.04 (Geneway et al), 0.18 (Schiff et al) and 0.06 (Mariette et al).Adverse events reported in elderly and younger patients are 83.3% and 77.1% respectively with etanercept, as reported by Fleischmann; 27.2% vs 12.5%, p=0.19, as reported by Chevillotte, and the rate of withdrawal due to an adverse event was 57,8% vs 29,2% with infliximab, p=0.03, 36% vs 15% p=0.06 with adalimumab and 10,3% and 9,5%, with no significant p value, as reported by Massara.
ConclusionsThe information to assess the efficacy and safety of anti-TNF therapy in elderly patients was obtained in all cases from sub analyses and therefore bias is possible. We can say, with a low to moderate level of evidence, that elderly patients undergoing anti-TNF treatments have a higher number of adverse events, and similar efficacy, when compared with younger patients.
A lo largo de los últimos años, y en gran parte gracias a la introducción de las terapias biológicas, ha mejorado el pronóstico de los pacientes con enfermedades articulares inflamatorias. Cada vez se es más consciente de que muchos de los pacientes afectos de alguna artropatía inflamatoria presentarán a lo largo del curso de su enfermedad un deterioro radiológico, funcional y social, por lo que se instaura el tratamiento con modificadores de la enfermedad (DMARD) lo antes posible, con el fin de reducir este daño. Aproximadamente una tercera parte de los pacientes no responden al tratamiento con los DMARD convencionales, por lo que reciben algún tipo de terapia biológica. Estos tratamientos presentan efectos secundarios ante los que se debe estar alerta.
La artritis reumatoide (AR) es una enfermedad inflamatoria crónica que afecta al 0,5–1% de la población1. A pesar de que la mayor incidencia de la artritis reumatoide se da entre los 30–50 años, aproximadamente de un 20–30% de pacientes con AR se diagnostican después de los 60 años, y dado que es una enfermedad crónica, los estudios epidemiológicos muestran que la prevalencia de la AR es mayor en la población de más de 65 años, siendo la edad media de las muestras poblacionales de AR 60–65 años2. Algo parecido pasa en el caso de la artritis psoriásica (APs) y la espondilitis anquilosante (EA). La APs y la EA son enfermedades que suelen debutar antes de los 40 años, siendo poco habitual a partir de los 65 años, pero al tratarse de enfermedades crónicas, que raramente remiten durante un largo periodo de tiempo, perduran durante toda la vida del individuo.
A pesar de ser probablemente el grupo más numeroso, los pacientes ancianos se excluyen con frecuencia de los ensayos clínicos, por lo que se tienen pocos datos de la eficacia y seguridad de estos tratamientos en gente de edad avanzada.
En la población anciana, debido a cambios en el metabolismo, la probabilidad de efectos adversos puede verse incrementada. Además, los pacientes ancianos presentan mayor número de comorbilidades, que requieren tratamiento concomitante, lo que conlleva mayor probabilidad de interacción medicamentosa.
Puesto que un tanto por ciento nada despreciable de los pacientes con AR que acuden a las consultas de reumatología se encuentra en la franja de edad por encima de los 65 años, es importante poder contestar a la pregunta de si el balance beneficio riesgo de las terapias anti TNF se mantiene en este grupo.
MétodosCon el objetivo de valorar si la eficacia y la seguridad de los tratamientos anti TNF era similar en los pacientes ancianos respecto a los pacientes jóvenes, se llevó a cabo una revisión sistemática. Un revisor (NB) diseñó la estrategia de búsqueda, realizó la selección de estudios y llevó a cabo la recogida de datos, bajo la supervisión de otro con experiencia (LC).
Los criterios utilizados para la selección de estudios en esta revisión fueron los siguientes: 1) por tipo de pacientes, que incluyera a ancianos (mayores de 65 años) dentro de los grupos de estudio de AR, EA o APs; 2) por tipo de estudios, no se pusieron limitaciones, salvo revisiones narrativas y series de casos de menos de 10 pacientes; 3) por tipo de medidas de resultado, que incluyera medidas de eficacia y de seguridad.
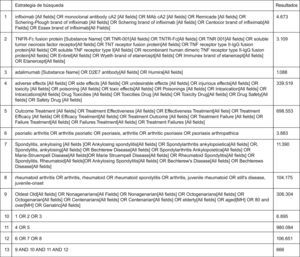
Estrategia de búsquedaSe realizó una búsqueda bibliográfica (disponible en anexo) en Medline vía Pubmed (1976–septiembre 2008) y en Embase vía Ovid (1980–septiembre 2008). La búsqueda incluyó los términos que identificaban a los distintos anti TNF, y se incluyeron además términos que acotaran a ancianos. Se limitó la búsqueda a humanos y a artículos en español, inglés o francés. Los términos infliximab, etanercept, adalimumab y elderly se introdujeron también como buscadores en la Cochrane Library. Asimismo se revisaron los abstracts presentados a los congresos del ACR (2002–2007) y de EULAR (2002–2008) y los artículos publicados sobre anti TNF en Reumatología Clínica (2005–2008). Se revisaron solo los abstracts que en el momento de la revisión estaban disponibles on-line.
Selección de estudiosTeniendo presentes los criterios de inclusión, se realizó una selección inicial de los estudios recuperados por las estrategias de búsqueda a partir de los títulos, seguida de una selección por resúmenes. Se obtuvieron para estudio detallado todos aquellos artículos en los que el resumen orientara a que el artículo podría contener la información necesaria para la revisión, así como aquellos con título dudoso y sin resumen. Una vez recuperados los artículos, se revisaron las listas de referencias para comprobar si existían artículos posiblemente relacionados y no recuperados con la estrategia de búsqueda.
Evaluación de la calidad y nivel de evidenciaDado que la intención inicial era incluir cualquier diseño, no solo ensayos clínicos, y dado que no existen escalas horizontales que permitan evaluar todos los diseños, decidimos establecer un juicio de la calidad en base a los parámetros específicos al tipo de diseño, estableciendo para cada estudio el nivel de evidencia según la escala de Niveles de Evidencia del Oxford Center for Evidence –Based Medicine3. Según esta escala, para preguntas de eficacia y seguridad, los niveles serían: 1a) revisión sistemática de ensayos clínicos con homogeneidad; 1b) ensayo clínico individual con intervalo de confianza estrecho; 1c) ensayo clínico con resultado «todos o ninguno»; 2a) revisión sistemática con homogeneidad de estudios de cohortes; 2b) estudio individual de cohortes o ensayo clínico de baja calidad (p.e., <80% seguimiento); 2c) investigación en resultados de salud, estudios ecológicos; 3a) revisión sistemática de estudios caso control con homogeneidad; 3b) estudio individual caso control; 4) series de casos y estudios de cohortes o casos control de baja calidad; 5) opinión de expertos sin evaluación crítica explícita o basada en fisiología, ciencia básica o principios.
Síntesis de la evidenciaSe crearon hojas de recogida de datos adaptadas a la pregunta de investigación. Se recogieron los siguientes datos de los estudios seleccionados: número de sujetos ancianos en el estudio, enfermedad que padecían, tratamiento biológico que recibieron y la dosis, duración del estudio, variables con las que los autores evaluaron la seguridad o la eficacia del tratamiento biológico, la calidad del estudio y conclusiones a las que llega el estudio. Se creó, con estos datos, una tabla de evidencia en la que apoyar el análisis cualitativo.
ResultadosLos resultados de la búsqueda se detallan en la figura 1. En total se incluyeron 10 estudios, que suman un total de 4.997 pacientes mayores de 65 años tratados con agentes anti TNF, aunque es posible que algunos pacientes estén incluidos en más de un estudio. La mayoría de los datos proceden de subanálisis retrospectivos de ensayos clínicos, aunque también del análisis de registros de pacientes en tratamiento biológico y de bases de datos administrativas con datos de salud. En la tabla 1 se describen ordenados por orden de publicación los estudios incluidos4–13, mostrándose las variables utilizadas para evaluar la eficacia y seguridad en cada estudio. La calidad es moderada, con un nivel de evidencia que oscila entre 2a (3 estudios) y 4 (3 estudios). Puede decirse que toda la evidencia proviene de estudios de AR, dado que el número de pacientes con otras enfermedades es mínimo (265 APs y 276 EA). En la tabla 2 se describen los estudios excluidos14–20.
Tabla de evidencia de los estudios incluidos en la revisión
| Autor, procedencia y año de publicación | Diseño, seguimiento y nivel de evidencia | Pacientes | Intervención | Variables utilizadas para evaluación | |
| Eficacia | Seguridad | ||||
| Genevay et al, Suiza y 2007 | Registro de biológicos | AR | Anti-TNF | DAS 28 | Suspensión del tratamiento por AA |
| n=1.571 | HAQ | ||||
| 2 años | ≥65 a.=344 | Respuesta EULAR | |||
| <65 a.=1.227 | RADAI | ||||
| Nivel Evidencia 2b | |||||
| Schneeweiss et al, EE.UU. y 2007 | Revisión de BD administrativa del sistema de salud de Pensilvania | AR | Metotrexato | NE | Infecciones bacterianas graves |
| n=15.597 (469 tratados con anti TNF) | Otros DMARD | ||||
| ≥65 a.=todos | Anti-TNF | ||||
| GC | |||||
| 8 años | |||||
| Nivel Evidencia 4 | |||||
| Massara et al*, Italia y 2007 | Análisis retrospectivo de BD de un hospital terciario | AR | Infliximab | NE | Efectos adversos |
| n=309 | Etanercept | ||||
| ≥65 a.=73 | Adalimumab | ||||
| <65 a.=236 | |||||
| Nivel Evidencia 4 | |||||
| Schiff et al, EE.UU. y 2006 | Meta-análisis de 3 | AR | Etanercept |
| NE |
| EC y 2 extensiones | ERA: ≥65 a.=37;<65 a.=170 | ||||
| LRA: ≥65 a.=20 | |||||
| Nivel Evidencia 2a | TEMPO: ≥65 a.=50;<65 a.=173 | ||||
| ERA extensión: ≥65 a.=69;<65 a.=47 | |||||
| LRA extensión: ≥65 a.=69;<65 a.=49 | |||||
| Fleischmann, Estados Unidos 2006 | Meta-análisis de 22 ECs | AR | Etanercept | NE |
|
| ≥65 a.=579 | |||||
| <65 a.=2.772 | |||||
| Nivel Evidencia 2a | APs | ||||
| ≥65 a.=14 | |||||
| <65 a.=251 | |||||
| EA | |||||
| ≥65 a.=4 | |||||
| <65 a.=272 | |||||
| Bathon et al, Estados Unidos 2006 | Meta-análisis de 3 EC y 2 extensiones | AR | Etanercept |
|
|
| ERA: ≥69 a.=37;<65 a.=355 | |||||
| LRA: ≥65 a.=39;<65 a.=208 | |||||
| Nivel Evidencia 2a | TEMPO: ≥65 a.=141;<65 a.=541 | ||||
| ERA extensión: ≥65 a.=64;<65 a.=404 | |||||
| LRA extensión: ≥65 a.=93;<65 a.=488 | |||||
| Mariette et al*, Francia, España, Alemania 2006 | EC multicéntrico (REACT Trial) | AR | Adalimumab |
|
|
| <40 a.=1.002 | |||||
| Nivel Evidencia 2b | 40–65 a.=4.125 | ||||
| 66–75 a.=1.245 | |||||
| >75 a.=238 | |||||
| Dabbous et al*, Japón 2006 | Estudio observacional | AR | Infliximab | Escala de 3 ítems |
|
| <45 a.=905 | |||||
| Nivel Evidencia 4 | 45–54 a.=1.213 | ||||
| 55–64 a.=1.692 | |||||
| 65–74 a.=1.003 | |||||
| >75 a.=187 | |||||
| Chevillotte et al, Francia 2005 | Estudio observacional de BD de 9 hospitales 1 año | AR=60 | Infliximab | Suspensión por ineficacia |
|
| EA=23 | |||||
| ≥70 a.=11 | |||||
| Nivel Evidencia 4 | |||||
| Fleischmann et al, EE.UU. 2003 | Meta-análisis de 4 EC y 5 estudios de extensión | AR | Etanercept |
|
|
| N=1128 | |||||
| <65 a.=931 | |||||
| Nivel Evidencia 2a | ≥65 a.=197 | ||||
a.: años; AA: acontecimiento adverso; Aps: artritis psoriásica; AR: artritis reumatoide; BD: base de datos; DLQI: dermatology life quality index; EA: espondilitis anquilosante; EC: ensayo clínico; ERA: estudio randomizado de etanercept con early AR; GC: glucocorticoides; HAQ-DI: health assesment questionaire disease index; LRA: estudio randomizado con etanercept con late AR; NAD: número de articulaciones dolorosas; NAT: número de articulaciones tumefactas; NE: no evaluada; TBC: tuberculosis.
Estudios excluidos y causas de exclusión
| Estudio (año) (referencia) | Causas de exclusión | Tipo de estudio | Referencia del estudio en el que se encuentra incluido |
| Fleischmann (2007)14 | Datos duplicados | Revisión | 8,9 |
| Salliot et al (2007)21 | No se adapta a la pregunta de investigación (evalúa la tasa de infecciones en pacientes con enfermedades reumáticas antes y después del tratamiento con anti TNF) | Estudio de cohortes | No se incluye en los resultados |
| Díaz-Borjon et al (2006)15 | No se adapta a la pregunta de investigación (describe las diferentes opciones de tratamiento biológico en la AR, espondiloartropatías, y otras enfermedades reumáticas, su mecanismo de acción y eficacia, pero no específicamente en ancianos) | Revisión | No se incluye en los resultados |
| Fleischmann (2006)16 | Datos duplicados | Revisión | 8,9 |
| Ornetti et al (2006)17 | Datos duplicados | Revisión | 4,8,9,12,13,18,19,21,22 |
| Harrison (2005)18 | No evalúa seguridad o eficacia. Compara la tasa de tratamientos usados en jóvenes y ancianos | Estudio casos control | No se incluye en los resultados |
| Legrand JL et al (2005)19 | Evalúa los tratamientos usados en el paciente anciano con artritis, incluyendo los anti TNF, la supervivencia del tratamiento, y la tasa de infecciones durante el tratamiento, pero no compara con un grupo control | Estudio de cohortes | No se incluye en los resultados |
| Maillard et al (2005)22 | No se adapta a la pregunta de investigación (Evalúa la tasa de infecciones piógenas en pacientes en tratamiento con anti TNF, no compara la tasa en ancianos con la tasa en jóvenes) | Estudio de cohortes | No se incluye en los resultados |
| Zih et al (2003)20 | No se adapta a la pregunta de investigación (describe los tratamientos anti TNF para artritis inflamatorias y vasculitis pero no específicamente en ancianos) | Revisión | No se incluye en los resultados |
La mayoría de los pacientes estaban tratados con etanercept7–9,13, hay algún artículo que incluye pacientes tratados con infliximab11,12, y se encontró un abstract publicado en la ACR que evaluaba la seguridad y eficacia en pacientes con adalimumab10. En otros artículos no especifica el tipo de anti TNF utilizado4,5. El tratamiento anti TNF es administrado en monoterapia o en combinación con metotrexato.
La mayoría de los artículos consideran paciente anciano al paciente mayor de 65 años, salvo un artículo que analiza pacientes mayores de 70 años12.
Seguridad del tratamiento con etanerceptLa seguridad del tratamiento con etanercept en ancianos se evalúa en el estudio de Fleischmann et al del 20068. Evalúan a pacientes con enfermedades reumáticas que habían participado en ensayos clínicos de eficacia y seguridad de etanercept: pacientes con AR (18 ensayos), artritis psoriásica (2 ensayos) y espondilitis anquilosante (2 ensayos). Se recogieron los datos de seguridad de pacientes a los que se les había administrado al menos una dosis de etanercept.
En este estudio, la proporción de pacientes que presentaban efectos adversos (EA), y efectos adversos importantes (EAI) fue aparentemente mayor en los pacientes mayores de 65 años, tanto si estaban tratados con etanercept o no lo estaban (126/170 (74,1%) EA en pacientes mayores de 65 años en el grupo control, 400/480 (83,3%) EA en pacientes mayores de 65 años en el grupo tratado con etanercept; 647/1.020 (63,4%) EA en pacientes jóvenes en el grupo placebo y 2.046/2.652 (77,1%) EA en pacientes jóvenes tratados con etanercept), pero cuando comparan la diferencia de proporciones de EA, y de EAI (diferencia entre el porcentaje de EA/EAI en los pacientes tratados con etanercept y tratados con placebo) no encuentran diferencias significativas entre los pacientes mayores de 65 años y los más jóvenes. Por otro lado, los pacientes menores de 65 años presentaron más infecciones que los mayores de 65 años debido a que se registró un mayor número de infecciones de vías altas (1.470/2.652 (55,4%) pacientes jóvenes con infecciones en el grupo tratado con etanercept, 406/1.020 (39,8%) infecciones en pacientes jóvenes en el grupo control, 234/480 (48,8%) infecciones en pacientes mayores en el grupo tratado con etanercept, 87/170 (51,2%) infecciones en pacientes mayores en el grupo control). Sin embargo, es de destacar que los pacientes mayores de 65 años presentaron mayor número de infecciones que requirieron hospitalización, pero esta diferencia no era estadísticamente significativa al compararlo con los sujetos menores de 65 años (10,4% en mayores tratados con etanercept, 7,1% en mayores en grupo control, 4% en jóvenes tratados con etanercept, 1,3% en jóvenes en el grupo control). No se describen casos de tuberculosis en ninguno de los grupos. No se encontraron diferencias en cuanto a los eventos cardiovasculares (EC) recogidos (57/650 (8,8%) pacientes mayores: 50 tratados con etanercept y 7 con placebo presentaron EC; 83/3672 (2,3%) pacientes: 78 tratados con etanercept y 5 con placebo, presentaron EC). Se describen 8 casos de enfermedad desmielinizante en los pacientes menores de 65 años. No se registró ninguna enfermedad desmielinizante en los mayores. El número de casos descritos de neoplasias (incluidos los linfomas), permaneció estable a lo largo del tiempo y fue similar en pacientes ancianos y jóvenes, y similar o inferior a la esperada en la población con AR. El número de fallecimientos fue similar en jóvenes que en ancianos, al ajustar las tasas por sexo y edad, pero diferían en cuanto a las causas. La principal causa de muerte en los mayores de 65 años fue cardiovascular y en los menores a 65 años fueron las causas gastrointestinales y las neoplasias.
En el estudio de Fleischmann et al del 20039, el tratamiento con etanercept fue bien tolerado. La mayoría de los efectos adversos fueron leves y ocurrieron con una frecuencia similar en los 2 grupos, salvo las reacciones locales a la inyección (en casos/paciente-año) (4,31 vs 1,47 p=0,036), la cefalea (0,37 vs 0,18 p<0,001) y la rinitis (0,19 vs 0,10 p=0,006) que son más frecuentes en jóvenes, y las infecciones (1,56 vs 1,36 p=0,036) que son más frecuentes en ancianos.
Las infecciones médicamente importantes (que requirieron hospitalización o tratamiento antibiótico endovenoso) fueron muy poco frecuentes [31/931 (3%) de pacientes menores de 65 años, y en un 14/197 (7%) de pacientes >65 años]. Estas infecciones fueron más frecuentes en los pacientes de más de 65 años de manera estadísticamente significativa. Los valores ajustados por tiempo de exposición fueron de 0,09 frente a 0,04 eventos/pacientes/año (p=0,003). En el grupo de pacientes mayores de 65 años se describen 5 fallecimientos. Las causas fueron: herida accidental, fallo cardiaco, cáncer de pulmón, cáncer de ovario, e infección. El número de muertes esperadas para una población de este tamaño para individuos de >65 años es de 6,5. En la población<65 años se describen 3 fallecimientos debidos a cáncer de pulmón, infarto de miocardio, y aneurisma de aorta. Se diagnosticó de cáncer a 9 pacientes menores de 65 años (2 casos) (mama (2 casos), pulmón (2 casos), ovario (2 casos), adenocarcinoma de conducto biliar (1 caso), enfermedad de Hodgkin (1 caso) y linfoma no Hodgkin de la parótida); y a 5 pacientes de más de 65 años (cáncer de próstata (2 casos), cáncer de pulmón (2 casos), enfermedad de Hodgkin (1 caso)). El número de casos esperados de neoplasias calculado por los autores era de 8,4 para los menores de 65 años y 5,5 para los mayores.
El estudio de Bathon et al9 también evalúa la seguridad del tratamiento con etanercept, a partir de la información de pacientes que participaron en los ensayos clínicos controlados LRA y ERA, y los estudios de extensión LRA y ERA, y el estudio TEMPO. En los grupos control de los estudios LRA y ERA, las tasas de efectos adversos, en eventos por paciente/año, tendieron a ser más altas en los pacientes ancianos, que en los pacientes jóvenes (LRA 0,510 vs 0,108; en ERA 0,417 vs 0,072). Al comparar grupos de tratamiento en el estudio controlado LRA, la tasa de efectos adversos era mayor en el grupo de ancianos tratados con placebo (0,510), respecto a los tratados con etanercept (0,116), mientras que las tasas eran comparables en ambos grupos de tratamiento en los pacientes jóvenes (0,108 vs 0,090). En el estudio ERA controlado, la tasa de efectos adversos fue mayor en el grupo tratado con metotrexato para ambos grupos de edad (0,417 vs 0,32 en ancianos y 0,072 vs 0,046 en jóvenes). En el estudio TEMPO, los efectos adversos fueron similares en ancianos y jóvenes tratados con metotrexato (0,240 vs 0,227). En cambio, las tasas de EA fueron más altas en los ancianos frente a los jóvenes en el grupo etanercept (0,360 vs 0,147) y en el grupo etanercept+metotrexato (0,242 vs 0,095).
Las tasas de infecciones fueron similares en ancianos en los estudios controlados ERA y LRA, excepto para los ancianos tratados con etanercept en el estudio LRA en los que no se describieron infecciones (0,680 vs 0,036 en el grupo placebo y 0 vs 0,140 en el grupo etanercept del estudio LRA, y en el estudio ERA fueron de 0,074 vs 0,016 en el grupo MTX y de 0,095 vs 0,010 en el grupo etanercept). Otras comparaciones entre grupos de tratamiento describen tasas similares de infecciones en los estudios controlados ERA, y LRA. En el estudio TEMPO, las tasas de infecciones fueron similares entre los grupos de tratamiento y entre los grupos de edad. Las tasas de infecciones en los estudios de extensión ERA, y LRA, mostraron tasas de infecciones similares a los estudios controlados respectivos. Las 5 infecciones más frecuentes en los estudios de extensión LRA, y ERA fueron la neumonía, la celulitis, la infección no especificada, la artritis bacteriana y la bronquitis. Las tasas de neoplasias fueron bajas.
Los autores dicen que en los estudios de extensión de estos estudios se encontraron tasa más altas de cáncer en los pacientes ancianos que en los pacientes jóvenes, pero el número de casos de cáncer no fue diferente del esperado en la población general. El número de linfomas observado fue mayor a lo esperado en la población general, excepto en los ancianos en el grupo ERA, donde no se detectaron linfomas. No se describieron infecciones oportunistas en los ancianos, en ninguno de los estudios. Se describieron 4 infecciones oportunistas en jóvenes: cistitis candidiásica (2 casos), candidiasis gastrointestinal, y varicela. No se describieron casos de tuberculosis.
Eficacia del tratamiento con etanerceptLa eficacia del tratamiento con etanercept en pacientes ancianos se evalúa en un artículo de Schiff et al7, que incluye pacientes procedentes de los estudios ERA, LRA, y TEMPO, mediante el HAQ y la EVA.
El HAQ-DI basal fue similar en los estudios ERA y TEMPO, y peor en ancianos en el estudio LRA (p<0,05). Ambos grupos ancianos, y jóvenes mostraron mejoría en el HAQ-DI respecto al basal durante los 3 primeros meses (de 0,39 –0,92 en jóvenes, y de 0,57–1,00 en ancianos). Las mejorías se mantuvieron en los estudios de extensión de ERA y de LRA, en ambos grupos de edad, a lo largo de los 48 meses de tratamiento. En los estudios ERA, LRA y TEMPO, el 60–88% de pacientes consiguieron una mejoría en el HAQ-DI de al menos 0,22 con respuesta similar en ambos grupos de edad. La proporción de pacientes que muestran empeoramiento del HAQ fue del 2–16% en ancianos, y del 2–6% en jóvenes. La proporción de pacientes que muestran HAQ de 0 fue de 4–27% en ancianos y de un 10–33% en jóvenes.
Basalmente, los pacientes mayores de 65 años presentaban valores de HAQ peores que los pacientes más jóvenes, atribuyendo esto a la discapacidad asociada a patologías más prevalentes en la edad anciana como la artrosis. La mejoría del HAQ fue similar en pacientes jóvenes y en ancianos.
La EVA basal fue similar en jóvenes y ancianos (de 5,82–6,78 en jóvenes, y de 6,07–6,85 en ancianos), alcanzando una meseta a los 3–6 meses de iniciado el tratamiento. Al final del tratamiento el EVA era de 2,54–3,88 en ancianos, y de 2,44–3,38 en jóvenes.
En el estudio de Bathon et al9, en cuanto al HAQ, los HAQ basales eran peores en los pacientes ancianos. En el estudio LRA, la mejoría media en el HAQ respecto al basal en ancianos tratados con etanercept fue de 0,46 (DE 0,52) a los 6 meses. Las mejorías en el HAQ son similares en ambos grupos de edad. En el ERA, la mejoría fue paralela a los jóvenes, y a los 24 meses fue de 0,46 (DE 0,66) para los ancianos tratados con etanercept. En el TEMPO, la mejoría respecto al basal en pacientes tratados con etanercept a los 12 meses fue de 0,71 (DE 0,78) y de 0,92 (DE 0,70) en los tratados con etanercept y metotrexato.
Se observaron grados de mejoría similares en ancianos y jóvenes, a pesar de que los ancianos presentaron mayor grado de mejoría con la combinación de etanercept y metotrexato, que en monoterapia, en comparación con los jóvenes.
En cuanto a la respuesta ACR, en el estudio LRA, los ancianos tratados con etanercept tenían respuestas ACR similares, o ligeramente más bajas, comparado con los pacientes jóvenes a los 6 meses (ACR 20/50/70 de 70%/45%/15% en ancianos vs 65%/39%/15% en jóvenes). En el ERA las repuestas tendían a ser más bajas en ancianos que en jóvenes a los 24 meses (ACR 20/50/70 de 54%/22%/14% en ancianos vs 77%/54%/32% en jóvenes). En el estudio TEMPO, los ancianos mostraron mayor incremento de eficacia que en jóvenes durante el tratamiento combinado con etanercept y metotrexato, que en monoterapia.
En cuanto a la progresión radiológica, el TSS (total Sharp Score) basal fue mayor en ancianos respecto a jóvenes, en todos los grupos de tratamiento. A pesar de las diferencias basales, los patrones de respuesta fueron similares en jóvenes (−0,73 (DE 0,24)) y en ancianos (TSS de 0,27 (DE 0,70)).
El interés del estudio de Fleischmann13 es que evalúa respuesta durante al menos 1 año. Las respuestas fueron rápidas y mantenidas en los 2 grupos de edad comparados. Un porcentaje similar de pacientes en ambos grupos de edad consiguieron un ACR 20/50/70 (69%/44%/20% vs 66%/40%/15% en jóvenes y ancianos respectivamente, p=0,480). La proporción de pacientes con AR precoz que consiguió un ACR 20 fue similar en ambos grupos de edad (58% vs 51% en jóvenes y ancianos respectivamente, p=0,265). Los hallazgos fueron comparables en los pacientes con AR de larga evolución, en ambos grupos de edad. El tratamiento con etanercept también mostró una mejoría rápida en el número de articulaciones dolorosas y tumefactas en ambos grupos.
Seguridad del tratamiento con infliximabExiste un estudio observacional de Chevillotte et al12 en el que evalúan a 83 pacientes con AR y EA procedentes de una base de datos de 9 hospitales de Borgoña, de los cuales 11 eran mayores de 70 años, en los que se constata un mayor porcentaje de infecciones graves. La suspensión del tratamiento por infecciones graves fue mayor en ancianos pero no de manera significativa, siendo de 18,2% en ancianos, y 2,8% en jóvenes (p=0,08). No se encontraron diferencias en cuanto a efectos adversos (27,2% en ancianos, y 12,5% en jóvenes, p=0,19), o reacciones alérgicas (9,1% en ancianos y 6,9% en jóvenes p=0,59) en ambos grupos de edad.
También existe un estudio publicado en forma de abstract en la ACR11 que evalúa a 5.000 pacientes con artritis reumatoide procedentes de un estudio de investigación postmarketing japonés de infliximab. Los resultados en cuanto a seguridad fueron similares en los pacientes ancianos y en los jóvenes. Transcribo los datos que aportan: El porcentaje de TBC en los subgrupos de edad fue de 0,11% <45a (años), 0,08% 45–54a, 0,4% 55–64a, 0,90% 65–74a, 0,53% ≥75a, p=0,6960; y el porcentaje de reacciones severas a la infusión fue de 0,7%<45a, 0,4% 45–54a, 0,4% 55–64a, 0,5% 65–74a, 0,5%≥75a p=0,6960.
Eficacia del tratamiento con infliximabLos 2 estudios encontrados muestran resultados de eficacia similares en los diferentes grupos de edad. El estudio de Chevillote describe porcentajes de suspensión del tratamiento por ineficacia similares (0% en ancianos, y 16,7% en jóvenes, p=0,35).
En el estudio de Dabbous los porcentajes de pacientes que experimentan mejoría a las 22 semanas son de 91% en <45a, 91% 45–54a, 92% 55–64a, 92% 65–74a, 94%≥75a p=0,8737.
Eficacia y seguridad del tratamiento con adalimumabEn cuanto a pacientes ancianos tratados con adalimumab existe un abstract que evaluaba el tratamiento con adalimumab en diferentes grupos de edad10 (n=1.002<40 años, n=4.125 40–65 años, n=1.245 66–75 años, n=238 >75 años), eran pacientes procedentes del estudio REACT. No se encontraron diferencias en cuanto a eficacia, valorada mediante el DAS28 (el cambio en el DAS28 es de −2,1 en <75a, y de −1,9 ≥75a), el HAQ (el cambio medio en el HAQ es de −0,54 40–<65a, −0,48 65–75a, −0,37≥75a) los criterios ACR (ACR 20/50/70 son respectivamente de 68/40/18% en pacientes de 40–<65a, 68/35/15% en pacientes de 65–75a, 61/35/12% en pacientes >75a) y la suspensión por ineficacia (7% en<65a y 6% en >65a), ni en cuanto a seguridad entre los diferentes grupos de edad (efectos adversos: 8% <40a, 10% 40–<65a,13% 65–<75a,19%≥75a; infecciones: 2,2%<40a, 2,6% 40–65a, 4,8% 65–75a, 5,9%≥75a).
Eficacia y seguridad de los tratamientos anti TNF evaluados conjuntamenteGenevay et al4 evalúan la seguridad y la eficacia de los tratamientos anti TNF en ancianos, incluyen pacientes procedentes del registro de biológicos de Suiza. Se trata de pacientes que habían recibido algún anti TNF, o más de uno. Los pacientes ancianos presentaron mejorías similares a los pacientes jóvenes en las variables de eficacia DAS 28 y RADAI.
El DAS 28 y el HAQ basales eran ligeramente más alto en los pacientes ancianos.
El DAS 28 muestra una disminución significativa y similar en ambos grupos de tratamiento. En ancianos y jóvenes respectivamente, las mejorías en el DAS 28 fueron del −0,63 vs −0,59 al año de tratamiento, y de −0,65 vs −0,58 a los 2 años.
El HAQ disminuye en ambos grupos, sin embargo a los 6 meses el efecto es menor en ancianos: en ancianos y jóvenes respectivamente el HAQ fue de 0,07±0,02 vs 0,09±0,01, y al año 0,08±0,02 vs 0,12±0,02. El análisis por subgrupos mostró ausencia de efecto de los anti TNF en el subgrupo de pacientes mayores a 75 años. En estos pacientes el HAQ empeoró a lo largo de los 2 años del estudio por la aparición de comorbilidad asociada a la edad.
Los criterios de respuesta del EULAR, fueron diferentes en los pacientes ancianos y en los jóvenes. Un porcentaje mayor de pacientes ancianos se clasificaron como malos respondedores (60,2% vs 51,5% p<0,01), y un porcentaje menor como buenos (7,2% vs 11,2% p<0,05). Los autores justifican esta diferencia porque los criterios de respuesta del EULAR dependen del valor absoluto de actividad alcanzado, por lo que las diferencias basales en el DAS28, aunque no las consideran clínicamente relevantes, pueden haber inducido diferencias en el porcentaje de respondedores.
En cuanto a la seguridad, encontraron una tasa de efectos adversos similares en jóvenes y ancianos. Destacan que en los individuos jóvenes se detectó una tasa de interrupción del tratamiento, de manera permanente, por reacciones alérgicas más alta que en ancianos (10,7% en ancianos, 20% en jóvenes), que es estadísticamente significativa cuando se incluyen las interrupciones temporales de tratamiento por reacciones alérgicas (p=0,040). También detectaron una tasa de interrupción permanente del tratamiento por neoplasia superior en ancianos que en jóvenes (7,1% en ancianos, vs 0% en jóvenes p<0,05), aunque describen pocos casos de neoplasias (0 en no ancianos y 2 en ancianos: 1 cáncer de mama con metástasis y un cáncer de páncreas). Las neoplasias descritas no se han asociado con el tratamiento anti TNF. No se encontraron diferencias en la tasa de interrupción permanente del tratamiento por infecciones (12% en jóvenes vs 14,3% en ancianos p=0,75), ni por eventos cardiovasculares entre los 2 grupos de edad (0% en jóvenes vs 3,6% en ancianos p=0,21).
Un estudio publicado en forma de abstract, de Massara et al6, evalúa pacientes en tratamiento con infliximab (n=19 mayores 65 años, n=82 menores de 65 años), etanercept (n=29 >65 años, n=94<65 años), y adalimumab (n=25 >65 años, n=60<65 años). Constata un porcentaje mayor de suspensión del tratamiento a causa de efectos adversos en los pacientes mayores de 65 años que recibían tratamiento con infliximab (57,8% vs 29,2%, p=0,03), y adalimumab (36% vs 15% p=0,06), no así en los pacientes que recibían tratamiento con etanercept (10,3% vs 9,5% p=no significativa).
Otro estudio evalúa el número de infecciones bacterianas graves en pacientes ancianos tratados con anti TNF5. Evalúa pacientes mayores a 65 años con una media de edad de 76,5 años. No lo compara con la población joven, pero cabe destacar que en el grupo de población anciana estudiado, los pacientes con anti TNF tuvieron un riesgo de infección similar a los pacientes tratados con metotrexato y un riesgo de infección inferior a los tratados con glucocorticoides.
DiscusiónSe han analizado los resultados de eficacia clínica y de seguridad de los tratamientos anti TNF en ancianos, en el tratamiento de la AR, la AP, y la EA, mediante una revisión sistemática de la literatura. Los estudios coinciden en una eficacia similar de los tratamientos anti TNF en los pacientes jóvenes y ancianos4,7,10–12, matizado por el estudio de Bathon9, en el que los autores concluyen que los ancianos tuvieron respuestas de eficacia menos robustas que los jóvenes, a pesar de que el patrón de respuesta fue similar en ambos grupos de edad.
En cuanto a la seguridad, existen resultados discordantes. Globalmente, aunque sin significación estadística, en los estudios incluidos los ancianos muestran una tasa de efectos adversos más alta, salvo en las reacciones locales a la inyección, cefalea, rinitis13, reacciones alérgicas4 e infecciones respiratorias, que son más frecuentes en jóvenes13, estas últimas a expensas de más infecciones de vías altas descritas. Otros estudios describen una tasa más alta de infecciones en ancianos12, que requirieron hospitalización8,13. Por otro lado, también encontramos estudios que describen tasas de EA similares en pacientes jóvenes y ancianos5,10,11, y existe un abstract6 que compara a los distintos anti TNF encontrando más efectos adversos en ancianos en los pacientes tratados con infliximab, y adalimumab, y similares en los tratados con etanercept.
En cuanto a las neoplasias, se describen más en ancianos, pero con una frecuencia similar a la esperada por edad9,11,13. No se describen EA atípicos en pacientes ancianos, ni efectos adversos de intensidad mayor, o no descritos en la población joven.
Se deben hacer algunas consideraciones sobre estos resultados. Los estudios publicados para evaluar la seguridad y la eficacia del tratamiento anti TNF en pacientes ancianos están realizados de manera retrospectiva usando bases de datos diseñadas para otros estudios, que no fueron diseñados para evaluar de manera específica la seguridad y eficacia del tratamiento anti TNF en ancianos. Esto puede llevar a sesgos en tanto en cuanto los grupos de edad pueden no estar equilibrados en cuanto a número, pero sobre todo en cuanto a otras variables, que pueden no ser dependientes de la edad, pero que interfieran con los resultados de eficacia o seguridad. Idealmente, se debería haber planeado el análisis por subgrupos en la fase de diseño de los ensayos clínicos por este motivo.
En general, los ensayos clínicos suelen incluir pocos ancianos, por lo que esta población suele estar infrarrepresentada, y se suelen excluir a pacientes con comorbilidades. Esto puede suponer que la población anciana utilizada para el estudio no sea representativa de la población anciana con enfermedades reumáticas8,9. En este sentido, la población de bases de datos administrativas o de registros es más representativa que la de los metaanálisis de ensayos clínicos, aunque el nivel de evidencia sea menor. Por otro lado, intentamos llevar a cabo un metaanálisis de los datos con el que aumentar el poder estadístico global para establecer conclusiones. Sin embargo, el distinto diseño de los estudios, pero especialmente de las distintas medidas de eficacia y seguridad contempladas y de los subgrupos comparados en los diferentes estudios, no nos permitió esta aproximación analítica.
Un aspecto difícil de abordar es la variabilidad existente en la definición de anciano, considerando anciano al individuo mayor de 65 años la mayor parte de las veces. Además, el término «anciano» no es preciso y no tiene en cuenta las diferencias que puede haber entre individuos de más de 65 años, más de 75 años, o más de 80 años, por lo que se requerirían análisis de subgrupos.
En los estudios, el clínico decide qué pacientes son tributarios de tratamiento anti TNF. Esta decisión suele ser tomada con cautela y ello puede constituir un sesgo cuando se analizan los datos, ya que los pacientes mayores tratados podrían pertenecer a un subgrupo de pacientes ancianos con menos factores de riesgo para efectos adversos que la población general de ancianos4,12. Además, existen estudios en los que se aprecian peores índices de actividad y peores índices funcionales al inicio del tratamiento en la población mayor respecto a la población joven4,7,9. Esto podría traducir una actitud más reacia a instaurar el tratamiento anti TNF en los pacientes mayores, constituyendo también un sesgo.
En conclusión, parece que el tratamiento con anti TNF tiene la misma eficacia, o al menos no menor, en pacientes ancianos que en adultos no ancianos. Los resultados son discordantes en cuanto a seguridad y se fundamentan en estudios observacionales. En nuestra opinión, esto se puede interpretar como que en condiciones ideales, en las del ensayo clínico, la seguridad parece razonable, pero en condiciones más reales, como las de los registros, la seguridad no es tan contundente, aunque probablemente esto esté más en relación con la comorbilidad, que con la edad en sí. La mayor parte de la información disponible es con etanercept, existiendo pocos estudios y de calidad baja que evalúen el balance riesgo beneficio del tratamiento con infliximab y adalimumab en ancianos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.