La osteoporosis causa gran morbilidad y mortalidad por el desarrollo de fracturas por fragilidad, entre ellas las vertebrales. Los pacientes con gota podrían mostrar un incremento de riesgo de fracturas osteoporóticas debido a una mayor resorción ósea por un estado inflamatorio producido por los cristales de urato. El objetivo de este estudio fue evaluar el riesgo de fracturas vertebrales dorsales osteoporóticas asociado a padecer gota.
MétodosEstudio transversal realizado con pacientes ingresados por evento cardiovascular. Se seleccionaron pacientes con radiografía torácica lateral reciente al ingreso o en los seis meses previos, que fueron revisadas de forma simultánea por dos observadores desconocedores de los datos clínicos. Se definió fractura vertebral como reducción de la altura vertebral ≥20%, registrando su presencia, número y grado mediante la escala semicuantitativa de Genant. Para analizar la relación entre gota y fractura vertebral, se calculó la odds ratio (OR) con intervalo de confianza al 95% (IC 95%) mediante regresión logística múltiple.
ResultadosSeleccionamos 126 pacientes, de los que 21 (16,67%) padecían gota. Se detectaron 18 casos con fracturas, siendo la prevalencia 14,3%. Se encontró una asociación estadísticamente significativa entre gota y fractura vertebral (28,6% gota, 11,4% no gota; OR 3,10, IC 95% 1,01-9,52). No hubo mayor número de fracturas por grupos, y la severidad fue superior en los controles. La asociación entre gota y fractura vertebral persistió tras ajuste multivariante (OR 5,21, IC 95% 1,32-20,61).
ConclusiónSe ha identificado una asociación independiente entre gota y fracturas vertebrales dorsales radiográficas en pacientes con evento cardiovascular.
Osteoporosis causes significant morbidity and mortality by the development of fragility fractures, including vertebral fractures. Patients with gout may show an increased risk of osteoporotic fractures, as accelerated bone resorption is likely linked to urate crystal-led inflammatory state. This study aims to evaluate the risk of osteoporotic dorsal vertebral fractures associated with gout.
MethodsCross-sectional study carried out in patients admitted for cardiovascular events. Patients with available lateral view of chest radiography (on admission or in the previous six months) were selected. Two observers blinded to clinical data reviewed the radiographies simultaneously. Vertebral fracture was defined as a vertebral height loss ≥20%, and presence, number, and severity (by Genant semi-quantitative scale) were registered. To analyse the relationship between gout and the presence of vertebral fractures, the odds ratio (OR) with 95% confidence interval (95%CI) was calculated by multiple logistic regression.
Results126 patients were analysed, 21 of them (16.67%) suffered from gout. Eighteen cases with fractures were detected, with a prevalence of 14.3%. A significant association was found between gout and vertebral fracture (28.6% gout, 11.4% controls; OR 3.10, 95%CI 1.01-9.52). There were no differences in the number of fractures, while the severity was found to be higher in the controls. The association between gout and vertebral fracture persisted after multivariate adjustment (OR 5.21, 95% CI 1.32-20.61).
ConclusionAn independent association between gout and radiological thoracic vertebral fractures was revealed in patients with a cardiovascular event.
La gota es una enfermedad derivada del depósito de cristales de urato monosódico en áreas articulares, periarticulares y subcutáneas. Se trata de un depósito persistente, pero potencialmente reversible con la normalización de la uricemia. Supone el tipo de artritis más común, manifestándose clínicamente como episodios recurrentes de artritis aguda. La hiperuricemia es una condición necesaria, pero no suficiente, para la aparición de gota, estableciéndose como dintel la concentración sérica de urato superior a 7 mg/dL1,2.
Hasta el momento, la relación entre gota y enfermedad metabólica ósea es incierta. Diversos estudios han demostrado que el ácido úrico puede afectar la homeostasis ósea, pero con resultados contradictorios sobre si ejerce un efecto protector o perjudicial sobre el remodelado óseo2-8. Los cristales de urato monosódico son reconocidos por el sistema inmune innato y producen inflamación mediante la activación del inflamasoma NLRP3, induciendo la síntesis y secreción de citoquinas proinflamatorias (IL-1, IL-6, TNF alfa). Estas citoquinas se han relacionado con la estimulación de la resorción ósea y la inhibición de la osteoformación8. Además, la hiperuricemia parece interrumpir la actividad de la 1-alfahidroxilasa, ocasionando un descenso de 1,25(OH)2-vitamina D y un aumento de la parathormona, lo que implica una mayor resorción ósea3,4,7. Respecto a los estudios clínicos, la asociación entre gota y fractura osteoporótica es controvertida y presenta resultados dispares en la literatura disponible [tabla 1]. De igual forma, se debe especificar si puede haber diferencias entre gota clínica (y sus características y evolución) o hiperuricemia asintomática, analizando además el efecto del tratamiento hipouricemiante. Asimismo, son necesarios estudios en poblaciones más homogéneas. La localización geográfica puede comprometer la validez externa de los resultados, ya sea por calidad de vida o dieta; así como otros factores acompañantes que pueden influir notablemente en la aparición de fracturas, como enfermedad cardiovascular, tabaco, alcohol, actividad física o función renal.
Estudios previos publicados que evalúan la asociación de gota, osteoporosis y fracturas
| Autor,Año | Tipo de estudio | Población estudio | Objetivos | Resultados primarios y secundarios | Conclusión |
|---|---|---|---|---|---|
| Estudios individuales | |||||
| Wang et al. 20183 | Transversal | -Shanghái (China)-55-85 años-Hombres y mujeres-N = 2.674 | Analizar la asociación entre la gota y un aumento de riesgo de fracturas osteoporóticas | -Fracturas osteoporóticas-Mujeres OR = 2IC 95% 1,1-3,6-Varones OR = 1,3IC 95% 0,6-2,9 | -Riesgo incrementado de fractura sólo en mujeres con gota |
| Kok et al. 20184 | Cohortes retrospectivo | - Taiwán- ≥20 años- Hombres y mujeres- N = 108.060 | Examinar si la gota está asociada con un aumento del riesgo de osteoporosis y de fractura (vertebral toraco-lumbar y cadera) | -Diagnóstico médico de osteoporosisIA = 3,3% cohorte gota vs 2,1% cohorte no gotaP = 0,004-Incidencia de fracturaHR = 1,0IC 95% 0,7-1,5 | -Sí aumento riesgo osteoporosis en pacientes con gota.- No aumento del riesgo de fractura toracolumbar por compresión en pacientes con gota |
| Sultan et al. 20185 | Casos y controles prospectivo | - Reino Unido- 63 años-73% Hombres y 27% mujeres- N = 154.742 | Cuantificar el riesgo de primera fractura osteoporótica (vertebras, humero, cadera, muñeca, otras) en pacientes con gota de Reino Unido y valorar el efecto de hipouricemiantes en relación con el riesgo de fractura | -Incidencia de primera fractura osteoporóticaHR = 1,0IC 95% 0,9-1,0 | -No aumento de riesgo en los pacientes con gota- No aumento de riesgo en tratamiento con hipouricemiantes. |
| Paik et al, 20177 | Cohortes prospectivo | - EE. UU.- Mujeres enfermeras- 30-55 años- N = 103.799 | Examinar la asociación entre gota y el riesgo incidente de fractura de cadera o de muñeca | -Incidencia de fractura de caderaRR = 1,4IC 95% 1,1-1,7-Incidencia fractura de muñecaRR = 1,1IC 95% 0,9-1,4 | -Aumento del riesgo de fractura de cadera, pero node muñeca. |
| Dogru et al. 20198 | Trasversal | Turquía75 pacientes con gota (28% mujeres) y 55 controles sanos (34,5% mujeres) | Estudiar la asociación entre gota y osteoporosis densitométrica | -Osteoporosis lumbar: 20% en gota, 7.3% en controles (p = 0,02)-Osteoporosis femoral: 10,7% en gota, 3.6% en controles (NS) | -Asociación entre gota y osteoporosis densitométrica lumbar |
| Revisiones sistemáticas con metaanálisis | |||||
| Zong et al. 20192 | Metaanálisis (estudios observacionales) | -N = 909.803 | Evaluar la asociación de hiperuricemia, gota, fármacos hipouricemiantes con el riesgo de fracturas (vertebral, cadera, muñeca). | -Riesgo para cualquier fracturaRR = 1,2IC 95% 1,0-1,3-Riesgo de fractura osteoporóticaRR = 1,1IC 95% 1,0-1,3 | -Aumenta el riesgo de fracturas osteoporóticas en gota, no en hiperuricemia-No impacto de terapia reductora de uricemia |
| Yin et al. 20176 | Metaanálisis (estudios observacionales) | -N = 291.110 | Determinar si el ácido úrico elevado es un factor protector para fracturas (fractura osteoporótica, fractura de cadera y todo tipo de fracturas). | -Incidencia de diversos tipos de fracturaHR = 0,8IC 95% 0,7-0,9 | -La hiperuricemia no aumenta el riesgo, es un factor protector |
IA: Incidencia acumulada; IC 95%: Intervalo de confianza al 95%; HR: Hazard ratio; NS: no significativo; OR: Odds ratio; RR: Riesgo relativo.
Las fracturas vertebrales osteoporóticas están ligadas a un aumento de la morbimortalidad y a una significativa carga social y económica, por lo que su prevención es fundamental en el contexto de la salud pública9,10. En muchas ocasiones, estas fracturas cursan sin dolor y pasan desapercibidas, por lo que su estudio mediante grandes trabajos de base poblacional constituye un reto. De hecho, con respecto a la gota, el estudio de Kok et al.4 realizado en Taiwán, es uno de los pocos que analiza fracturas vertebrales; los autores no detectaron un riesgo aumentado en pacientes con gota, pero, de nuevo, se trata de fracturas codificadas en historias clínicas, con posibilidad de un notable infra-registro. Por ello, sería interesante establecer la prevalencia y riesgo de fracturas vertebrales osteoporóticas en pacientes con gota, empleando estrategias de detección de fracturas subclínicas.
Para el presente estudio, partimos de la hipótesis que los pacientes con gota presentarán un riesgo aumentado de fractura vertebral de tipo osteoporótico, y con asociación independiente. El principal objetivo de nuestro estudio es evaluar el riesgo de fracturas vertebrales dorsales osteoporóticas, determinadas mediante radiografía torácica lateral, asociado a padecer gota. Como objetivos secundarios pretendemos conocer la influencia de otros factores del paciente como el sexo o grupo de edad en la asociación con gota, así como la posible influencia del grado de control de la enfermedad y el tratamiento específico de la misma.
Material y métodosTipo de estudio y poblaciónEstudio observacional, analítico, de corte transversal o de prevalencia, realizado en el Hospital General Universitario de Alicante. El presente estudio fue aprobado por el comité ético local (ref. 180179).
La población de estudio fueron pacientes incluidos en un estudio previo11, ingresados por evento cardiovascular (síndrome coronario agudo o enfermedad arterial coronaria, insuficiencia cardiaca «de novo» o descompensada, ictus o accidente isquémico transitorio y enfermedad arterial aguda periférica o crónica revascularizada) en los servicios de cardiología, neurología y cirugía vascular del centro, seleccionados mediante muestreo sistemático no consecutivo y entrevistados para estimar la prevalencia de gota en esta población. El número total de pacientes que se reclutó en el estudio fue de 266, y el período de reclutamiento fue de enero a octubre de 2018. Los pacientes se agruparon según el diagnóstico de gota, establecida mediante revisión de historia clínica y entrevista estructurada, en 40 pacientes con gota y 226 pacientes sin gota.
Para el presente análisis secundario, se seleccionaron aquellos participantes con radiografía torácica lateral, disponible en el ingreso por el evento cardiovascular o, en su defecto, la más reciente en los seis meses previos. No se aplicaron criterios de exclusión adicionales.
VariablesEn este trabajo se evaluó la presencia de fracturas vertebrales dorsales detectables mediante radiografía lateral de tórax. Se asumió que las fracturas detectadas a nivel torácico son principalmente de tipo osteoporótico, al ser el tipo de fractura más vinculado con la osteoporosis. Diversos trabajos han mostrado que más del 90% de estas fracturas están relacionadas con una baja densidad mineral ósea, y solo un porcentaje pequeño se atribuye a causas traumáticas o malignas12-14.
La variable principal de estudio fue la prevalencia de fractura vertebral, codificada como variable dicotómica (fractura sí/no). Se consideró fractura vertebral a aquella pérdida de altura igual o superior al 20% respecto a la altura total14. Además, se determinó: 1) el número de fracturas existentes, y 2) mediante la escala de Genant, método de evaluación con el que se visualiza la forma vertebral (cuña, cóncava o aplastamiento) y la disminución existente en la altura vertebral interna, posterior y/o media, se estableció la gravedad de la fractura, en tres grupos: leves o de grado 1 (pérdida de altura entre 20-25%), moderadas o de grado 2 (pérdida de altura entre 25-40%) y graves o de grado 3 (pérdida de altura superior al 40%)15. La escala de Genant ha demostrado una buena concordancia intra e interobservador para la evaluación de fracturas vertebrales.
Como variables independientes, se registró la presencia de gota (definida por criterios clínicos y/o mediante microscopia, según ACR/EULAR16,17), sus características y tratamientos asociados. Además, se recogió la edad en años, posteriormente categorizada en terciles (T1, T2 y T3), IMC (en kg/m2), sexo, factores de riesgo cardiovascular (hipertensión arterial, diabetes mellitus, dislipemia, tabaco, alcohol), enfermedad cardiovascular establecida previa (síndrome coronario agudo o enfermedad arterial coronaria, insuficiencia cardiaca de novo o descompensada, ictus o accidente isquémico transitorio, y enfermedad arterial periférica aguda o crónica revascularizada), presencia de enfermedad renal crónica (filtrado glomerular < 60 ml/min/1,73 m2) y uso de diuréticos hiperuricemiantes (tiazidas o de asa).
ProcedimientosSe revisaron de forma retrospectiva las radiografías de tórax realizadas a los pacientes incluidos en el estudio, en su proyección lateral, para evaluar la presencia, número y severidad de las fracturas vertebrales. Se seleccionó la más próxima a la fecha de inclusión del estudio precedente. En caso de no disponer de dicha técnica durante el ingreso, se revisó su registro electrónico y se tomó la última disponible en los seis meses previos. La revisión se realizó de forma simultánea por dos observadores, desconocedores de los datos clínicos de los pacientes. Las discrepancias fueron comentadas a un tercer investigador (MA), resolviéndose de forma conjunta, siempre sin conocer los datos clínicos de los pacientes. Los observadores previamente realizaron la formación específica web recomendada por la International Osteoporosis Foundation (IOF) denominado «Vertebral fracture teaching program» para facilitar el entendimiento y diagnóstico por imagen de este tipo de fracturas en la práctica clínica, siendo más exhaustivos y minimizando los errores en el momento de evaluar las radiografías de los pacientes17.
Plan de análisisSe utilizaron frecuencias y porcentajes para expresar la variable cualitativa principal (prevalencia de fractura vertebral torácica osteoporótica). En cuanto a las variables cuantitativas, se expresaron medidas de tendencia central como la media y la mediana, y medidas de dispersión como la desviación estándar y percentil 25-75.
Para la estimación de riesgo entre gota y fractura vertebral, se estimó la odds ratio (OR) con un intervalo de confianza al 95% (IC 95%). Se utilizó la prueba χ2 para comparar los diferentes grados en la escala Genant de las fracturas presentes entre los grupos de estudio. Y se usó la U de Mann-Whitney para comparar el número de fracturas existentes. También se usaron la χ2 y test exacto de Fisher para analizar las variables independientes categóricas, y para las cuantitativas se usó la U de Mann-Whitney (edad, índice de masa corporal). Posteriormente, se construyó un modelo de regresión logística multivariante, analizando aquellas variables independientes (gota e insuficiencia renal crónica), con asociación significativa con la dependiente o consideradas clínicamente relevantes (edad, sexo femenino), para analizar el efecto de factores de confusión.
El análisis estadístico se realizó mediante el programa informático SPSS v25 (IBM, Armonk, NY). Para este estudio se empleó un nivel de significación estadística inferior a 0,05.
ResultadosDe los 266 pacientes del estudio, se dispuso de radiografía torácica lateral en 126 pacientes (47,4%), por lo que se seleccionaron para el presente análisis. No hubo diferencias en la disponibilidad de radiografías por grupos de estudio (52,5% en gota versus 46,5% en no gota, p = 0,481). Los pacientes incluidos o excluidos según la disponibilidad de las radiografías laterales de tórax, mostraron características clínicas comparables (material suplementario, Tabla 1 S).
La tabla 2 muestra la población total y los grupos de estudio. Los grupos fueron comparables de forma global, salvo en cuanto a la presencia de enfermedad renal crónica, superior en aquellos con gota. Se recogieron diferentes características relacionadas con la gota, las cuales se muestran en la tabla 3.
Características clínicas de la población de estudio y comparativa por grupos de interés. Datos mostrados como n (%), salvo especificado lo contrario
| Total (n = 126) | No Gota (n = 105) | Gota (n = 21) | P | |
|---|---|---|---|---|
| Edad (años), mediana (p25-75) | 71 (62-78) | 70 (61-78) | 74 (68-78) | 0,098 |
| Sexo femenino | 36 (28,6) | 32 (30,5) | 4 (19,0) | 0,290 |
| Hipertensión arterial | 102 (81,0) | 83 (79,0) | 19 (90,5) | 0,223 |
| Diabetes mellitus | 69 (54,8) | 57 (54,3) | 12 (57,1)) | 0,810 |
| Dislipemia | 84 (66,7) | 73 (69,5) | 11 (52,4) | 0,128 |
| Consumo activo de tabaco | 29 (23,0) | 25 (23,8) | 4 (19,0) | 0,636 |
| Consumo activo de alcohol | 24 (19,0) | 21 (20,0) | 3 (14,3) | 0,543 |
| IMC (kg/m2), mediana (p25-75) | 27,5(24,6-30,8) | 27,3(24,5-30,5) | 27,9(25,6-30,8) | 0,290 |
| Enfermedad renal crónica | 37 (29,4) | 26 (24,8) | 11 (52,4) | 0,011 |
| Uso de diuréticos hiperuricemiantes | 58 (46,0) | 47 (44,8) | 11 (52,4) | 0,523 |
Características clínicas y de tratamiento del grupo con gota
| Gota (n = 21) | |
|---|---|
| Uricemia en el evento cardiovascular, mediana (p25-75) [n = 11] | 7,2 (4,4-8,3) |
| Uricemia en cinco años previo, mediana (p25-75) [n = 19] | 6,5 (4,5-7,5) |
| Uricemia en objetivo actual, % [n = 11] | 27,3 |
| Años desde el primer episodio, mediana (p25-75) | 20,0 (8,0-30,0) |
| Núm. episodios, mediana (p25-75) | 3,0 (1,0-13,5) |
| Núm. articulaciones, mediana (p25-75) | 1,0 (1,0-2,0) |
| Presencia de tofos, % | 0 |
| Hipouricemiante, % | 61,9 |
| Hipouricemiante al ingreso, % | 42,9 |
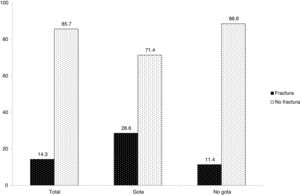
Se detectaron 18 casos con fracturas, siendo la prevalencia global de fracturas en la población de estudio del 14,3%. De éstos, seis pacientes pertenecían al grupo de gota (28,6% del total de este grupo) mientras que 12 pacientes pertenecían al grupo no gota (11,4% del total de este grupo) (fig. 1). Respecto a la comparación por grupos, se encontró una asociación estadísticamente significativa entre gota y fractura vertebral (OR 3,1, IC 95% 1,01-9,52).
En un análisis de prevalencia según el tercil de edad, los resultados encontrados fueron los siguientes: en el tercil 1 (≤ 64 años), hubo una prevalencia de fractura del 50,0% en el grupo gota frente a una prevalencia de fractura de 7,5% en el grupo no gota (p = 0,184). En el tercil 2 (64,1-74,0 años), la prevalencia de fractura fue de 30,0% en el grupo gota frente a 6,9% en el grupo no gota (p = 0,096). Y en el tercil 3 (≥ 74,1 años), existía una prevalencia de fractura del 22,2% en el grupo gota y de 19,4% en el grupo no gota (p = 1,000).
En el subanálisis por sexo, la prevalencia de fractura en las mujeres con gota fue de un 50,0% frente a un 28,1% en las mujeres que no presentaban gota (p = 0,570). Respecto a la prevalencia de fractura de los hombres con gota, ésta fue de un 23,5%, frente a un 4,1% en los hombres que no padecían gota (p = 0,022).
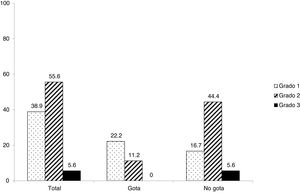
En cuanto al número de fracturas por paciente, la mediana de fracturas fue de 0 (p25-75 0-0) para el grupo sin gota y de 0 (0-1) para el grupo con gota, sin alcanzar diferencias estadísticamente significativas (p = 0,051). El número máximo de fracturas por paciente encontrado para cada grupo fue de cuatro fracturas para el grupo no gota y de dos fracturas para el grupo gota. Respecto a la severidad de las fracturas según la escala de Genant, siete pacientes presentaron fracturas grado 1 (38,9%), 10 pacientes grado 2 (55,6%) y un paciente grado 3 (5,6%) (fig. 2). Estas puntuaciones de la escala Genant mostraron diferencias por grupos (p = 0,028): en gota, 22,2% grado 1, 11,1% grado 2 y ningún grado 3, mientras que, en el grupo sin gota, 16,7% mostraron un grado 1, 44,4% un grado 2, y 5,6% grado 3).
Además de gota, el análisis multivariante incluyó como covariables la edad, el sexo femenino y la enfermedad renal crónica. Los resultados se muestran en la tabla 4: padecer gota mostró una asociación estadísticamente significativa e independiente con la presencia de fractura vertebral dorsal radiográfica.
Modelo de regresión logística múltiple para evaluar la asociación con la variable de resultado (presencia de fractura vertebral torácica radiográfica)
| Odds ratio ajustada | IC 95% | p-valor | |
|---|---|---|---|
| Gota | 5,21 | 1,32-20,61 | 0,019 |
| Edad | 1,04 | 0,98-1,10 | 0,176 |
| Sexo femenino | 6,40 | 1,90-21,53 | 0,003 |
| Enfermedad renal crónica | 0,34 | 0,14-1,95 | 0,336 |
En el presente estudio transversal, llevado a cabo en pacientes ingresados por evento cardiovascular, se ha identificado la presencia de una prevalencia de fractura vertebral dorsal radiográfica que puede considerarse elevada (14,3%). Además, se ha identificado una asociación estadísticamente significativa entre tener gota y presentar una fractura vertebral dorsal radiográfica. Dicho riesgo ha persistido pese a ajustar por factores de confusión, lo que sugiere un efecto directo e independiente. En el grupo de pacientes con gota, el número de fracturas únicamente fue superior de forma numérica, aunque con menor grado de severidad según la escala de Genant. Al tratarse de una muestra seleccionada, estos resultados deben confirmarse en poblaciones con gota más numerosas y sin evento cardiovascular asociado.
En ambos sexos se encontró un mayor porcentaje de pacientes que sufrieron fracturas en el grupo con gota, pero esta diferencia únicamente fue significativa en los hombres. La tasa de fractura en hombres sin gota con evento cardiovascular fue la más baja de la serie (4,1%). Este hecho probablemente se deba a la baja frecuencia de otros factores osteopenizantes en esos pacientes, ya que la enfermedad cardiovascular por sí misma no se considera como tal18. De hecho, parece existir un fuerte vínculo a la inversa, relacionando la osteoporosis con la aparición de arteriosclerosis y el desarrollo de eventos cardiovasculares18-20.
Por los tres grupos de edad, el porcentaje de pacientes con fractura fue superior en aquellos que padecían gota. La comparación no alcanzó la significación probablemente por el bajo tamaño de cada grupo por separado. La detección de fracturas en población más joven demuestra el papel de la inflamación en el desarrollo de osteoporosis y fracturas, tal y como ocurre en otras enfermedades21,22. Una elevada carga inflamatoria en un paciente podría considerarse como indicación para cribado de osteoporosis y de fracturas, pese a la ausencia de otros factores de riesgo. Hasta el momento, la única enfermedad inflamatoria contemplada como tal es la artritis reumatoide23,24, pero la gota podría ser otra de ellas.
El reducido tamaño muestral en el grupo de pacientes con gota impidió un subanálisis sobre el impacto del control de la enfermedad (ataques de gota o tratamiento hipouricemiante). Ninguno de los pacientes presentaba tofos, indicativos de gota insuficientemente tratada; junto a la carga inflamatoria de la gota tofácea25, las fracturas en este grupo también podrían asociarse a la activación local de osteoclastos inducida por los cristales de urato monosódico26. Un estudio reciente concluye que el tratamiento hipouricemiante prescrito de manera temprana en el curso de la enfermedad no parece afectar al riesgo de fractura a largo plazo5. En la misma línea, la hiperuricemia no se asocia al riesgo de fractura mientras que padecer gota sí guarda relación2,5. Asimismo, la presencia de cristales de urato en hiperuricemia asintomática, estimado en cerca del 20% de los sujetos, no ha sido evaluada con esta perspectiva hasta la fecha. Dichos cristales, a través de mediadores inflamatorios, podría acelerar la resorción ósea5, siendo quizá su situación comparable a la gota clínica.
Como fortalezas del estudio destacamos que los investigadores realizaron una formación previa, avalada por la IOF, para analizar y evaluar las radiografías de forma sistemática. En el momento de evaluar la radiografía, desconocían cualquier característica del paciente, de este modo se evitaba un posible sesgo de clasificación. También cabe destacar el uso de la escala de Genant como método semicuantitativo, siendo la escala más útil y la más frecuentemente utilizada en la valoración de estas fracturas osteoporóticas, existiendo muy pocas diferencias intra e interobservadores.
Los pacientes con gota presentan con mayor frecuencia factores del síndrome metabólico (hipertensión arterial, dislipemia, obesidad), enfermedad cardiovascular y enfermedad renal27,28. Sin embargo, en el presente estudio únicamente se ha detectado una mayor prevalencia de enfermedad renal crónica. Este hecho probablemente se debe a la población de estudio (hospitalaria, mayoritariamente masculina y con evento cardiovascular), que de base cuenta con una elevada prevalencia de factores de riesgo tradicionales29. Este hecho debe tenerse en cuenta ya que puede limitar la extrapolación de resultados. Por otro lado, la relación entre hiperuricemia-gota y enfermedad renal es muy estrecha, con implicaciones patogénicas y pronósticas entre ambas entidades30,31. En población ingresada por evento cardiovascular, en caso de no disponer de resultados de uricemia, la enfermedad renal predice de forma independiente la presencia de gota11.
En cuanto a las limitaciones, la principal fue la significativa reducción del tamaño muestral dada la baja disponibilidad de radiografía torácica lateral, pese tratarse de pacientes ingresados por un evento cardiovascular; no obstante, dichas pérdidas fueron similares en ambos grupos, grupos además con características comparables. La evaluación de fracturas se realizó sobre radiografías de tórax, no dirigidas a la exploración específica de la columna vertebral; esto pudo influir a la hora de interpretarlas, si bien trabajos previos avalan la utilización de radiografías torácicas laterales para la identificación de fracturas, en su gran mayoría asintomáticas, por lo que pasan desapercibidas12,14. Además, muchos pacientes recibían tratamiento diurético, lo cual también puede influir en el desarrollo de osteoporosis y fracturas. Las tiazidas pueden atenuar la pérdida ósea estimulando la reabsorción de calcio en el túbulo distal, mientras que los diuréticos de asa tienen un efecto opuesto32. Se ha de tener en cuenta que el número de pacientes que presentaban gota era pequeño en esta subpoblación.
La importancia de este trabajo radica en que, si estudios posteriores confirman la asociación entre gota y fractura vertebral dorsal, se podría realizar una búsqueda activa de fractura o un cribado mediante densitometría a todos aquellos pacientes con gota, identificándolos y tratándolos a tiempo para evitar la gran morbimortalidad que supone una fractura osteoporótica. De hecho, la osteoporosis no es todavía una de las comorbilidades a evaluar en pacientes con gota según los expertos de EULAR33. En investigaciones futuras se podría analizar la relación en base al control de la uricemia y la aparición de fracturas en función del nivel de ácido úrico de cada paciente. De cara a nuevos estudios sería conveniente ampliar el número de pacientes en el grupo gota para poder hacer comparaciones más consistentes, incluir un mayor número de mujeres, y analizar fracturas a otros niveles.
ConclusiónLa prevalencia de fractura se muestra aumentada en pacientes ingresados por evento cardiovascular que presentaban gota, y tal asociación es independiente de otras variables. Ese incremento de riesgo de fracturas en gota se apreció para ambos sexos, si bien sólo fue significativa en hombres (donde podría influir más la carga inflamatoria). Además, detectar un incremento de fracturas en grupos de menor edad refuerza el papel de la inflamación como factor osteopenizante. Queda por dilucidar la influencia del control de los niveles de uricemia en la aparición de fracturas osteoporóticas. Aunque debe ser confirmado en investigaciones futuras, se podría considerar el cribado de osteoporosis y fracturas en pacientes con gota y enfermedad cardiovascular.
FinanciaciónEl presente trabajo ha recibido financiación del Instituto de Investigación Sanitaria y Biomédica de Alicante (V Convocatoria de Ayudas para el Apoyo y Fomento de la Investigación, exp. 180179).
Conflicto de interesesMA declara honorarios como ponente y becas de investigación por parte de laboratorios Grünenthal y Menarini. El resto de autores declara no tener conflictos de interés con respecto al actual trabajo de investigación.
A Antonio Palazón Bru por su asesoramiento estadístico.