Distintos modelos de predicción han sido aplicados en pacientes con artritis indiferenciada (AI) con el objetivo de identificar a aquellos que progresarán a artritis reumatoide (AR). El modelo de predicción de Leiden (MPL) ha demostrado su utilidad en distintas cohortes de AI.
ObjetivoAplicar el MPL a una cohorte de pacientes con AI del noreste de México.
MétodosSe incluyó a 47 pacientes con AI; al ingreso se aplicó el MPL, después de un año de seguimiento se clasificaron en 2 grupos: los que progresaron a AR (de acuerdo con los criterios ACR 1987) y los que no progresaron.
ResultadosEl 43% de los pacientes con AI progresó a AR. De los pacientes que progresaron a AR, el 56% obtuvo una puntuación ≤ 6 y solo el 15% ≥ 8 puntos. El 70% de los que no progresaron alcanzaron una puntuación entre 6 y ≤ 8. No existió diferencia en la mediana de la puntuación del MPL entre los grupos, p=0,940.
ConclusiónLa mayoría de los pacientes que progresó a AR obtuvieron menos de 6 puntos en el MPL. A diferencia de lo observado en otras cohortes, en nuestra población el modelo no permitió predecir la progresión de la enfermedad.
Different prediction rules have been applied to patients with undifferentiated arthritis (UA) to identify those that progress to rheumatoid arthritis (RA). The Leiden Prediction Rule (LPR) has proven useful in different UA cohorts.
ObjectiveTo apply the LPR to a cohort of patients with UA of northeastern Mexico.
MethodsWe included 47 patients with UA, LPR was applied at baseline. They were evaluated and then classified after one year of follow-up into two groups: those who progressed to RA (according to ACR 1987) and those who did not.
Results43% of the AI patients developed RA. In the RA group, 56% of patients obtained a score ≤ 6 and only 15% ≥ 8. 70% who did not progress to RA had a score between 6 and ≤ 8. There was no difference in median score of LPR between groups, p=0.940.
ConclusionMost patients who progressed to RA scored less than 6 points in the LPR. Unlike what was observed in other cohorts, the model in our population did not allow us to predict the progression of the disease.
La artritis reumatoide (AR) es una enfermedad inflamatoria crónica caracterizada por deterioro articular progresivo que puede generar incapacidad permanente, lo que afecta la calidad de vida y economía del paciente, debido al ausentismo laboral y al alto costo del tratamiento1. El diagnóstico y el tratamiento en etapas iniciales evitan la progresión de la enfermedad2. La identificación de los pacientes con mayor riesgo de progresión a AR es fundamental para el rápido inicio de tratamiento y constituye uno de los objetivos de las Clínicas de Artritis Temprana (CAT), en las que habitualmente se incluyen pacientes con artritis indiferenciada (AI), definida como la artritis que no reúne criterios de clasificación de una enfermedad inflamatoria específica3. Los pacientes con AI pueden evolucionar a la remisión, permanecer como AI, o progresar a una enfermedad inflamatoria definida, como la AR4. Se han desarrollado diferentes modelos de predicción para evaluar a los pacientes con AI que están en riesgo de desarrollar AR5,6; la Universidad de Leiden elaboró un modelo de predicción (MPL) para identificar a estos pacientes, con una metodología previamente descrita7. El MPL incluye las siguientes variables clínicas: edad, sexo, distribución de articulaciones afectadas, severidad de la rigidez matutina, articulaciones dolorosas e inflamadas, medición de la proteína C reactiva (PCR), la presencia de factor reumatoide (FR) y de anticuerpos antipéptidos cíclicos citrulinados (anti-PCC). Este modelo establece una probabilidad del 84% de progresión a AR en el primer año en aquellos pacientes que presentan al inicio de su evaluación una puntuación igual o mayor a 8. El MPL ha sido aplicado y validado en diversas cohortes en el mundo, con diferentes criterios de inclusión8-10. En México, no se ha reportado la aplicación de este modelo, por lo que el objetivo de este estudio fue conocer si el MPL es de utilidad en nuestra población para predecir la progresión de AI a AR.
Material y métodosSe seleccionó a pacientes pertenecientes a una CAT establecida en un hospital universitario de tercer nivel, que atiende a pacientes del noreste de México. La CAT está integrada por individuos mayores de 18 años, provenientes de un estudio epidemiológico del estado de Nuevo León, realizado mediante la metodología Community Oriented Program for the Control of the Rheumatic Diseases, COPCORD por sus siglas en inglés) que ha sido previamente descrito11 y por pacientes que son referidos de otras consultas que acuden al hospital. Los pacientes, al ser ingresados a la CAT, se clasifican en alguno de los siguientes 3 grupos: aquellos con AR de menos de un año de inicio de sintomatología, los que tienen AI definida por la presencia de una o más articulaciones inflamadas por más de una semana y menos de un año de evolución, y otro grupo de pacientes en alto riesgo de artritis (pacientes con dolor articular sin presencia de artritis). Se excluye a los pacientes que cumplen criterios de clasificación de otras enfermedades inflamatorias bien definidas a su ingreso. Dos reumatólogos certificados evalúan a los pacientes en la CAT en cada visita, en las que se realiza exploración física con evaluación de articulaciones inflamadas y dolorosas.
En este estudio, comprendido entre el año 2008 y el 2011, se incluyó solo a pacientes con AI a quienes se les aplicó el MPL al ingreso a la clínica. A todos los pacientes se les realizó en su primera visita FR por nefelometría (Behring nefelómetro láser no. 441197/71160) y anticuerpos anti-PCC por medio de ELISA de primera generación (EUROINMUN®) y en cada evaluación se determinó velocidad de sedimentación globular y PCR.
Posteriormente, al año de seguimiento, los pacientes se reclasificaron sobre la base de la progresión o no a AR de acuerdo con los criterios de clasificación de 1987 del Colegio Americano de Reumatología12.
Análisis estadístico: las variables numéricas se expresaron con media ± desviación estándar o mediana y rango intercuartílico (RIQ), de acuerdo con su distribución. Las variables categóricas se expresaron con porcentajes. Se realizó un análisis bivariado de las variables numéricas comparando con la t de Student o la U de Mann Whitney en función de su distribución. Para las variables categóricas se utilizó la prueba de la chi al cuadrado. EL MPL se analizó comparando las medianas de la puntuación obtenido con la prueba de U de Mann-Whitney; posteriormente, se subdividió a los pacientes de acuerdo con el resultado en mayor o menor de 8 puntos y se evaluó por medio de la curva de Kaplan-Meier a un año de sobreviva para progresar a AR. Finalmente, se realizó una gráfica de distribución de acuerdo con la puntuación obtenida del MPL y la progresión o no a AR.
ResultadosSe incluyó a 47 pacientes con AI, con una edad media de 51,6±9,5 años, 46 pacientes (98%) mujeres; 42 (89%) pacientes provenían del estudio COPCORD. Al final del seguimiento, 20 pacientes (43%) desarrollaron AR (grupo AR) y 27 (57%) no progresaron a AR (grupo no AR). En el grupo no AR, 6 pacientes (13%) presentaron resolución de la artritis, 12 pacientes (25%) persistieron con AI, 9 pacientes (19%) cumplieron criterios de clasificación de otras enfermedades reumáticas (6 con la osteoartritis, uno con fibromialgia, uno con síndrome de Sjögren y uno con artritis enteropática).
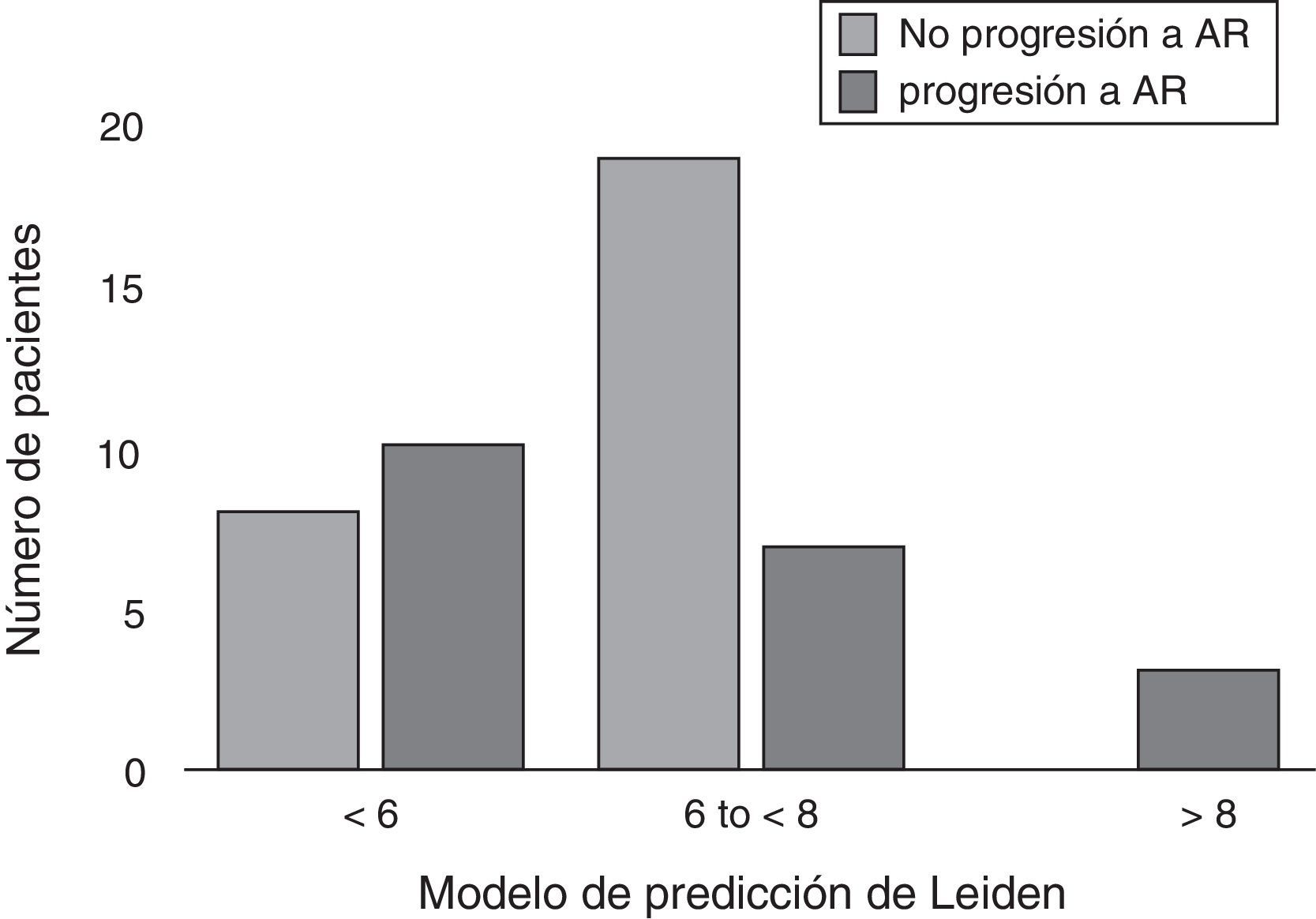
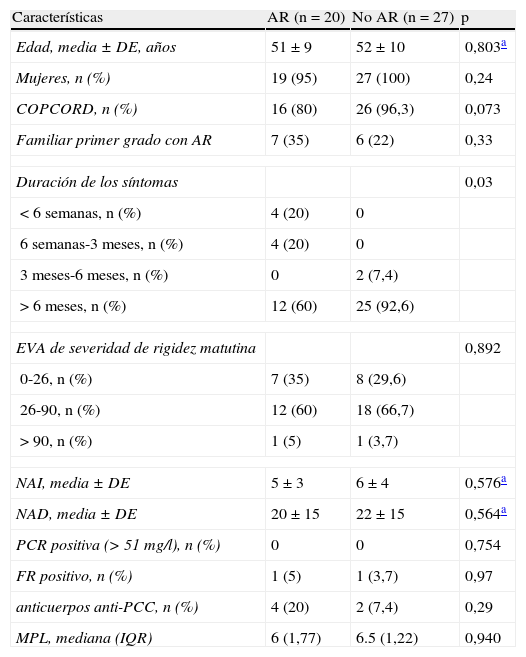
Las características basales de los pacientes y el análisis bivariado se muestran en la tabla 1. En la evaluación de la puntuación obtenida por MPL, en el grupo AR se encontraron: 10 pacientes (50%) con una puntuación < 6, 7 pacientes (35%) con una puntuación entre 6 y < 8, y finalmente 3 pacientes (15%) con ≥ 8 puntos. En el grupo no AR se encontró: 8 pacientes (30%) con < 6 puntos, 19 pacientes (70%) con una puntuación entre 6 y < 8, y ninguno con 8 o más puntos (fig. 1). El grupo AR tuvo una puntuación media del MPL de 6 (RIQ 1,77), mientras que en el grupo no AR fue 6,5 (RIQ 1,22) (p=0,940).
Características basales y análisis bivariado
| Características | AR (n=20) | No AR (n=27) | p |
| Edad, media ± DE, años | 51 ± 9 | 52 ± 10 | 0,803a |
| Mujeres, n (%) | 19 (95) | 27 (100) | 0,24 |
| COPCORD, n (%) | 16 (80) | 26 (96,3) | 0,073 |
| Familiar primer grado con AR | 7 (35) | 6 (22) | 0,33 |
| Duración de los síntomas | 0,03 | ||
| <6 semanas, n (%) | 4 (20) | 0 | |
| 6 semanas-3 meses, n (%) | 4 (20) | 0 | |
| 3 meses-6 meses, n (%) | 0 | 2 (7,4) | |
| > 6 meses, n (%) | 12 (60) | 25 (92,6) | |
| EVA de severidad de rigidez matutina | 0,892 | ||
| 0-26, n (%) | 7 (35) | 8 (29,6) | |
| 26-90, n (%) | 12 (60) | 18 (66,7) | |
| > 90, n (%) | 1 (5) | 1 (3,7) | |
| NAI, media ± DE | 5 ± 3 | 6 ± 4 | 0,576a |
| NAD, media ± DE | 20 ± 15 | 22 ± 15 | 0,564a |
| PCR positiva (> 51mg/l), n (%) | 0 | 0 | 0,754 |
| FR positivo, n (%) | 1 (5) | 1 (3,7) | 0,97 |
| anticuerpos anti-PCC, n (%) | 4 (20) | 2 (7,4) | 0,29 |
| MPL, mediana (IQR) | 6 (1,77) | 6.5 (1,22) | 0,940 |
Análisis estadísticos realizados por chi al cuadrado.
anti-PCC: anti-péptidos cíclicos citrulinados; AR: artritis reumatoide; DE: desviación estándar; EVA: escala visual análoga; FR: factor reumatoide; RIQ: rango intercuartílico; NAI: número de articulaciones inflamadas; NAD: número de articulaciones dolorosas; PCR: proteína C reactiva.
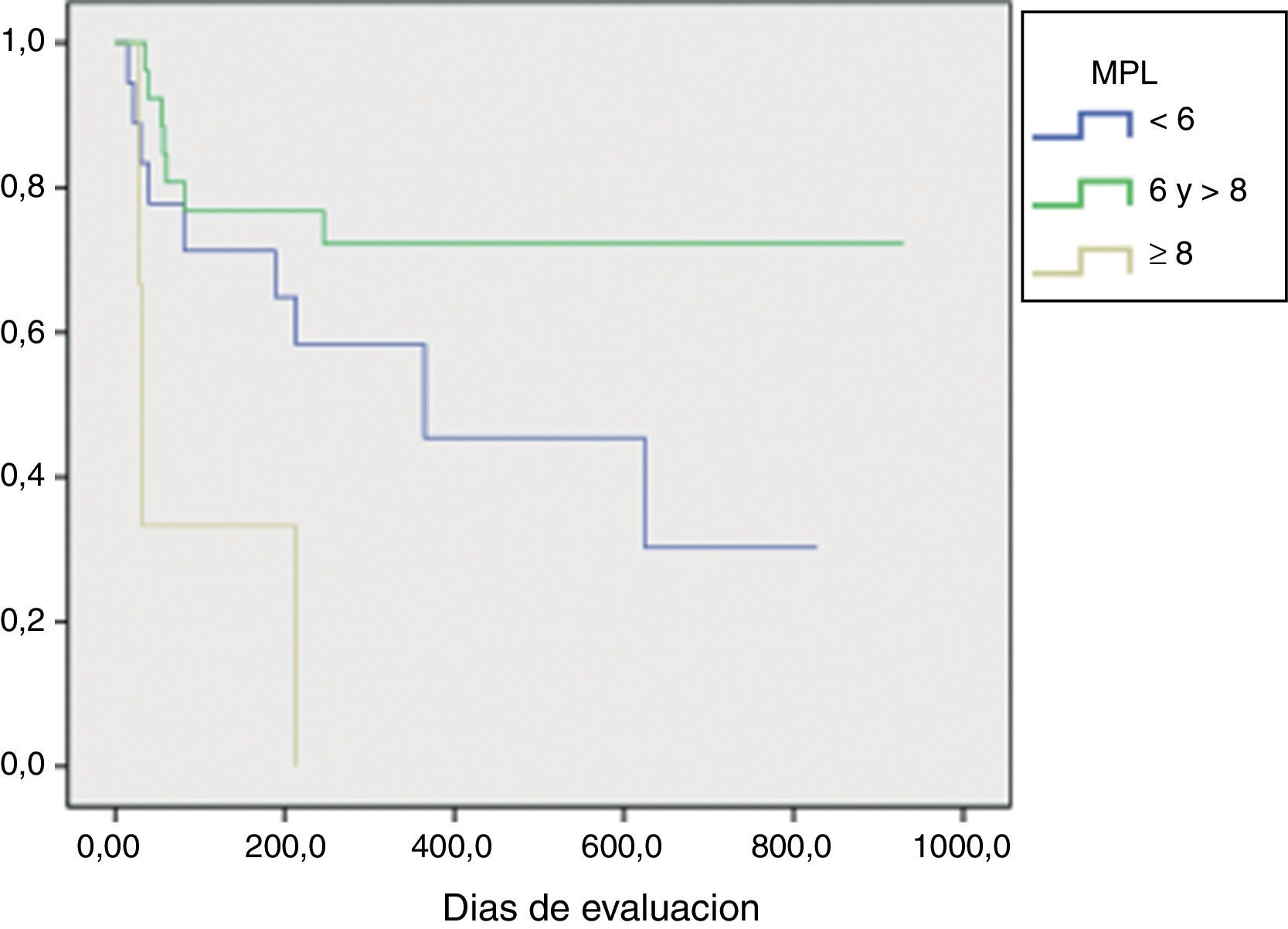
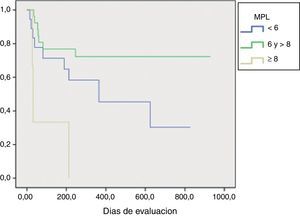
La puntuación MPL se evaluó mediante Kaplan Meier y Log rank, y se encontró que los pacientes con una puntuación ≥ 8 mostraron una diferencia estadísticamente significativa en la progresión a AR (p=0,01) (fig. 2).
DiscusiónLa detección temprana de los pacientes con AI en alto riesgo de progresión a AR se ha convertido en el reto actual para iniciar el tratamiento de manera oportuna y, por lo tanto, modificar el curso de la enfermedad y prevenir la destrucción articular, la deformidad y la discapacidad de los pacientes13.
En las características basales de nuestra población encontramos resultados significativos en la duración de la enfermedad para la progresión a AR, observando que la mayoría de los pacientes que progresaron a AR tenían una evolución mayor a 6 meses, aunque también fue significativo en el grupo no AR; así mismo se observó una baja prevalencia de FR y anticuerpos anti-PCC en los 2 grupos evaluados, sin encontrar diferencia entre los grupos y la progresión a AR (p=0,97 y p=0,29, respectivamente).
La incidencia de progresión de AI a AR en nuestra clínica fue similar a la reportada por otros estudios. A diferencia de otras cohortes en las que el MPL ha sido previamente validado, donde en cada una se utilizaron criterios de inclusión diferentes, los pacientes que progresaron a AR en este estudio obtuvieron una puntuación menor8-10. En nuestra cohorte, todos los pacientes que lograron una puntuación de 8 o más progresaron a AR, aunque la mayoría de los pacientes de este grupo obtuvo una puntuación menor a 6, por lo tanto, este resultado no nos permitió identificar a los pacientes que progresarán AR mediante el MPL (fig. 1). Datos similares a nuestro estudio fueron publicados recientemente por Krabben et al.; quienes evaluaron 1.219 pacientes con AI y su riesgo de progresión a AR en 3 diferentes cohortes (Leiden, Birmingham y Ámsterdam), utilizando el MPL y la presencia de otras variables, como los autoanticuerpos. Al final de la evaluación, se observó que solo del 0-6% de los pacientes presentó anticuerpos anti-PCC y 0-1% presentaron puntuaciones altas del MPL, resultando estas 2 variables insuficientes para predicción de progresión a AR14.
Los modelos de predicción de AI a AR han sido aplicados en clínicas de referencia, pero no se ha reportado su uso a nivel comunitario. La metodología COPCORD permite la identificación de pacientes con afecciones musculoesqueléticas dolorosas en población abierta, incluso antes de la referencia a un médico15. La mayoría de nuestros pacientes provenían del COPCORD y el 40% de los pacientes que progresaron a AR fueron incorporados al estudio con menos de 3 meses de evolución, lo que de alguna manera podría aumentar la posibilidad de resultados negativos en el FR y los anticuerpos anti-PCC y, por lo tanto, en la puntuación de MPL.
Existen limitaciones en el estudio que deben considerarse en el momento de interpretar los resultados; la primera es que el tamaño de muestra fue pequeño, aunque se incluyó la totalidad de los pacientes con AI de la CAT; sin embargo, nos permitió observar el bajo desempeño del MPL en nuestra población; la segunda limitación es que la determinación de los anticuerpos anti-PCC fue por ELISA de primera generación, cuya sensibilidad es menor que los de segunda generación16, lo cual pudo influir en la baja puntuación del MPL. La diferencia entre articulaciones dolorosas e inflamadas en el grupo AR puede explicarse por la procedencia de los pacientes y además, debido a que no se ajustó el estudio para la presencia de otras enfermedades concomitantes, como fibromialgia, que pueden aumentar la percepción de dolor.
En conclusión, el 43% de los pacientes con AI progresó a AR tras un año de seguimiento. El 56% de los pacientes que progresaron a AR obtuvo una puntuación ≤ 6 en el MPL, diferente de lo reportado en la cohorte de Leiden, donde fue menos del 10%; estos resultados no nos permitieron establecer una relación de predicción de progresión a AR con el MPL.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran que no existe ningún conflicto de interés en el presente escrito.