La hemorragia pulmonar (HP) se presenta en el 2 al 5% de los pacientes con lupus eritematoso sistémico (LES) y puede alcanzar una mortalidad del 70 al 90%. Los criterios para el diagnóstico de HP son: a) infiltrados alveolares en 3 cuartas partes de los campos pulmonares en la radiografía de tórax; b) insuficiencia respiratoria de inicio agudo, y c) descenso de la hemoglobina > 3g/dl. La HP puede conducir a neumonía organizada, depósito de colágeno en vías aéreas pequeñas y, consecuentemente, fibrosis pulmonar, lo cual puede alterar la función pulmonar con cambios obstructivos o restrictivos.
ObjetivoEstablecer, mediante pruebas de funcionamiento respiratorio (PFR), si existen alteraciones en la función respiratoria después de haber presentado una HP.
MétodosSe incluyó a pacientes con LES o con vasculitis primaria que presentaron HP. En el momento de la HP, se determinó actividad con SLEDAI para los pacientes con LES, «five factor store» (FFS) para poliangitis microscópica (PAM) y «Birmingham Vasculitis Activity Store» (BVAS) para granulomatosis con poliangitis (GP) (Wegener). Se determinaron el número de eventos de HP, el tratamiento utilizado y el requerimiento de asistencia mecánica ventilatoria (AMV) para determinar su probable asociación con las alteraciones de la función respiratoria medidas por pletismografía y/o espirometría.
ResultadosSe incluyó a 10 pacientes, 7 con LES y 3 con vasculitis primaria (2 con PAM y uno con GP (Wegener). La media ± desviación estándar de SLEDAI fue de 20,4 ± 7,5, la de FFS 2 y la de BVAS 36. Un paciente presentó 2 episodios de HP y otro 5. El tratamiento fue metilprednisolona (MPD) en 3 pacientes, MPD más ciclofosfamida (CFM) en 6 pacientes y MPD, CFM, inmunoglobulina por vía intravenosa y plasmaféresis en un paciente. Cinco pacientes requirieron AMV. Se encontró disfunción pulmonar en 8 pacientes; 3 tuvieron patrón obstructivo y 5 patrón restrictivo; 2 tuvieron PFR normales. No se encontró asociación significativa entre las variables y las alteraciones de la función respiratoria.
ConclusiónLa HP causa alteraciones de la función respiratoria en un alto porcentaje de pacientes y es probable que se requiera tratamiento inmunosupresor a largo plazo una vez resuelto el episodio agudo.
Pulmonary hemorrhage (PH) occurs in 2-5% of SLE patients, and is associated with a high mortality rate (79-90%). Diagnostic criteria for this complication include: 1) Pulmonary infiltrates, with at least ¾ of lung tissue involved in a chest x ray, 2) Acute respiratory failure, 3) A decrease of 3g/dL or more in hemoglobin levels. PH might lead to organized pneumonia, collagen deposition, and pulmonary fibrosis which in time might cause changes in pulmonary function tests with either restrictive or obstructive patterns.
AimTo evaluate the existence of abnormalities in pulmonary function tests after a PH episode.
MethodsWe included patients with SLE and primary vasculitis that developed PH. During the acute episode, we measured SLEDAI in SLE patients, five factor score in microscopic polyangiitis (MPA) and Birmingham Vasculitis Activity Store (BVAS) in granulomatosis with polyangiitis (GPA) (Wegener). We determined the number of PH events, treatment, and ventilator assistance requirements and correlated its association with abnormal pulmonary function tests.
ResultsWe included 10 patients, 7 with SLE, 2 with MPA and 1 with GPA (Wegener). The mean activity measures were: SLEDAI 20.4 ± 7.5, FFS 2, and BVAS 36. Treatment consisted in methylprednisolone (MPD) in 3 patients, MPD plus cyclophosphamide (CY) in 6 patients, and MPD, CY, IV immunoglobulin, and plasmapheresis in one patient. Five patients required ventilatory support. We found abnormalities in pulmonary function tests in 8 patients, three had an obstructive pattern and five a restrictive pattern; 2 patients did not show any change. We did not find a significant association with any of the studied variables.
ConclusionPH might cause abnormalities in pulmonary function tests and prolonged immunosuppressive treatment could be required.
La hemorragia pulmonar (HP) o hemorragia alveolar difusa es un síndrome clínico-patológico que pone en riesgo la vida; se puede presentar como episodio único o recurrente y puede conducir a neumonía organizada y depósito de colágeno en las vías aéreas pequeñas con el desarrollo de fibrosis pulmonar1,2.
Existen diversas causas de HP y la mayoría de ellas comparten la misma fisiopatogenia, dentro de la que destaca el daño a la microcirculación alveolar con hemorragia local3. Histopatológicamente, se presenta como capilaritis pulmonar, la cual se caracteriza por infiltración de neutrófilos en los vasos de pequeño calibre, eritrocitos intersticiales, depósito de hemosiderina y oclusión capilar septal interalveolar4; si bien esta capilaritis no es patognomónica, usualmente señala la presencia de una vasculitis sistémica subyacente5. En pacientes con enfermedades reumáticas, la HP se puede presentar como manifestación primaria de actividad de la enfermedad; las afecciones a los que se asocia con mayor frecuencia son el lupus eritematoso sistémico (LES) y las vasculitis sistémicas primarias6.La HP ocurre en el LES en el 2 al 5% de los casos y representa el 3,7% de las admisiones hospitalarias debido a actividad de LES, con una mortalidad del 70 al 90%7–9. En 1985, Abud-Mendoza et al.10 publicaron los criterios para diagnosticar HP: a) infiltrados alveolares densos en 3 cuartas partes o más de los campos pulmonares en la radiografía de tórax; b) insuficiencia respiratoria de inicio agudo, y c) descenso de la hemoglobina > 3g/dl; lo anterior se confirmó en un estudio de Barile et al.11, en el que se incluyó a 34 pacientes con HP secundaria a LES, que presentaron como manifestaciones más frecuentes: descenso de la hemoglobina (91,17%), insuficiencia respiratoria (100%), hemoptisis (58,82%), infiltrados radiológicos (100%) e hipoxemia (82,35%), destacando como dato importante que 14 de los pacientes no presentaron hemoptisis (41%). En los pacientes que no tienen la tríada clásica para diagnosticar HP, las imágenes de tomografía computarizada (TC) pueden confirmar el diagnóstico en un porcentaje elevado. En un estudio de Cortese et al., se revisaron radiografías de 20 pacientes con HP y se compararon con la TC; se encontró que esta última es superior a la radiografía de tórax convencional para detectar opacidades en vidrio deslustrado. Se destacó la mayor utilidad de este método diagnóstico y se sugirió su realización en casos de sospecha de HP con radiografía de tórax normal o sin la tríada clásica de la HP12-14.
Otro estudio valioso para el diagnóstico de HP es la broncoscopia con lavado broncoalveolar, la cual permite confirmar la HP, además de que es muy útil para buscar el origen de la hemorragia15,16. Este estudio se puede realizar incluso en pacientes con apoyo mecánico ventilatorio (AMV), el cual frecuentemente se utiliza en los pacientes con insuficiencia respiratoria secundaria a HP como medida de soporte vital. El AMV incrementa la supervivencia de estos pacientes, aunque puede dejar como secuela disfunción pulmonar secundaria a áreas de cicatrización, de gravedad variable, las cuales se pueden resolver completamente o no durante su evolución.
En cuanto al tratamiento de la HP, no hay un consenso establecido. Se han dado diferentes regímenes de tratamiento; el más utilizado incluye pulsos de metilprednisolona, 1g/día (requiriéndose en algunos casos hasta 5 días), y ciclofosfamida, con resultados variables. La plasmaféresis es controversial; sin embargo, ha demostrado ser útil en pacientes con vasculitis asociadas con anticuerpos anticitoplasma de neutrófilo y en pacientes con LES que no responden a la terapia convencional con glucocorticoides17,18.
La HP puede ocasionar fibrosis intersticial y esto puede repercutir sobre la función pulmonar, con cambios restrictivos u obstructivos, provocando daño parenquimatoso y de las vías aéreas pequeñas, lo que ocasiona bronquiolitis y enfisema19,20. Con los antecedentes previos, se buscó establecer las alteraciones en la función respiratoria después de la HP, en pacientes con LES y vasculitis primaria, mediante pletismografía, ya que esta última permite evaluar el grado y el tipo de disfunción del sistema respiratorio a través de la medición de la capacidad vital forzada (FVC), volumen espiratorio forzado en el primer segundo (FEV1) y relación FEV1/FVC o índice de Tiffeneau.
Los objetivos de este estudio fueron establecer, mediante pletismografía o espirometría, la prevalencia de las alteraciones de la función respiratoria y determinar los factores asociados a esta disfunción en pacientes con LES y vasculitis sistémica primaria, después de una HP.
Pacientes y métodosSe incluyó a pacientes del servicio de reumatología con diagnóstico de LES o vasculitis sistémica primaria del Hospital de Especialidades del Centro Médico Nacional Siglo XXI, los cuales tuvieron HP demostrada por la tríada que consta de insuficiencia respiratoria aguda, descenso de la cifra de hemoglobina > 3g/dl e infiltrados alveolares difusos en 3 cuartas partes de los campos pulmonares en la radiografía de tórax, o en los que se confirmó HP con tomografía de alta resolución o broncoscopia.
Se incluyó a pacientes mayores de 18 años, que cumplieran los criterios de clasificación del Colegio Estadounidense de Reumatología para LES21 o los criterios de Chapel Hill para vasculitis sistémica primaria22,23, y en quienes fue posible la medición de la función pulmonar con pletismografía o espirometría para determinar el volumen residual, la capacidad pulmonar total (TLC), la capacidad funcional residual, la FVC, el FEV1 y la relación FEV1/FVC o índice de Tiffeneau, además del grado de obstrucción y restricción pulmonar.
Se midieron los índices SLEDAI y SLICC en pacientes con LES y la escalas de actividad de las vasculitis, «five factor store» (FFS) en poliangitis microscópica (PAM) y BVAS en granulomatosis con poliangitis (GP) (Wegener), para establecer el grado de actividad en el momento de la HP; se determinaron también el número de eventos de HP y el tipo de tratamiento utilizado, así como el requerimiento de AMV, en búsqueda de factores asociados a la disfunción respiratoria crónica.
Diseño del estudioRetrospectivo, transversal, analítico.
Análisis estadísticoSe realizaron estadística descriptiva y análisis bivariado con prueba de la chi al cuadrado, prueba exacta de Fisher y OR (razón de momios) con intervalos de confianza del 95% (IC del 95%); se consideró estadísticamente significativo una p < 0,05. Se utilizó el programa SPSS 15.0.
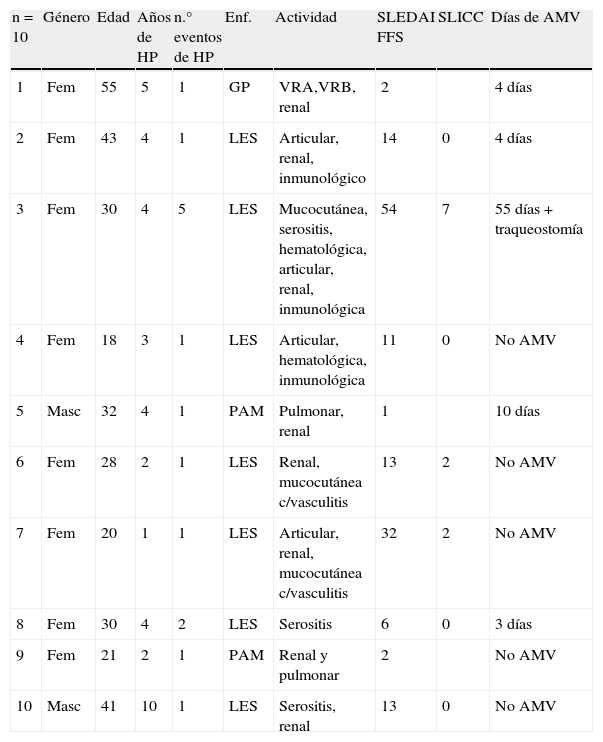
ResultadosSe efectuó un análisis retrospectivo de pacientes con LES y vasculitis sistémica, de septiembre de 1998 a noviembre del 2007; se identificó a 11 pacientes que presentaron HP y sobrevivieron, 10 de los 11 pacientes fueron contactados en la consulta externa para la realización de pruebas de funcionamiento pulmonar, previa firma de consentimiento informado. Uno de los pacientes no fue localizado. Se incluyó a un total de 10 pacientes que habían tenido HP dentro de las fechas señaladas, de los cuales 3 tuvieron vasculitis sistémica: uno con GP (Wegener) con anticuerpos anticitoplasma de neutrófilo citoplásmicos positivos y 2 con PAM con anticuerpos anticitoplasma de neutrófilo perinucleares positivos; el resto (7 pacientes) tenía diagnóstico de LES. La edad promedio de los pacientes en el momento del estudio fue de 30 años (con rango de 18-43 años) para los pacientes con LES y de 35 años (rango de 21-55 años) para los pacientes con vasculitis sistémica. Las características basales de los pacientes se muestran en la tabla 1.
Características basales de los pacientes
| n = 10 | Género | Edad | Años de HP | n.° eventos de HP | Enf. | Actividad | SLEDAI FFS | SLICC | Días de AMV |
| 1 | Fem | 55 | 5 | 1 | GP | VRA,VRB, renal | 2 | 4 días | |
| 2 | Fem | 43 | 4 | 1 | LES | Articular, renal, inmunológico | 14 | 0 | 4 días |
| 3 | Fem | 30 | 4 | 5 | LES | Mucocutánea, serositis, hematológica, articular, renal, inmunológica | 54 | 7 | 55 días + traqueostomía |
| 4 | Fem | 18 | 3 | 1 | LES | Articular, hematológica, inmunológica | 11 | 0 | No AMV |
| 5 | Masc | 32 | 4 | 1 | PAM | Pulmonar, renal | 1 | 10 días | |
| 6 | Fem | 28 | 2 | 1 | LES | Renal, mucocutánea c/vasculitis | 13 | 2 | No AMV |
| 7 | Fem | 20 | 1 | 1 | LES | Articular, renal, mucocutánea c/vasculitis | 32 | 2 | No AMV |
| 8 | Fem | 30 | 4 | 2 | LES | Serositis | 6 | 0 | 3 días |
| 9 | Fem | 21 | 2 | 1 | PAM | Renal y pulmonar | 2 | No AMV | |
| 10 | Masc | 41 | 10 | 1 | LES | Serositis, renal | 13 | 0 | No AMV |
AMV: apoyo mecánico ventilatorio; SNP: sistema nervioso periférico; VRA: vías respiratorias altas; VRB: vías respiratorias bajas.
De los 10 pacientes, 8 no tenían establecido el diagnóstico de LES o de vasculitis sistémica en el momento de la HP y solo presentaron síntomas constitucionales los días previos a la misma. Un paciente presentó 2 eventos de HP, con un intervalo entre los 2 eventos de 25 días; el primer evento de HP se trató con 1g de metilprednisolona cada 24 h por 3 dosis y en el segundo evento necesitó AMV por 3 días, y nuevamente 3 pulsos de metilprednisolona de 1g cada 24 h. Otro paciente presentó 5 eventos de HP en el periodo comprendido entre el 6 de abril y el 12 de mayo del 2004; en el primer evento recibió 7 pulsos de metilprednisolona de 1g cada uno y no precisó AMV. En el segundo evento (15 días posteriores al primero), requirió AMV; los otros 3 eventos de HP los presentó intubado, siendo manejado en terapia intensiva, donde durante su evolución presentó crisis convulsivas tonicoclónicas generalizadas y se documentó un infarto occipital bilateral por TC de cráneo. Este paciente recibió en forma consecutiva: metilprednisolona, ciclofosfamida, inmunoglobulina IV y plasmaféresis, por actividad grave de LES; con ello se logró controlar la hemorragia. Los 8 pacientes restantes solo presentaron un evento de HP. La puntuación media del SLEDAI fue de 20,8 en los pacientes con LES; en los pacientes con PAM, el FFS fue de 2 y el paciente con GP (Wegener) tuvo un BVAS de 36 puntos (todos los índices medidos en el momento de la HP). De los 7 pacientes con LES, solo 3 de ellos presentaron puntuación de SLICC mayor de un punto en el momento del estudio, 2 de ellos con puntuación de 2 y uno con puntuación de 7 (paciente 3), con una media de 2,25 (tabla 2).
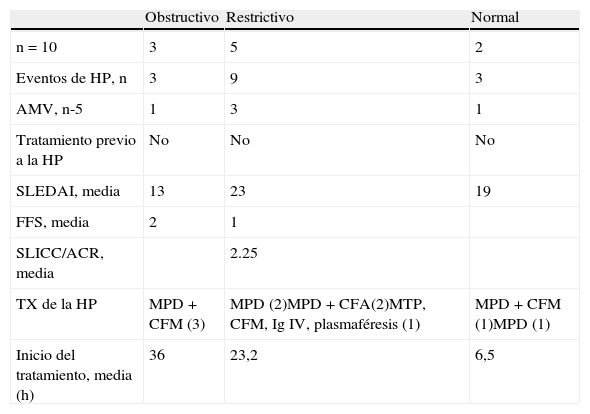
Patrones de mecánica respiratoria
| Obstructivo | Restrictivo | Normal | |
| n = 10 | 3 | 5 | 2 |
| Eventos de HP, n | 3 | 9 | 3 |
| AMV, n-5 | 1 | 3 | 1 |
| Tratamiento previo a la HP | No | No | No |
| SLEDAI, media | 13 | 23 | 19 |
| FFS, media | 2 | 1 | |
| SLICC/ACR, media | 2.25 | ||
| TX de la HP | MPD + CFM (3) | MPD (2)MPD + CFA(2)MTP, CFM, Ig IV, plasmaféresis (1) | MPD + CFM (1)MPD (1) |
| Inicio del tratamiento, media (h) | 36 | 23,2 | 6,5 |
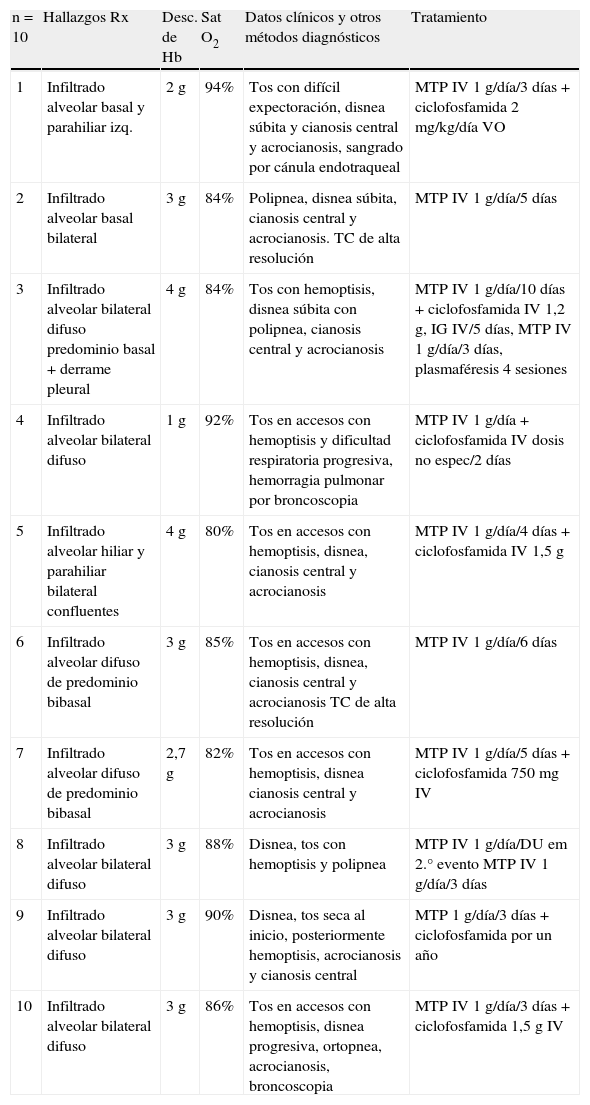
Se observó que 8 pacientes iniciaron con síndrome de pulmón-riñón, 5 de ellos con diagnóstico de LES y los 3 con vasculitis sistémica (tabla 1). De los 10 pacientes, 3 recibieron como único tratamiento en el episodio agudo metilprednisolona (3 con LES), un paciente recibió metilprednisolona, ciclofosfamida IV, inmunoglobulina IV y plasmaféresis, y los 6 restantes recibieron metilprednisolona y ciclofosfamida (tabla 3). Todos los pacientes recibieron antibiótico y solo en 2 se documentó infección agregada, un paciente tuvo Candida albicans (en vías urinarias) y Streptococcus spp. (pulmonar) y un paciente neumonía asociada a intubación prolongada, en el que se aislaron Calcoaceticus baumanili y Acinetobacter.
Características en el momento de la hemorragia y tratamiento administrado
| n = 10 | Hallazgos Rx | Desc. de Hb | Sat O2 | Datos clínicos y otros métodos diagnósticos | Tratamiento |
| 1 | Infiltrado alveolar basal y parahiliar izq. | 2g | 94% | Tos con difícil expectoración, disnea súbita y cianosis central y acrocianosis, sangrado por cánula endotraqueal | MTP IV 1 g/día/3 días + ciclofosfamida 2 mg/kg/día VO |
| 2 | Infiltrado alveolar basal bilateral | 3g | 84% | Polipnea, disnea súbita, cianosis central y acrocianosis. TC de alta resolución | MTP IV 1 g/día/5 días |
| 3 | Infiltrado alveolar bilateral difuso predominio basal + derrame pleural | 4g | 84% | Tos con hemoptisis, disnea súbita con polipnea, cianosis central y acrocianosis | MTP IV 1 g/día/10 días + ciclofosfamida IV 1,2g, IG IV/5 días, MTP IV 1 g/día/3 días, plasmaféresis 4 sesiones |
| 4 | Infiltrado alveolar bilateral difuso | 1g | 92% | Tos en accesos con hemoptisis y dificultad respiratoria progresiva, hemorragia pulmonar por broncoscopia | MTP IV 1 g/día + ciclofosfamida IV dosis no espec/2 días |
| 5 | Infiltrado alveolar hiliar y parahiliar bilateral confluentes | 4g | 80% | Tos en accesos con hemoptisis, disnea, cianosis central y acrocianosis | MTP IV 1 g/día/4 días + ciclofosfamida IV 1,5 g |
| 6 | Infiltrado alveolar difuso de predominio bibasal | 3g | 85% | Tos en accesos con hemoptisis, disnea, cianosis central y acrocianosis TC de alta resolución | MTP IV 1 g/día/6 días |
| 7 | Infiltrado alveolar difuso de predominio bibasal | 2,7g | 82% | Tos en accesos con hemoptisis, disnea cianosis central y acrocianosis | MTP IV 1 g/día/5 días + ciclofosfamida 750mg IV |
| 8 | Infiltrado alveolar bilateral difuso | 3g | 88% | Disnea, tos con hemoptisis y polipnea | MTP IV 1 g/día/DU em 2.° evento MTP IV 1 g/día/3 días |
| 9 | Infiltrado alveolar bilateral difuso | 3g | 90% | Disnea, tos seca al inicio, posteriormente hemoptisis, acrocianosis y cianosis central | MTP 1 g/día/3 días + ciclofosfamida por un año |
| 10 | Infiltrado alveolar bilateral difuso | 3g | 86% | Tos en accesos con hemoptisis, disnea progresiva, ortopnea, acrocianosis, broncoscopia | MTP IV 1 g/día/3 días + ciclofosfamida 1,5g IV |
Hb: hemoglobina; Rx: radiográficos; Sat O2: saturación de oxígeno.
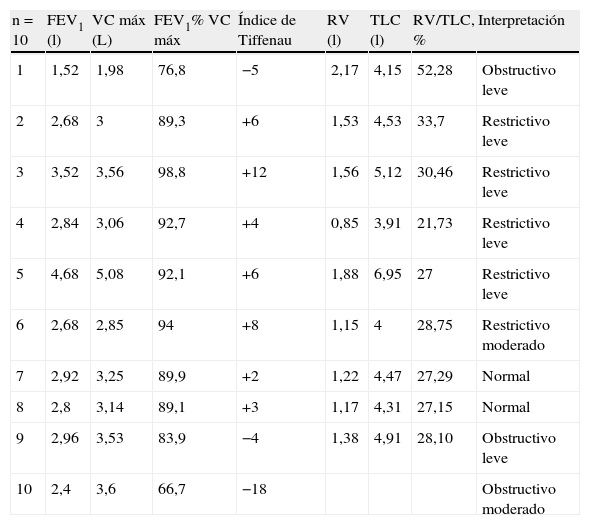
En 7 de los 10 pacientes se demostró la tríada para el diagnóstico de HP; en 3 pacientes el descenso de la hemoglobina fue menor a 3g. Las características en el momento de la hemorragia y el tratamiento administrado se muestran en la tabla 3. A los 10 pacientes se le realizaron pruebas de funcionamiento respiratorio (PFR), a 9 pletismografía y a uno espirometría. Los resultados obtenidos se muestran en la tabla 4. En las PFR se observó patrón de mecánica respiratoria obstructiva en 3 pacientes, restrictiva en 5 pacientes y patrón normal en los 2 restantes. De acuerdo con el índice de Tiffeneau, 8 de los pacientes presentaron disfunción respiratoria crónica, 3 de los cuales presentaron patrón obstructivo, 2 leve y uno moderado. De los 5 pacientes que presentaron patrón restrictivo, en 4 fue leve y en uno moderado; únicamente un paciente con patrón obstructivo presentó hipoxemia leve (tabla 2). Se observó que los 2 pacientes que presentaron patrón de mecánica respiratoria normal fueron los que recibieron tratamiento en forma más precoz; sin embargo, al realizar el análisis bivariado no se observó diferencia estadísticamente significativa. Lo mismo sucedió con el tiempo de evolución de la HP, ya que de acuerdo con los resultados, en el paciente con mayor tiempo de evolución se observó mayor disfunción respiratoria al compararse con el resto de los pacientes, lo cual no se corroboró en el análisis divariado. Al analizar el resto de las variables con la prueba de la chi al cuadrada y la prueba exacta de Fisher, tampoco se observó diferencia estadísticamente significativa (tabla 5).
Pruebas de función respiratoria: capacidades, volúmenes e índice de Tiffenau
| n = 10 | FEV1 (l) | VC máx (L) | FEV1% VC máx | Índice de Tiffenau | RV (l) | TLC (l) | RV/TLC, % | Interpretación |
| 1 | 1,52 | 1,98 | 76,8 | −5 | 2,17 | 4,15 | 52,28 | Obstructivo leve |
| 2 | 2,68 | 3 | 89,3 | +6 | 1,53 | 4,53 | 33,7 | Restrictivo leve |
| 3 | 3,52 | 3,56 | 98,8 | +12 | 1,56 | 5,12 | 30,46 | Restrictivo leve |
| 4 | 2,84 | 3,06 | 92,7 | +4 | 0,85 | 3,91 | 21,73 | Restrictivo leve |
| 5 | 4,68 | 5,08 | 92,1 | +6 | 1,88 | 6,95 | 27 | Restrictivo leve |
| 6 | 2,68 | 2,85 | 94 | +8 | 1,15 | 4 | 28,75 | Restrictivo moderado |
| 7 | 2,92 | 3,25 | 89,9 | +2 | 1,22 | 4,47 | 27,29 | Normal |
| 8 | 2,8 | 3,14 | 89,1 | +3 | 1,17 | 4,31 | 27,15 | Normal |
| 9 | 2,96 | 3,53 | 83,9 | −4 | 1,38 | 4,91 | 28,10 | Obstructivo leve |
| 10 | 2,4 | 3,6 | 66,7 | −18 | Obstructivo moderado |
FEV1: volumen espiratorio forzado en el primer segundo; FVC: capacidad vital forzada; RV: volumen de reserva; TLC: capacidad pulmonar total; VC máx: capacidad vital máxima.
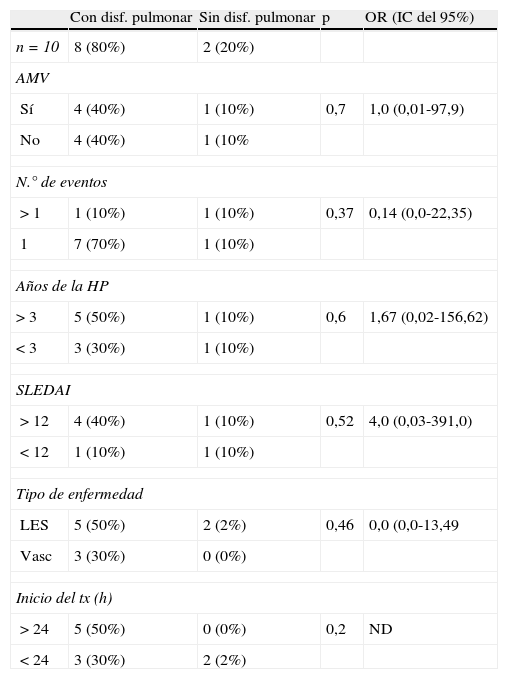
Asociación entre variables incluidas y hemorragia pulmonar
| Con disf. pulmonar | Sin disf. pulmonar | p | OR (IC del 95%) | |
| n = 10 | 8 (80%) | 2 (20%) | ||
| AMV | ||||
| Sí | 4 (40%) | 1 (10%) | 0,7 | 1,0 (0,01-97,9) |
| No | 4 (40%) | 1 (10% | ||
| N.° de eventos | ||||
| > 1 | 1 (10%) | 1 (10%) | 0,37 | 0,14 (0,0-22,35) |
| 1 | 7 (70%) | 1 (10%) | ||
| Años de la HP | ||||
| > 3 | 5 (50%) | 1 (10%) | 0,6 | 1,67 (0,02-156,62) |
| < 3 | 3 (30%) | 1 (10%) | ||
| SLEDAI | ||||
| > 12 | 4 (40%) | 1 (10%) | 0,52 | 4,0 (0,03-391,0) |
| < 12 | 1 (10%) | 1 (10%) | ||
| Tipo de enfermedad | ||||
| LES | 5 (50%) | 2 (2%) | 0,46 | 0,0 (0,0-13,49 |
| Vasc | 3 (30%) | 0 (0%) | ||
| Inicio del tx (h) | ||||
| > 24 | 5 (50%) | 0 (0%) | 0,2 | ND |
| < 24 | 3 (30%) | 2 (2%) | ||
La HP es una complicación poco frecuente de las enfermedades autoinmunes, pero se asocia a una elevada morbimortalidad. Las series de HP publicadas en la literatura son descriptivas e incluyen un pequeño número de pacientes; una de las más grandes, de Barile et al., incluyó a 34 pacientes con HP y LES11. La HP se presenta clínicamente con un patrón muy heterogéneo, desde una forma crónica hasta un evento catastrófico agudo de hemoptisis masiva. Dentro de las manifestaciones clínicas de la HP se encuentran el descenso de la hemoglobina, la insuficiencia respiratoria aguda, los infiltrados radiológicos y la hemoptisis, aunque esta última puede estar ausente, como lo demostraron Abud-Mendoza et al.10 en su serie de 12 casos publicada en 1985, hallazgo corroborado por Barile et al. en 1997, en una serie en la que se demostró ausencia de hemoptisis en 41% de los casos11. Estos estudios concuerdan en que para hacer el diagnóstico de HP es necesaria la tríada integrada por insuficiencia respiratoria aguda, descenso de la hemoglobina >3g/dl e infiltrados radiológicos en al menos 3 cuartas partes de campos pulmonares, aunque en etapas precoces el descenso de la hemoglobina puede ser menor y los infiltrados abarcar menos de 3 cuartas partes del parénquima pulmonar. En estos casos, el diagnóstico se establece por broncoscopia y/o TC de alta resolución. En nuestro estudio, 7 de los 10 pacientes presentaron la tríada, pero en 3 de ellos el descenso de hemoglobina fue menor de 3g. En la mayoría de nuestros pacientes con HP secundaria a LES, esta fue la manifestación inicial de la enfermedad; esto se ha reportado entre el 12 y el 20% de los casos. En el caso de la GP (Wegener), la HP aparece en el 42% de los casos y en la PAM en el 29% de los casos24.
En el presente estudio encontramos que 5 de los pacientes con LES y los 3 pacientes con vasculitis sistémica no tenían establecido el diagnóstico y solo habían presentado síntomas constitucionales previo al evento de HP. Solo 2 de los pacientes con LES tenían el diagnóstico establecido de la enfermedad 2 meses antes de la HP y por decisión propia no tomaban medicamento inmunosupresor ni glucocorticoide.
Se ha descrito en la literatura que del 75 al 93% de los casos de HP en lupus se presenta como un síndrome pulmón-riñón10,11, lo cual concuerda con lo encontrado en nuestro estudio. La fisiopatogenia de la HP no es un proceso completamente entendido ni uniforme para todas las entidades agrupadas bajo esta nomenclatura. Aunque es frecuente encontrar capilaritis asociada a la HP, esta asociación no se presenta en el 100% de los casos. La presencia de capilaritis es un hallazgo patológico que podría orientar hacia un desorden vasculítico sistémico16 como LES, GP o PAM, entre otros; en el caso de las enfermedades en las que se encuentra histopatológicamente capilaritis, parece que el depósito de complejos inmunes desempeña un papel muy importante en el desarrollo de estas afecciones, con la activación posterior del complemento, así como liberación de aminas vasoactivas y factores quimiotácticos.
La presencia de complejos inmunes circulantes o depositados en las membranas basales favorece el desarrollo de inflamación vascular25, aunque su ausencia no implica que no participen en la patogénesis de la HP, ya que pueden ser removidos tanto de la circulación como de los tejidos por los granulocitos pocas horas después de su generación26.
Los anticuerpos anticitoplasma de neutrófilo se consideran anticuerpos que participan en la generación de vasculitis sistémicas como la GP y la PAM, ya que son importantes en la activación de neutrófilos y monocitos circulantes, y tienen reacción cruzada con antígenos presentes en la superficie endotelial. En forma general, la activación de neutrófilos desencadena liberación de radicales libres de oxígeno y enzimas lisosomales, lo que causa lesión endotelial.
Los episodios recurrentes de HP pueden conducir a fibrosis intersticial y cambios restrictivos en el patrón de la mecánica ventilatoria, lo que se demuestra con las pruebas de funcionamiento pulmonar (pletismografía o espirometría) con disminución de la TLC y de la FVC, con preservación de la relación FEV1/FVC; también se pueden encontrar cambios obstructivos, demostrados por un incremento de la TLC y una disminución de la relación FEV1/CVF. Como ya se mencionó, en 8 de nuestros pacientes se encontraron alteraciones en la función respiratoria, 3 tuvieron patrón obstructivo y 5 patrón restrictivo.
En este estudio no se encontró asociación entre la actividad de la enfermedad (LES o vasculitis), el uso de AMV, el tiempo de inicio del tratamiento, los años transcurridos de la HP ni el número de eventos de HP con el desarrollo de disfunción respiratoria crónica, lo que puede deberse al tamaño de la muestra, que es tan solo de 10 pacientes. Esto constituye una debilidad del estudio.
Podemos concluir que encontramos disfunción respiratoria crónica en un alto porcentaje de pacientes, en los que probablemente el mecanismo de producción sea inflamación aguda con patrón de citocinas Th1 y, posteriormente, daño crónico con patrón de citocinas Th2. También es probable que se requiera tratamiento inmunosupresor a largo plazo una vez que se resuelva el episodio agudo de HP. Este es el único estudio que ha medido las alteraciones en la función pulmonar asociada a HP en pacientes con LES o vasculitis sistémica primaria. Se requieren estudios prospectivos controlados con un mayor número de pacientes para corroborar estos hallazgos.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes y que todos los pacientes incluidos en el estudio han recibido información suficiente y han dado su consentimiento informado por escrito para participar en dicho estudio.
Derecho a la privacidad y consentimiento informadoLos autores han obtenido el consentimiento informado de los pacientes y/o sujetos referidos en el artículo. Este documento obra en poder del autor de correspondencia.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.