Revisar la evidencia clínica sobre abatacept subcutáneo (sc) y emitir recomendaciones con objeto de aclarar su uso en reumatología.
MétodoUn panel de expertos reumatólogos resumió de forma objetiva las pruebas existentes sobre el mecanismo de acción, el modo de uso, la eficacia y la seguridad de abatacept sc y desarrolló un documento sobre el uso de este fármaco en situaciones concretas, previa revisión de la bibliografía.
ResultadosEl abatacept sc sustenta su eficacia y seguridad en 7 ensayos clínicos, 3 doble ciego, 3 abiertos y uno mixto, en los que se compara la administración sc frente a la iv de abatacept, se estudia el posible impacto sobre la inmunogenicidad, el efecto de sustituir la vía iv por la sc en pacientes que previamente venían recibiendo abatacept iv, la monoterapia y la no inferioridad frente a adalimumab. No se han encontrado diferencias significativas frente a abatacept iv ni en cuanto a la eficacia ni en cuanto a la seguridad. El desarrollo de abatacept sc ha permitido un estudio complementario al del iv, con lo que el perfil del mismo queda más definido.
ConclusionesSe trata de un documento práctico como complemento a la información en ficha técnica. En resumen, el abatacept sc se presenta como un fármaco eficaz y seguro y, por lo tanto, como una alternativa más para utilizar entre los múltiples tratamientos con que cuenta hoy en día el reumatólogo. Además, cuenta con la ventaja de ser el único agente biológico que se puede administrar por vía iv y sc, lo cual puede facilitar su uso en determinados pacientes.
To review the clinical evidence on subcutaneous (sc) abatacept and to formulate recommendations in order to clear up points related to its use in rheumatology.
MethodAn expert panel of rheumatologists objectively summarized the evidence on the mechanism of action, practicality, effectiveness, and safety of abatacept sc and formulated recommendations after a literature review.
ResultsThe efficacy and safety of abatacept sc was studied in 7 clinical trials, 3 double-blind, 3 open, and one mixed, with the following endpoints: comparison against abatacept iv, impact on immunogenicity, effect of replacing iv by sc, abatacept sc in monotherapy, and non-inferiority to adalimumab. No significant differences were found between sc and iv abatacept on efficacy or safety. The development of sc abatacept has allowed a complementary study to the iv, formulation, thus making the abatacept profile better defined.
ConclusionsThis is a practical document to supplement the summary of product characteristics. In summary, abatacept sc is presented as an effective and safe drug and, therefore, as an alternative for use within the broad armamentarium the rheumatologist has to treat RA. It also has the advantage of being the only biological agent that can be administered iv and sc which can facilitate its use in certain patients.
La eficacia y la seguridad de un fármaco biológico son los elementos clave a la hora de su elección para el tratamiento de la artritis reumatoide (AR); sin embargo, otros factores desempeñan también un papel importante, entre ellos la vía de administración. Muchos pacientes prefieren la autonomía que aporta la posibilidad de autoinyectarse por vía subcutánea (sc) frente a la necesidad de acudir a un hospital de día o unidad de infusión intravenosa (iv). También un número importante de médicos prefieren la vía sc, a igualdad de eficacia y seguridad, debido, entre otros factores, a que ofrece menos complejidades organizativas. De ahí el interés por desarrollar formulaciones administrables por vía sc para fármacos disponibles para uso exclusivo iv.
El cambio de la vía iv por la sc en un fármaco de naturaleza proteica no es en absoluto un tema de simple sustitución. La administración sc plantea diferencias significativas respecto a la vía iv, tanto desde el punto de vista de eficacia como de seguridad, que obligan a realizar un estudio y desarrollo independientes. Algunos aspectos tienen una relevancia especial. El primero es la posología; la vía sc conlleva diferencias farmacocinéticas que se traducen en pautas distintas de administración, con dosificaciones e intervalos diferentes de los de la vía iv. Otro aspecto clave es el de la inmunogenicidad. La administración parenteral de fármacos de naturaleza proteica se asocia, al menos teóricamente, a la posibilidad de producción de anticuerpos frente al fármaco (AAF). La vía de administración y la dosis son factores que pueden condicionar este fenómeno, debido, entre otros aspectos, a diferencias en la presentación de antígeno1; además, la composición diferente de los excipientes para ambas formulaciones puede contribuir también a diferencias de inmunogenicidad. De ahí la enorme importancia de analizar la inmunogenicidad dentro del proceso de desarrollo de un fármaco biológico para administración sc. Además, hay factores, como la interrupción temporal y la posterior reintroducción, el cambio en un mismo paciente de la vía iv a la sc o el uso del fármaco en monoterapia o asociado a fármacos modificadores de la enfermedad (FAME), que pueden modificar las propiedades inmunogénicas de un medicamento proteico2. Otro aspecto de seguridad que merece un análisis especial es el de la posible aparición de reacciones en el sitio de la inyección sc.
Abatacept es un fármaco biológico de naturaleza proteica, modulador selectivo de la coestimulación de linfocitos T, aprobado para el tratamiento de la AR. Su uso por vía iv ha demostrado eficacia, con un perfil de seguridad adecuado en diferentes poblaciones de pacientes con esta enfermedad, incluyendo pacientes que anteriormente nunca habían recibido metotrexato (MTX), pacientes con respuesta inadecuada a fármacos modificadores de la enfermedad (FAME) sintéticos, así como a biológicos anti-TNF3-5.
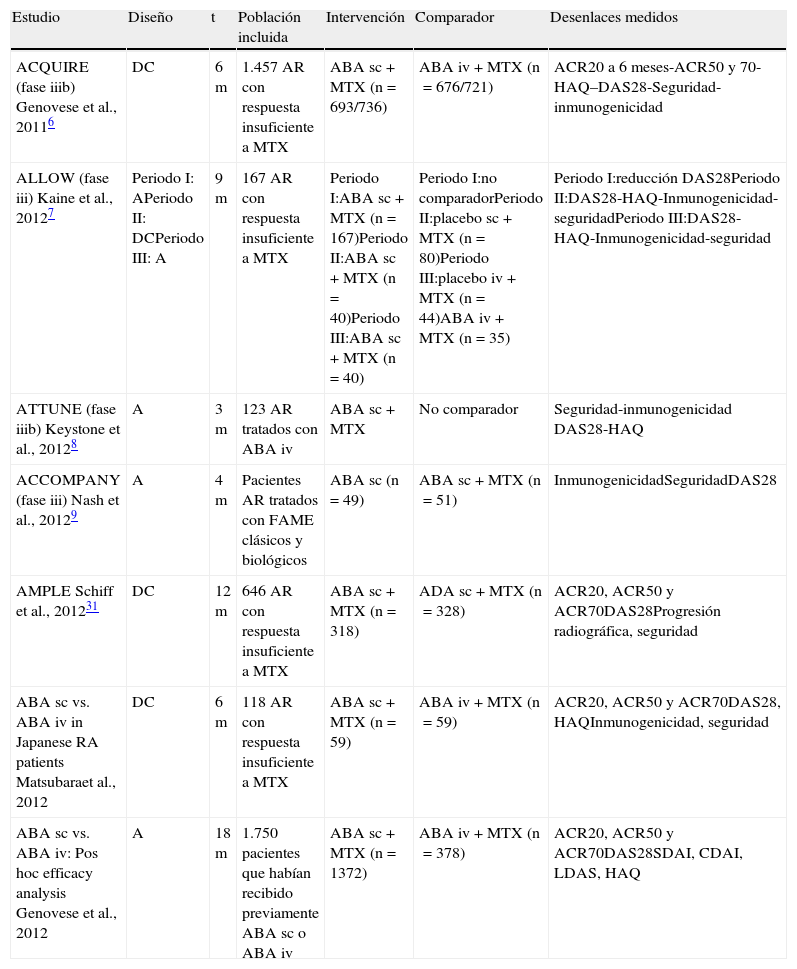
Además de la formulación iv, en los últimos años se ha desarrollado una nueva forma de abatacept para uso por vía sc. La tabla 1 refleja el resumen de los principales ensayos clínicos realizados. El estudio ACQUIRE es el ensayo principal, con un mayor número de pacientes, en el que se compara, desde el punto de vista de eficacia y seguridad, la administración sc frente a la iv de abatacept6. El estudio ALLOW analiza específicamente el posible impacto sobre la inmunogenicidad de la suspensión y la posterior reintroducción del fármaco7. En el ATTUNE se estudia el efecto de sustituir la vía iv por la sc en pacientes que previamente venían recibiendo abatacept iv8. En el ACCOMPANY, se investiga el efecto de la administración sc de abatacept en monoterapia frente a la combinación con MTX, fundamentalmente desde el punto de vista de su inmunogenicidad9. En el estudio AMPLE, se comparan la eficacia y la seguridad de 2 fármacos biológicos: abatacept y adalimumab, en combinación con MTX10.
Descripción de los ensayos clínicos de abatacept sc
| Estudio | Diseño | t | Población incluida | Intervención | Comparador | Desenlaces medidos |
| ACQUIRE (fase iiib) Genovese et al., 20116 | DC | 6m | 1.457 AR con respuesta insuficiente a MTX | ABA sc+MTX (n=693/736) | ABA iv+MTX (n=676/721) | ACR20 a 6 meses-ACR50 y 70-HAQ–DAS28-Seguridad-inmunogenicidad |
| ALLOW (fase iii) Kaine et al., 20127 | Periodo I: APeriodo II: DCPeriodo III: A | 9m | 167 AR con respuesta insuficiente a MTX | Periodo I:ABA sc+MTX (n=167)Periodo II:ABA sc+MTX (n=40)Periodo III:ABA sc+MTX (n=40) | Periodo I:no comparadorPeriodo II:placebo sc+MTX (n=80)Periodo III:placebo iv+MTX (n=44)ABA iv+MTX (n=35) | Periodo I:reducción DAS28Periodo II:DAS28-HAQ-Inmunogenicidad-seguridadPeriodo III:DAS28-HAQ-Inmunogenicidad-seguridad |
| ATTUNE (fase iiib) Keystone et al., 20128 | A | 3m | 123 AR tratados con ABA iv | ABA sc+MTX | No comparador | Seguridad-inmunogenicidad DAS28-HAQ |
| ACCOMPANY (fase iii) Nash et al., 20129 | A | 4m | Pacientes AR tratados con FAME clásicos y biológicos | ABA sc (n=49) | ABA sc+MTX (n=51) | InmunogenicidadSeguridadDAS28 |
| AMPLE Schiff et al., 201231 | DC | 12m | 646 AR con respuesta insuficiente a MTX | ABA sc+MTX (n=318) | ADA sc+MTX (n=328) | ACR20, ACR50 y ACR70DAS28Progresión radiográfica, seguridad |
| ABA sc vs. ABA iv in Japanese RA patients Matsubaraet al., 2012 | DC | 6m | 118 AR con respuesta insuficiente a MTX | ABA sc+MTX (n=59) | ABA iv+MTX (n=59) | ACR20, ACR50 y ACR70DAS28, HAQInmunogenicidad, seguridad |
| ABA sc vs. ABA iv: Pos hoc efficacy analysis Genovese et al., 2012 | A | 18m | 1.750 pacientes que habían recibido previamente ABA sc o ABA iv | ABA sc+MTX (n=1372) | ABA iv+MTX (n=378) | ACR20, ACR50 y ACR70DAS28SDAI, CDAI, LDAS, HAQ |
A: abierto; AR: artritis reumatoide; ABA: abatacept; ADA: adalimumab; DC: doble ciego; MTX: metotrexato; PBO: placebo; m: meses.
Abatacept para uso sc se presenta en jeringas de cristal precargadas con 125mg de principio activo en 1ml de volumen. La fórmula para administración sc no contiene maltosa, a diferencia de la iv11. Estudios de fase i y ii han concluido que una dosis semanal sc de 125mg aporta niveles de abatacept terapéuticos12.
La disponibilidad de una nueva fórmula de abatacept para uso sc amplía las opciones para el tratamiento de la AR. El objetivo de este documento es el de revisar la evidencia clínica sobre abatacept sc y comentar las ventajas potenciales que su uso podría comportar.
MétodosEl documento se realizó a partir de una reunión de discusión en la que se debatió la evidencia disponible sobre abatacept sc y se tomaron decisiones acerca de los temas que eran más importantes para la práctica clínica. A continuación, cada panelista realizó una revisión del tema correspondiente, que le fue asignado basándose en búsquedas en Pubmed, congresos ACR y EULAR y la ficha técnica. El documento final fue consensuado por todos los panelistas. El nivel de evidencia se graduó con la escala de Oxford13.
ResultadosFarmacocinéticaDiversos estudios han demostrado que la concentración valle en estado de equilibrio de abatacept para proporcionar una inhibición óptima de las células T y obtener así una adecuada respuesta clínica es ≥ 10μg/mL14. Estas concentraciones se alcanzan con la dosis iv aprobada para abatacept y en más del 90% de los pacientes tratados con abatacept sc11. Para demostrar la eficacia y la seguridad de abatacept sc en comparación con la pauta clásica iv utilizada hasta el momento, se han llevado a cabo estudios tanto en animales15,16, como en humanos6,11,17,18. Con este fin, se diseñaron ensayos clínicos con y sin dosis de carga iv en los que se evaluó el impacto de dicha dosis en la eficacia clínica, el perfil farmacocinético y la inmunogenicidad del abatacept sc. En varios ensayos clínicos de abatacept sc (incluido el estudio fundamental, ACQUIRE) se incluye una dosis de carga iv de abatacept el día uno para alcanzar rápidamente concentraciones terapéuticas y después comparar si la eficacia de la administración sc es similar a la de la administración iv6,11,17,18. En estos estudios, se demuestra un perfil de eficacia y seguridad similar para las 2 vías de administración, y se demuestra cómo la gran mayoría de los pacientes que reciben abatacept sc alcanzan una concentración de abatacept estable en el valle ≥ 10μg/mL, con menor variación entre la concentración pico y valle que con la administración iv18.
Aunque con cierta reserva, debido al diseño diferente de los estudios (ALLOW y ACCOMPANY), se puede deducir que la eficacia clínica de abatacept sc, precedido o no de una dosis de carga iv, es similar a los 3 meses de iniciar el tratamiento, obteniéndose niveles terapéuticos de abatacept a las 2 semanas en la mayoría de aquellos pacientes (88%) en los que no se utilizó dosis de carga17,19. Por lo tanto, en aquellos pacientes en los que se vaya a iniciar abatacept sc no parece necesario administrar una dosis de carga. (Nivel de evidencia 2b).
En diversos estudios en los que se ha determinado el nivel de abatacept en suero, así como la presencia de anticuerpos antiabatacept por ELISA, se ha demostrado que el abatacept sc es bien tolerado y presenta un perfil de seguridad y de inmunogenicidad similar a abatacept iv6,9,11,20. De igual modo, se ha demostrado en voluntarios sanos que tanto la administración de abatacept iv como de abatacept sc produce una ocupación similar del receptor (75%) (información facilitada por Bristol-Myers Squibb).
El abatacept sc presenta una farmacocinética lineal y presenta menos variaciones en el valle que la administración iv12. La biodisponibilidad de la administración sc comparada con la administración iv es del 78,6%18. La media estimada para el aclaramiento sistémico (0,28mL/h/kg), volumen de distribución (0,11L/kg) y la semivida de eliminación (14,3 días) son comparables entre la administración sc y la administración iv. Al igual que por vía iv, el análisis de la farmacocinética de la forma sc muestra que el aclaramiento del fármaco aumenta con el incremento del peso. La edad y el sexo —corregido por peso corporal— no afectaron al aclaramiento. La medicación concomitante, como el MTX, corticoides y AINE, aparentemente no influye en el aclaramiento de abatacept12,21. (Nivel de evidencia 2b).
EficaciaEficacia a corto y largo plazo. (Nivel de evidencia 1b)El desarrollo clínico de abatacept sc se basa en un estudio fase iia de seguridad y búsqueda de dosis y 4 estudios fase iii (tabla 1).
El estudio ACQUIRE6 comparó la eficacia a las 24 semanas de abatacept 150mg sc semanal frente a la pauta tradicional iv. Se incluyó a 1.457 pacientes con AR activa pese al tratamiento con MTX. Los del grupo sc recibieron una dosis de carga iv el primer día. Se permitió incluir a algunos pacientes con fracaso a FAME biológicos (3,3% en el grupo sc y 4,5% iv). El objetivo primario del estudio era demostrar la no inferioridad de la formulación sc frente a la iv, mediante ACR20 a 24 semanas. Las características de los pacientes incluidos fueron similares en ambos grupos y presentaban una actividad clínica importante, ya que se requerían pacientes con un número de articulaciones dolorosas y tumefactas superior a 10 y un DAS28 superior a 6 en ambos grupos. El objetivo primario demostró que no había diferencias significativas, ya que el grupo tratado con abatacept sc tuvo una respuesta ACR20 de 76% y los pacientes tratados iv un 75,8%. Otros objetivos secundarios, ACR 50 y 70, fueron similares. No existieron diferencias al estratificar pacientes por peso. La discapacidad medida por el Health Assessment Questionnaire (HAQ) mejoró en ambos grupos. Se objetivó respuesta HAQ en el 68,2 vs. 63,8% en los pacientes sc e iv, respectivamente. La reducción del DAS28 fue similar en ambos grupos: 2,57 (sc) y 2,55 (iv). En ambos grupos se obtuvieron porcentajes similares de pacientes con baja actividad a los 6 meses (DAS28<3,2: 39,5 sc y 41,3 iv) y remisión: 24,2 y 24,8 para sc e iv, respectivamente. Tampoco existieron diferencias en la valoración por el paciente del dolor y la actividad de la enfermedad.
Comparación del ACQUIRE con el AIMLos datos de las fase de extensión abierta de los estudios AIM4 y ACQUIRE6 sirven como comparación de la administración de abatacept por vía iv y sc22. El análisis incluye a 1.372 pacientes del ACQUIRE y 378 del AIM en su fase de extensión abierta. Los pacientes incluidos en ambos estudios presentaban índices de actividad elevados, con un recuento de articulaciones inflamadas al inicio de 31 para el AIM y 29,6 en el ACQUIRE, y DAS28 de 6,4 y 6,2, respectivamente. Para la comparación de ambos grupos de tratamiento, se consideró el inicio a los 253 días, hasta la última visita, realizada el día 897. Los valores de ACR20, 50 y 70 fueron similares en ambos estudios tanto al inicio, como al final del seguimiento. Se obtuvo una eficacia ACR20 del 81,8 y 80,1% al inicio de los grupos iv y sc, que se mantuvo al final del periodo de observación (83,6 y 83,4%). El comportamiento fue similar para ACR 50, 50,8% (iv) y 54,9% (sc) al inicio de la comparación y al final 58,6% (iv) y 59,9% (sc). Las cifras de ACR 70 son 27,1% frente al 32% y 34,7 y 38,1% para el tratamiento iv y sc al principio y al final del tratamiento, respectivamente. La actividad de la enfermedad desciende a un DAS de 2,72 (iv) y 3,01 (sc) respecto a la basal al inicio de la comparación en el grupo ACQUIRE, con valores prácticamente idénticos en el AIM. El porcentaje de pacientes con baja actividad medida por DAS28 < 3,2 y remisión < 2,6 fue similar en ambos grupos de tratamiento. La baja actividad en el AIM pasó del 40% al inicio al 50,2% al final, y un porcentaje de remisión de 20,5 y 29,7. En el grupo ACQUIRE, se obtuvo baja actividad en el 44 y el 53,8%; remisión en el 27,3% al inicio y el 35% al final. En definitiva, los resultados de abatacept sc son superponibles a los obtenidos con la vía iv, tras comparar a los pacientes incluidos en el estudio AIM, con poblaciones similares, pacientes con enfermedad muy activa refractaria a MTX. El grado de mejoría ACR y los porcentajes de pacientes en remisión o baja actividad se mantiene durante el periodo de observación durante 2 años y medio.
Dosis de carga. (Nivel de evidencia 1b)Algunos estudios incluyeron una dosis iv de carga para conseguir rápidamente concentraciones terapéuticas del fármaco. En el inicio de la fase de estudio abierta del ensayo ALLOW, 167 pacientes recibieron abatacept sc con una dosis inicial iv de carga (aproximadamente 10mg/kg de peso). En la extensión a largo plazo del estudio ACCOMPANY, los pacientes fueron estratificados a abatacept sc, 125mg semanal sin dosis de carga inicial. En ambos estudios, los pacientes eran refractarios a FAME o a biológicos y similares según otros datos demográficos, aunque la gravedad de la enfermedad era menor en los pacientes que recibieron sobrecarga iv que en los que no la recibieron.
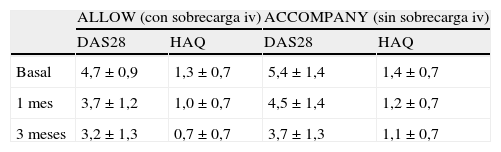
Un total de 167 pacientes participaron en el estudio ALLOW, en el que recibieron abatacept sc más dosis de carga iv inicial, y 100 pacientes entraron en el estudio ACCOMPANY y recibieron abatacept sc, con o sin MTX, pero sin sobrecarga. Las mejorías en DAS28 y HAQ fueron similares en ambos grupos con o sin dosis de carga iv (tabla 2). Aunque los datos deberían usarse con cautela por ser poblaciones de gravedad basal diferente, la magnitud de la mejoría fue similar en ambos estudios, independientemente de que se administrara una dosis inicial iv de carga23.
Comparación de los resultados de eficacia de los estudios ALLOW y ACCOMPANY
| ALLOW (con sobrecarga iv) | ACCOMPANY (sin sobrecarga iv) | |||
| DAS28 | HAQ | DAS28 | HAQ | |
| Basal | 4,7±0,9 | 1,3±0,7 | 5,4±1,4 | 1,4±0,7 |
| 1 mes | 3,7±1,2 | 1,0±0,7 | 4,5±1,4 | 1,2±0,7 |
| 3 meses | 3,2±1,3 | 0,7±0,7 | 3,7±1,3 | 1,1±0,7 |
Los resultados están expresados en media±desviación estándar.
Los datos farmacocinéticos obtenidos en estos estudios (comentados en extenso en este documento) indican también que no es precisa una dosis de carga iv, puesto que se obtienen concentraciones terapéuticas con abatacept sc en el momento de la segunda dosis semanal17.
Dosis fija de abatacept sc independiente del peso. (Nivel de evidencia 1b)Tanto en el estudio dase ii11 de dosis múltiples dependientes del peso comparadas con dosis fijas de 125mg de abatacept semanal, como en el estudio ACQUIRE6, los resultados de farmacocinética mostraron que una dosis semanal de 125mg de abatacept sc proporciona concentraciones séricas en rango terapéutico independientemente del peso del paciente.
En el ensayo ACQUIRE, los pacientes con AR activa, estratificados según peso corporal (< 60kg, 60-100kg, > 100kg), fueron aleatorizados a recibir abatacept iv, 10mg/kg de peso corporal cada 4 semanas, o abatacept sc 125mg. El grupo de abatacept sc recibió en el día 1 una infusión iv (10mg/kg) una hora antes de la primera dosis sc. El estudio farmacocinético y de inmunogenicidad mostró que dosis fijas de 125mg/semana eran bien toleradas, no inducían inmunogenicidad frente a CTLA-4 y producían concentraciones en rango terapéutico. La eficacia medida en respuesta ACR 20/50/70, DAS28, actividad baja de la enfermedad y remisión fue igual en los grupos de abatacept iv y sc. El análisis de subgrupos según el peso corporal no mostró tampoco diferencia en la respuesta ACR20 dependiente de la vía de administración.
Sustitución de abatacept por vía intravenosa por abatacept por vía subcutánea. (Nivel de evidencia 2b)En el estudio ATTUNE8, un ensayo abierto de brazo único de tratamiento, 71 pacientes procedentes de la extensión del AIM (abatacept en pacientes con fallo a MTX4) y 52 procedentes del estudio ATTAIN (abatacept en pacientes con fallo a anti-TNF5) fueron incluidos en un estudio de 12 semanas con extensión a un año para evaluar la seguridad del cambio de la formulación de abatacept iv a la sc (ambas en combinación con MTX). El porcentaje de pacientes en situación basal de remisión o actividad baja de la enfermedad se mantuvo estable, así como la función física evaluada mediante HAQ durante el periodo del estudio y en el seguimiento a un año. Esto se produjo en la totalidad de los pacientes y cuando ambas poblaciones, del AIM o ATTAIN, fueron analizadas por separado.
Eficacia tras suspender y reiniciar el tratamiento. (Nivel de evidencia 2b)En el estudio ALLOW7, 167 pacientes fueron tratados con abatacept sc+MTX. De ellos, 120 pacientes con disminución mayor de 0,6 en DAS28 a las 12 semanas fueron aleatorizados para continuar en abatacept sc+MTX o placebo+MTX hasta la semana 24. Al final de este periodo, todos los pacientes entraron en un estudio de extensión de tratamiento con abatacept sc junto con los 37 pacientes que no habían obtenido respuesta en la semana 12. La reintroducción de abatacept en el grupo de pacientes que lo había suspendido temporalmente recuperó la tasa de eficacia e indujo una respuesta clínica de la misma magnitud que la del grupo en que abatacept se había mantenido de manera ininterrumpida.
Monoterapia. (Nivel de evidencia 2b)En un estudio a 4 meses20, un grupo de 100 pacientes fueron estratificados para recibir abatacept sc+MTX (n=51) o abatacept sc en monoterapia (n=49). De estos, 50 y 46, respectivamente, entraron en el estudio de extensión. Ambos grupos de tratamiento eran similares, excepto que el grupo de monoterapia tenía mayor actividad que el grupo de combinación (DAS28 basal 5,6 frente a 5,0). Al cabo de 4 meses, el 55,3% (abatacept sc+MTX) y el 44,2% (abatacept en monoterapia) de los pacientes presentaban actividad baja de la enfermedad. Al final de un periodo de observación de 18 meses, esta situación estaba presente en el 57,5 del grupo con terapia combinada y en el 69,4% del brazo en monoterapia. Al cabo de 4 meses, la remisión DAS28 se produjo en 29,8 del grupo con terapia combinada y en el 32,6% de los que recibieron monoterapia. En la fase de extensión a los 18 meses, la remisión obtuvo unas tasas de un 42,5% (terapia combinada) y un 58,3% (monoterapia). Las tasas de abandono fueron también equivalentes.
Capacidad funcional. (Nivel de evidencia 2b)Abatacept sc mejora la capacidad funcional de los pacientes con AR de igual manera que abatacept iv. Igualmente, mantiene dicha mejora de la capacidad funcional cuando los pacientes o bien reciben abatacept sc tras un periodo de retirada, o bien lo reciben como continuación a abatacept iv. Las variaciones en la función física medida por el HAQ con abatacept sc se evaluaron frente a abatacept iv en pacientes con respuesta inadecuada a MTX (estudio ACQUIRE)6, en adultos con AR activa (estudio ALLOW)7 y en pacientes que cambian de tratamiento iv a sc (estudio ATTUNE)8.
El porcentaje de pacientes que alcanzó una mejoría en el (HAQ) en el ensayo ACQUIRE fue del 68,2% (intervalo de confianza del 95% [IC del 95%], 64,8 a 71,6) y del 63,8% (IC del 95%, 60,3 a 67,3) para los grupos de abatacept sc e iv, respectivamente (estimación de la diferencia [4,5%; IC del 95%, –0,4 a 9,4]). El cambio en la media ajustada±desviación estándar desde el momento basal hasta el mes 6 para el grupo de abatacept sc fue de 0,69±0,02 y de 0,70±0,02 para el grupo de abatacept iv. El criterio principal de valoración, la no inferioridad de abatacept sc frente a abatacept iv, basado en las respuestas ACR20 en el mes 6, se cumplió.
En el ensayo ALLOW, el criterio principal de valoración se cumplió (inmunogenicidad). Las evaluaciones de eficacia eran objetivos secundarios. Al final del periodo i, todos los pacientes presentaban reducciones similares en la puntuación de la actividad de la enfermedad (DAS 28). La media de las reducciones de HAQ para aquellos pacientes que permanecieron en el grupo de abatacept sc fueron: en el periodo i de –0,74 (IC del 95%, –0,91 a –0,57), en el periodo ii de –0,72 (IC del 95%, –0,95 a –0,50) y en el periodo iii de –0,86 (IC del 95%, –1,04 a –0,67). Para los pacientes a los que se suspendió abatacept sc en el periodo ii, la media de las reducciones de HAQ fue: en el periodo i de –0,63 (IC del 95%, –0,76 a –0,49), en el periodo ii de –0,50 (IC del 95%, –0,63 a –0,37) y en el periodo iii de –0,72 (IC del 95%, –0,85 a 0,60).
El objetivo principal del estudio ATTUNE era evaluar la seguridad de abatacept sc durante los 3 primeros meses después de cambiar de abatacept iv. El cambio de abatacept iv a sc se toleró bien, con un perfil de seguridad consistente con el observado durante el tratamiento con abatacept iv a largo plazo en los ensayos AIM4 y ATTAIN5. En el momento basal, la media±DE del HAQ para los pacientes que presentaban una respuesta inadecuada a MTX (n=71) era 0,91 (0,68) y para los pacientes con respuesta inadecuada a anti-TNF (n=52) era 0,98 (0,71). La media del HAQ, basado en un análisis según lo observado, para los pacientes con respuesta inadecuada a MTX en el mes 3 (n=71) fue 0,82±0,69 y en el mes 12 (n=69) fue 0,86±0,70. Para los pacientes con respuesta inadecuada a anti-TNF, el HAQ en el mes 3 (n=49) fue 0,92±0,67 y en el mes 12 (n=45) fue 0,97±0,66. Por lo que se puede concluir que abatacept sc mantiene la mejoría en el HAQ obtenida previamente con abatacept iv.
Comparación con adalimumab y progresión radiológica. (Nivel de evidencia 1b)La inhibición de la progresión radiográfica con abatacept sc fue evaluada en el ensayo clínico AMPLE10. Este estudio llevó a cabo una comparación de abatacept sc vs. adalimumab en pacientes, ambos con sus dosis estándar, con respuesta insuficiente a MTX. El objetivo primario era la no inferioridad en el ACR20 a los 12 meses de tratamiento, obteniéndose una respuesta clínica y de cinética similar con ambos fármacos. Un resumen presentado en el último congreso del ACR (Washington, 2012) demostró también que otras variables secundarias, como dolor, HAQ y los distintos componentes del SF36, alcanzaron valores similares24. Además, un criterio secundario de valoración importante fue la ausencia de progresión radiográfica evaluada usando el método de la puntuación total de Sharp modificada (mTSS) por van der Heijde. Se disponía de imágenes radiográficas emparejadas del año 1 de 290 y 289 pacientes de los grupos de abatacept y adalimumab, respectivamente. En ambos grupos de tratamiento, se observó una inhibición similar del daño radiográfico. Después de un año, la media de los cambios desde el momento basal en los grupos abatacept+MTX y adalimumab+MTX fue: puntuación total, 0,58 y 0,38; puntuación de erosión, 0,29 y –0,01, y estrechamiento del espacio articular, 0,28 y 0,39, respectivamente. La tasa de ausencia de progresión radiográfica (definida como el cambio detectable más pequeño ≤ 2,8) se observó en el 84,8 y el 88,6% de los pacientes de los grupos abatacept+MTX y adalimumab+MTX, respectivamente. Como conclusión, se puede decir que abatacept sc es similar en eficacia a adalimumab respecto a la inhibición de la progresión radiológica en la AR.
Inmunogenicidad. (Nivel de evidencia 2a)Todas las proteínas transformadas, como los agentes biológicos, tienen el potencial de desarrollar una respuesta inmunológica, pero la estructura es uno de los factores más importantes que determinan la aparición de la inmunogenicidad25. Los anticuerpos quiméricos, como el infliximab, debido a su parte murina, son los que con más frecuencia la desarrollan, mientras que los compuestos proteicos que se forman a partir de la porción extracelular de un receptor unido a una inmunoglobulina son los que menos potencial tienen, como sucede con el etanercept y el abatacept.
El abatacept es una proteína recombinante totalmente humana, formada por el dominio extracelular de la molécula CTLA4 y un fragmento de la porción Fc de la IgG1 humana, con solo un cambio de 4 aminoácidos en la región de la unión o bisagra, genéticamente modificados para reducir su unión a los receptores Fc y evitar la activación del complemento, por lo que, básicamente, si exceptuamos la región de unión o bisagra, la proteína es totalmente humana y no tiene por qué ser reconocida como extraña por el sistema inmunitario. Adicionalmente, también se ha propuesto que el abatacept puede reducir la formación de AAF debido a su mecanismo de acción.
Las consecuencias clínicas de la inmunogenicidad dependen de la cantidad de la reacción inmunológica y de la afinidad por el ligando y puede desde no tener consecuencias clínicas, si la cantidad de anticuerpo es pequeña y de baja afinidad, hasta provocar importantes alteraciones de la farmacocinética, la eficacia o la seguridad. La formación de AAF no neutralizantes origina la formación de pequeños inmunocomplejos, que son lentamente eliminados por el hígado y el bazo pero, teóricamente, el fármaco todavía conserva la capacidad de unirse al ligando y, por tanto, no pierden totalmente su eficacia. La formación de anticuerpos neutralizantes va a impedir que el fármaco se una a su diana terapéutica, por lo que su eficacia clínica va a verse afectada directamente. En el caso del abatacept, por ejemplo, existe el riesgo teórico de que el desarrollo de AAF neutralizantes pueda reaccionar con la molécula CTLA4 endógena expresada en los linfocitos T neutralizando la actividad de la proteína endógena y originar un estado inmunoestimulatorio que potencialmente puede empeorar la enfermedad de base o desarrollar nuevas enfermedades autoinmunes.
Uno de los aspectos más importantes del estudio de la inmunogenicidad es el desarrollo de la metodología para determinarla y, debido a que no existe todavía una estandarización de los métodos, los resultados no pueden ser contrastados ni comparados25. En la actualidad, solo existen datos de inmunogenicidad con abatacept reportados por Bristol-Myers Squibb y no existen grupos independientes que la hayan estudiado. Es importante reseñar que, con frecuencia, los datos proporcionados por las compañías en los estudios de registro y los datos originados en la práctica clínica a menudo no son similares, debido principalmente a la selección de los pacientes, diferentes metodologías y mayor duración del seguimiento de todos los pacientes en los estudios observacionales, mientras que en los estudios de extensión solo continúan los que obtienen un beneficio con el tratamiento, que son probablemente los que no forman AAF.
Se han usado 2 métodos para el estudio de la inmunogenicidad del abatacept sc y se basan en los primeros ensayos utilizados en los estudios de abatacept iv con algunas mejoras que aumentan la sensibilidad. Inicialmente, se desarrolló un ELISA dirigido contra la molécula entera de abatacept, pero para evitar los falsos positivos y la señal producida por la presencia del factor reumatoide y Ac no específicos anti-Fc, se desarrolló un ensayo más específico utilizando solo la parte de la molécula correspondiente al CTLA4 y utilizando como control positivo un pool de Ac policlonales antiabatacept obtenidos inoculando un mono26. Todos los ELISA están expuestos a que sus resultados estén interferidos por la presencia de fármaco libre, que no permite detectar los AAF27. Para minimizar este hecho, todas las muestras se recogieron justo antes de la administración de la siguiente dosis y se han realizado también estudios en pacientes en los que se habían perdido algunas infusiones o después del periodo de tratamiento.
El segundo método se basa en otro ELISA, denominado electroluminiscence (ECL), y ha demostrado ser más sensible y no se interfiere tanto por los niveles de fármaco circulante. Las muestras se tratan primero con ácido para disociar los complejos inmunes y minimizar los efectos de otros Ac inespecíficos. Este ensayo puede detectar AAF contra todas las regiones del abatacept8. Todas las muestras positivas con anticuerpos anti-CTLA4 en el ELISA y el ECL se estudiaron para identificar la presencia de Ac neutralizantes mediante un bioensayo para determinar si el suero de pacientes con AAF tiene la capacidad de inhibir el efecto inmunosupresor del abatacept en un cultivo de linfocitos. (Nivel de evidencia 5).
Los resultados de inmunogenicidad en los estudios con abatacept iv, tanto durante la fase de tratamiento ciego como la extensión a largo plazo, muestran unas cifras globales de inmunogenicidad muy bajas. De un total de 2.237 pacientes estudiados, 62 (2,8%) demostraron Ac antiabatacept o anti-CTLA4. Mediante el ECL, la cifra aumentó al 3% y no se demostró un efecto protector del MTX (2,3% con MTX frente a 1,4% sin MTX). Los pacientes que suspendieron el tratamiento tenían frecuencias de AAF ligeramente mayores que los que continuaban el tratamiento (7,4% frente al 2,6%) y solo en 8 pacientes de 13 estudiados se demostró actividad neutralizante. Aunque no se demostró ninguna relevancia clínica en cuanto a pérdida de eficacia, necesidad de aumentar la dosis o relación con efectos secundarios o aumento de desarrollo de enfermedades autoinmunes26.
El desarrollo del abatacept sc debía conseguir resultados de eficacia y seguridad similares a los de la ruta iv, con unos niveles de inmunogenicidad similar, contando con que la ruta de administración sc es más inmunogénica que la iv al formar agregados en el lugar de la inyección, procesar los antígenos de manera diferente y más eficiente y pasar casi todo el volumen administrado por la vía linfática para llegar al torrente sanguíneo1. El estudio se ha basado en 4 principios generales, un estudio comparando las 2 vías de administración, otro después de la suspensión y la reintroducción del fármaco, otro que investiga la relación con la medicación concomitante con MTX y finalmente el desarrollo de inmunogenicidad en pacientes que pasan de la ruta iv a la sc.
En el estudio ACQUIRE, fueron tan pocos los pacientes que desarrollaron Ac antiabatacept o dieron resultados positivos en el ensayo anti-CTLA4, que no se pudo demostrar ningún efecto en la eficacia o la seguridad en estos pacientes6. Estos resultados apoyan que la inmunogenicidad no está aumentada cuando se utiliza la ruta sc en comparación con la iv. En el estudio similar realizado en Japón28, a los 6 meses de tratamiento no se objetivaron AAF en ningún paciente de 59 del grupo sc frente a uno de 59 con iv.
En el estudio ALLOW7, se investiga el efecto de la suspensión y la reintroducción del fármaco en la inmunogenicidad en pacientes que reciben MTX. En los 3 primeros meses, todos los pacientes fueron tratados con abatacept sc de forma abierta y al final del periodo, 2 (1,7%) de 118 pacientes desarrollaron AAF. En el periodo abierto, ninguno de los pacientes que continuaron con el tratamiento desarrolló inmunogenicidad mientras que sí los desarrollaron 7 (9,6%) de entre los 73 que habían suspendido el fármaco durante 3 meses. En la fase iii de reintroducción del fármaco, se demostraron AAF en 1 (2,6%) de los 38 pacientes que permanecieron con el tratamiento durante todo el periodo y en 2 (2,7%) de 73 en los pacientes que reintrodujeron el tratamiento. Estos resultados pueden deberse a un efecto directo del fármaco inhibiendo el desarrollo de AAF durante el periodo de administración o a la pérdida de la interferencia del ELISA en presencia del fármaco. Independientemente de los motivos, se confirma, igual que el desarrollo iv, que la frecuencia de inmunogenicidad al suspender el fármaco y reintroducirlo es muy baja.
En el estudio ACCOMPANY, se investiga el efecto del tratamiento concomitante con MTX en la inmunogenicidad sin utilizar dosis de carga iv29. A los 4 meses de tratamiento, 3 (6,2%) de 48 pacientes en tratamiento combinado demostraron AAF frente a 2 (4,2%) de 47 en monoterapia. En el periodo de extensión, que llegó hasta los 16 meses, se demostraron AAF en 1 (2,1%) de los pacientes tratados en combinación frente al 0% en monoterapia. No se demostraron efectos en la eficacia ni en la seguridad.
Finalmente, en el estudio ATTUNE8, que investiga el desarrollo de inmunogenicidad en pacientes que cambian del tratamiento iv procedentes de los estudios AIM y ATTAIN al tratamiento sc, a los 3 meses del tratamiento sc, se demostraron AAF en 8 (6,6%) de 122 pacientes en el ELISA y en solo 1 (0,8%) de los 122 pacientes en el ensayo de ECL, lo que confirma las tasas muy bajas de inmunogenicidad del abatacept sc. (Nivel de evidencia 2b).
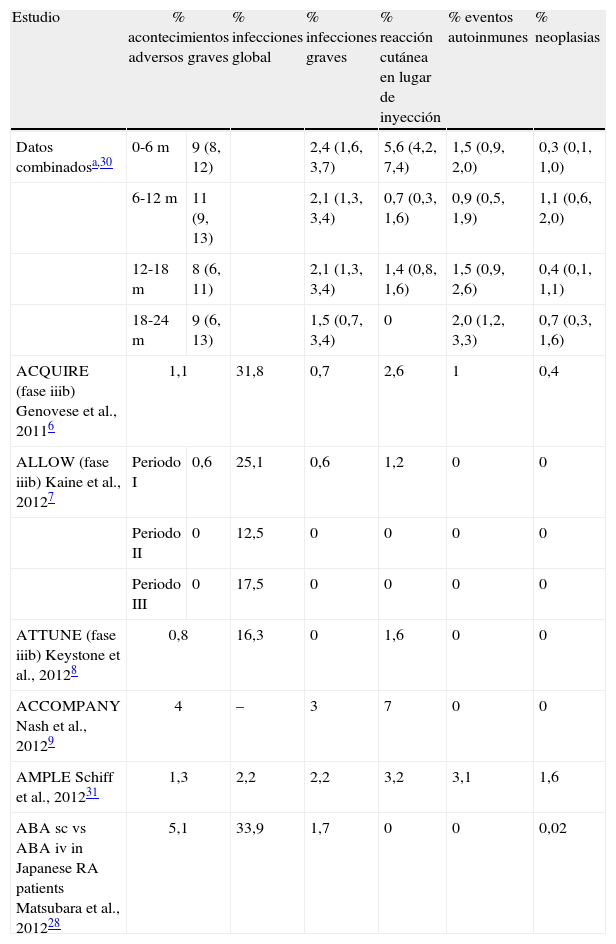
SeguridadLa administración de un medicamento biológico por vía sc o vía iv puede acompañarse de diferencias en la inmunogenicidad y en la farmacocinética. Estas diferencias pueden ir paralelas a las diferencias en la seguridad. La asunción «a priori» de que ambas formas de administración van a tener un perfil de seguridad similar puede ser errónea. Por tanto, la comparación es esencial (tabla 3).
Seguridad de abatacept sc en los ensayos clínicos
| Estudio | % acontecimientos adversos graves | % infecciones global | % infecciones graves | % reacción cutánea en lugar de inyección | % eventos autoinmunes | % neoplasias | |
| Datos combinadosa,30 | 0-6m | 9 (8, 12) | 2,4 (1,6, 3,7) | 5,6 (4,2, 7,4) | 1,5 (0,9, 2,0) | 0,3 (0,1, 1,0) | |
| 6-12m | 11 (9, 13) | 2,1 (1,3, 3,4) | 0,7 (0,3, 1,6) | 0,9 (0,5, 1,9) | 1,1 (0,6, 2,0) | ||
| 12-18m | 8 (6, 11) | 2,1 (1,3, 3,4) | 1,4 (0,8, 1,6) | 1,5 (0,9, 2,6) | 0,4 (0,1, 1,1) | ||
| 18-24m | 9 (6, 13) | 1,5 (0,7, 3,4) | 0 | 2,0 (1,2, 3,3) | 0,7 (0,3, 1,6) | ||
| ACQUIRE (fase iiib) Genovese et al., 20116 | 1,1 | 31,8 | 0,7 | 2,6 | 1 | 0,4 | |
| ALLOW (fase iiib) Kaine et al., 20127 | Periodo I | 0,6 | 25,1 | 0,6 | 1,2 | 0 | 0 |
| Periodo II | 0 | 12,5 | 0 | 0 | 0 | 0 | |
| Periodo III | 0 | 17,5 | 0 | 0 | 0 | 0 | |
| ATTUNE (fase iiib) Keystone et al., 20128 | 0,8 | 16,3 | 0 | 1,6 | 0 | 0 | |
| ACCOMPANY Nash et al., 20129 | 4 | – | 3 | 7 | 0 | 0 | |
| AMPLE Schiff et al., 201231 | 1,3 | 2,2 | 2,2 | 3,2 | 3,1 | 1,6 | |
| ABA sc vs ABA iv in Japanese RA patients Matsubara et al., 201228 | 5,1 | 33,9 | 1,7 | 0 | 0 | 0,02 | |
Acontecimiento adverso grave: acontecimiento que conlleva la suspensión del fármaco.
En el análisis combinado de seguridad30 de los ensayos de fase iia de búsqueda de dosis, ACCOMPANY9, ACQUIRE6, ALLOW7 y ATTUNE8, con una exposición de 4.214 pacientes-años de 1879 pacientes, las tasas de incidencia de acontecimientos adversos graves por 100 pacientes-años para abatacept sc eran 9,25 (IC del 95%, 7,46 a 11,48), 10,75 (IC del 95%, 8,72 a 13,24), 8,21 (IC del 95%, 6,29 a 10,72) y 8,85 (IC del 95%, 6,26 a 12,51) en los periodos 0-6, 6-12, 12-18 y 18-24 meses. En el ensayo AMPLE31 a un año, un 1,3% de los pacientes tratados con abatacept sc+MTX y un 3,0% de los pacientes tratados con adalimumab sc+MTX suspendieron la medicación por acontecimientos adversos graves.
En el ensayo ACQUIRE6, los porcentajes de suspensión de abatacept sc y abatacept iv por acontecimientos adversos graves eran del 1,1 y el 1,9%, respectivamente. En el ensayo ACCOMPANY9 a 4 meses, esas tasas fueron del 5,9% para abatacept sc+MTX y el 2,0% para abatacept sc en monoterapia. En el ensayo ATTUNE8, los porcentajes de suspensión por acontecimientos adversos graves fueron del 0,8% a los 3 meses y el 3,3% en el periodo acumulado. Estos porcentajes eran mayores en los pacientes que previamente habían fracasado con antagonistas de TNF.
Infecciones gravesEn el análisis combinado de seguridad30, las tasas de incidencia por 100 pacientes-años de infecciones graves para abatacept sc en los periodos 0-6, 6-12, 12-18 y 18-24 meses eran 2,42 (IC del 95%, 1,60 a 3,68), 2,12 (IC del 95%, 1,33 a 3,36), 1,28 (IC del 95%, 0,66 a 2,46) y 1,51 (IC del 95%, 0,68 a 3,36). Las neumonías y las infecciones urinarias fueron las infecciones graves más frecuentes. Quizás estas cifras son algo inferiores a las publicadas en ensayos clínicos con otros biológicos. Estas incidencias muestran que el riesgo de infección grave no aumenta en el tiempo. En el ensayo AMPLE31 a un año, el 2,2% de los pacientes tratados con abatacept sc+MTX y el 2,7% de los pacientes tratados con adalimumab sc+MTX tuvieron una infección grave.
Reacciones cutáneas en el lugar de la inyecciónEn el análisis combinado de seguridad30, el 3% de los pacientes tratados con abatacept sc desarrolló algún tipo de reacción cutánea en el lugar de la inyección. La tasa de acontecimientos adversos por 100 pacientes-años fue de 2,2. Estos porcentajes son algo inferiores a los de etanercept (6,5% a los 3 meses y 10% al año) y adalimumab (19,5-26,1% a 1 año)32-34. Por periodos de exposición, las tasas de incidencia por 100 pacientes-años de reacción cutánea en el lugar de la inyección entre 0-6, 6-12, 12-18 y 18-24 meses eran 5,59 (IC del 95%, 4,24 a 7,38), 0,72 (IC del 95%, 0,32 a 1,59), 1,40 (IC del 95%, 0,77 a 1,59) y 030. En el ensayo AMPLE a un año, el 3,2% de los pacientes tratados abatacept sc+MTX desarrolló algún tipo de reacción cutánea en el lugar de la inyección comparado con el 9,1% de los pacientes tratados con adalimumab sc+MTX.
En el ensayo ACQUIRE6 a 6 meses, el 2,6% de los pacientes en el grupo de los pacientes tratados con abatacept sc tuvo algún tipo de reacción cutánea en el lugar de la inyección comparado con el 2,5% en el grupo tratado con abatacept iv. Las reacciones más frecuentes en el grupo tratado con abatacept sc fueron el prurito y el eritema. En el ensayo ACCOMPANY9 a 4 meses, el 5,9% de los pacientes tratados con abatacept sc+MTX desarrolló reacciones cutáneas en el lugar de la inyección y el 8,2% de los pacientes tratados solo con abatacept sc. Las reacciones sistémicas 24 h después de la inyección aparecieron en el 7,8% de los pacientes tratados con terapia combinada y el 8,2% de los pacientes tratados con abatacept en monoterapia.
Acontecimientos autoinmunesEn el análisis combinado de seguridad30, la tasa de acontecimientos autoinmunes por 100 pacientes-años era 1,28 (IC del 95%, 0,9 a 1,75) en los pacientes tratados con abatacept sc y 1,99 (IC del 95%, 1,74 a 2,26) en los pacientes tratados con abatacept iv. Las tasas de incidencia para en abatacept sc en los periodos 0-6, 6-12, 12-18 y 18-24 meses eran 1,54 (IC del 95%, 0,91 a 2,60), 0,94 (IC del 95%, 0,47 a 1,88), 1,50 (IC del 95%, 0,85 a 2,63) y 2,00 (IC del 95%, 1,20 a 3,31). En el ensayo AMPLE a un año, el 3,1% de los pacientes tratados abatacept sc+MTX desarrollo algún tipo de acontecimiento autoinmune comparado con el 1,2% de los pacientes tratados con adalimumab sc+MTX.
En el ensayo ACQUIRE6, el 1% de los pacientes tratado con abatacept sc+MTX y el 0,8% de los tratados con abatacept iv+MTX, respectivamente, desarrollaron acontecimientos autoinmunes. En el ensayo ACCOMPANY9 a 4 meses, ninguno de los pacientes desarrolló acontecimientos autoinmunes. En el ensayo ATTUNE8, en el periodo acumulado, el 1,6% de los pacientes desarrolló acontecimientos autoinmunes.
TumoresEn el análisis combinado de seguridad30, las tasas de incidencia por 100 pacientes-años de tumores malignos para abatacept sc en los periodos 0-6, 6-12, 12-18 y 18-24 meses eran 0,33 (IC del 95%, 0,11 a 1,02), 1,05 (IC del 95%, 0,55 a 2,01), 0,37 (IC del 95%, 0,12 a 1,14) y 0,65 (IC del 95%, 0,27 a 1,57). En el ensayo AMPLE31 a un año, el 1,6% de los pacientes tratados con abatacept sc+MTX desarrolló algún tipo de tumor comparado con el 1,2% de los pacientes tratados con adalimumab sc+MTX.
En el ensayo ACQUIRE6 a 6 meses, el 0,4% de los pacientes en el grupo de los pacientes tratados con abatacept sc tuvo un tumor maligno o benigno comparado con el 0,7% en el grupo tratado con abatacept iv. Las reacciones más frecuentes en el grupo tratado con abatacept sc fueron el prurito y el eritema. En el periodo acumulado del ensayo ATTUNE8, el 1,6% de los pacientes desarrollo algún tumor.
En conclusión, el perfil de seguridad en los ensayos clínicos con abatacept sc es similar al de abatacept iv. Hay que tener en cuenta que la exposición en estos ensayos es aun corta y que es necesario que este perfil se complete con los datos que surgirán de los estudios observacionales generados por los registros.
DiscusiónEl tratamiento con terapias biológicas admiten 2 vías de administración, la iv y la sc. Cada una de ellas tiene sus ventajas y sus inconvenientes, aunque no cabe duda de que la segunda proporciona a los pacientes un grado de autonomía muy superior a la iv y les evita estancias en el hospital de día.
En este artículo, se revisan la eficacia y la seguridad de abatacept sc, un agente biológico que fue aprobado en España para uso iv hace 5 años. Abatacept es, hasta la fecha, el único agente biológico que admite ser administrado tanto por vía iv como sc, lo cual supone una ventaja añadida para el paciente, ya que en un momento determinado puede estar más indicado su administración por una de las 2 vías.
No obstante, el desarrollo de un fármaco por otra vía, en este caso sc, que la inicialmente aprobada requiere un desarrollo clínico prácticamente completo, ya que una forma de administración diferente de la aprobada inicialmente supone evaluar la farmacocinética, averiguar la dosis y la pauta de administración más idóneas y finalmente demostrar un grado de eficacia y seguridad al menos similar a la administración inicialmente aprobada. Otro hecho añadido es el de la inmunogenicidad. Está demostrado que el desarrollo de AAF tiene un impacto negativo en la eficacia del fármaco25,27. Por otro lado, la vía sc, por sus características, que se explican al principio de este artículo, tiene más posibilidades de producir inmunogenicidad.
Al margen de ensayos en fase ii, en los que se determinaron la dosis idónea y la seguridad11, el estudio quizás más relevante fue el ACQUIRE6, que demostró a las 24 semanas que abatacept sc a la dosis de 125mg semanales no era inferior a la administración iv a la dosis habitual. Todas las medidas de desenlace evaluadas fueron similares, siendo el objetivo principal el ACR20, que obtuvo una tasa de respuesta del 76 y el 75,8% en los grupos tratados iv y sc, respectivamente. Sin embargo, es preciso hacer notar que los pacientes tratados subcutáneamente recibieron una dosis de carga iv previo al paso de administración sc. Los pacientes que fueron seguidos de forma abierta y que recibían abatacept sc fueron comparados con los del estudio AIM, abatacept iv22, que por su diseño y características permitía comparar ambas poblaciones con diferentes vías de administración. Aunque siempre hay que tener mucha cautela al comparar poblaciones de ensayos clínicos diferentes, el seguimiento de ambas poblaciones no evidenció diferencias entre las principales medidas de actividad valoradas.
Otro de los temas discutidos ha sido la necesidad o no de administrar una dosis de carga iv previa al paso a sc. En el estudio ALLOW y el ACCOMPANY se compara la eficacia de abatacept sc con y sin dosis de carga, respectivamente (tabla 2), no encontrándose diferencias en la respuesta. Nuevamente, y como se comenta anteriormente, los resultados hay que tomarlos con cautela, al proceder de estudios distintos; no obstante, los datos de farmacocinética tampoco apoyan el uso de una dosis de carga.
Otro dato que despierta interés es si la dosis variaría en función del peso del paciente. El estudio ACQUIRE no demostró diferencias en la respuesta ACR20 en función del peso del paciente. Así mismo el paso a abatacept sc en pacientes previamente tratados con la formulación iv no produjo pérdida de eficacia ni un aumento de acontecimientos adversos8. Otro aspecto muy interesante dentro del desarrollo clínico del abatacept sc ha sido valorar si la suspensión del tratamiento y su posterior reiniciación supondrían una pérdida de eficacia. La respuesta fue que pacientes que habían sido tratados durante varias semanas con placebo más MTX, tras haber recibido previamente abatacept sc, perdían eficacia, pero la recuperaban con una respuesta de igual intensidad a la obtenida cuando estuvieron recibiendo el fármaco activo7. Otro estudio indica que la administración de abatacept sc en monoterapia puede ser una opción terapéutica en pacientes que no toleren MTX20. Finalmente, distintos estudios8,23,28 han demostrado que abatacept sc tiene idéntica capacidad que su homólogo iv en producir una mejoría de la función medida por el HAQ.
Uno de los ensayos más interesantes realizados con abatacept sc ha sido el llevado a cabo en una comparación directa con adalimumab10. El estudio estaba diseñado para no demostrar inferioridad en el ACR20 al año de tratamiento con ambos fármacos y además se estudiaron otros objetivos secundarios, tanto clínicos como radiológicos. Abatacept no demostró ser inferior en eficacia ni en otros parámetros secundarios que medían otros componentes de actividad o discapacidad. Pero quizás lo más relevante fue que abatacept sc se mostró como un fármaco con la misma capacidad de impedir la progresión radiológica que adalimumab. Abatacept iv siempre ha sido considerado como un fármaco con menor capacidad para frenar el daño estructural, comparado con los anti-TNF en su globalidad35. Si esta nueva situación se debe a la nueva formulación o, por el contrario, la extrapolación de datos que se hizo con abatacept iv llevó a conclusiones no del todo acertadas, es una cuestión que no tiene respuesta, pero lo que deja fuera de dudas es que para hablar con rotundidad de mayor o menor eficacia, o de otras medidas de desenlace, la demostración más contundente es la comparación directa entre fármacos y no la obtención de datos por medios indirectos.
Con respecto a otros aspectos de interés, abatacept sc se comporta como un fármaco muy poco inmunógeno. Prácticamente todos los estudios realizados con esta nueva formulación (ACQUIRE, ALLOW, ACCOMPANY y ATTUNE) demuestran tasas de AAF nulas o meramente simbólicas y que no tuvieron ningún impacto en la eficacia ni en la seguridad del paciente.
Finalmente, y en lo que a seguridad concierne, y relacionándolo específicamente con acontecimientos adversos graves, los distintos estudios clínicos no han demostrado un incremento significativo de los acontecimientos adversos graves6-9. Así, en el estudio combinado de seguridad de los ensayos de fase de búsqueda (fase ii) y los de fase iii6-9, las tasas de acontecimientos adversos graves estuvieron dentro del margen esperado. Por otro lado, en el análisis combinado de seguridad30, las tasas de incidencia por 100 pacientes-años de infecciones graves estuvieron ligeramente por debajo de lo publicado y además demuestran que no aumentan con el tiempo.
En el estudio AMPLE10, que comparó abatacept sc con adalimumab, solo el 1,3% de los tratados con abatacept sc tuvieron acontecimientos adversos graves comparados con un 3% en los pacientes que recibieron adalimumab. Con respecto a las reacciones cutáneas, solo el 3% desarrolló manifestaciones clínicas. Estas cifras son algo inferiores a lo mostrado por etanercept y adalimumab, por encima del 10%. Las reacciones más frecuentes son prurito y eritema, y parece existir una tendencia superior a su aparición cuando abatacept sc es administrado en monoterapia que cuando se dé en combinación con MTX. En lo que concierne a los acontecimientos autoinmunes, las tasas de aparición fueron también muy bajas, no sobrepasando en ningún caso el 2%6,8-10,30. El desarrollo de abatacept sc no despertó ningún signo de alarma en lo que respecta a un incremento de la tasa de tumores.
En resumen, abatacept sc se presenta como un fármaco eficaz y seguro y, por lo tanto, como una alternativa más para utilizar entre los múltiples tratamientos con que cuenta hoy en día el reumatólogo para tratar la AR. Además, cuenta con la ventaja de ser el único agente biológico que se puede administrar por vía iv y sc, lo cual puede facilitar su uso en determinados pacientes.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
FinanciaciónEste documento práctico se ha financiado a través de una aportación realizada al Servicio de Reumatología del Hospital Universitario La Paz (AREPAZ) por Bristol Myers Squibb (España). La elección de los expertos fue responsabilidad exclusiva del coordinador del proyecto (EMM). Ningún empleado de la compañía participó en las reuniones científicas ni conoció su desarrollo hasta que el proyecto estuvo finalizado.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.