Las infecciones son una importante causa de morbimortalidad en los pacientes con enfermedades autoinmunes sistémicas. El objetivo del presente estudio es describir la frecuencia de infecciones en una cohorte histórica de la policlínica de EAS del Hospital Maciel, según tipo de enfermedad y tratamiento recibido.
Material y métodosSe realizó un estudio analítico, retrospectivo y observacional de 339 pacientes con EAS asistidos en la consulta ambulatoria en el período comprendido entre el 1 de enero de 2012 y el 28 de febrero del 2019. Se analizaron las complicaciones infecciosas, según tratamiento y enfermedad.
ResultadosSe encontraron 339 casos, mediana de edad de 56, mayoría sexo femenino. La mayoría de los casos presentaron LES (30,1%) y AR (23,6%), seguidos de síndrome antifosfolipídico (20,4%) y síndrome de Sjögren (12,1%). La hidroxicloroquina (66%), seguida de los corticoides (55,5%) fueron los tratamientos más frecuentemente utilizados. El 13,3% recibieron terapias biológicas. 46,9% de los casos presentaron alguna complicación infecciosa, 95% fueron no oportunistas. Las infecciones respiratorias fueron las más frecuentes (48,6%), seguidas de las urinarias (31,7%) y de piel y partes blandas (17,6%). Al comparar los grupos de infectados y no infectados se hallaron diferencias significativas en las siguientes variables: metotrexate, micofenolato, corticoides, terapias biológicas, combinación de fármacos, enfermedad activa, AR y casos con solapamiento. El uso de hidroxicloroquina y sulfasalazina se asoció con menor riesgo de infecciones en pacientes con AR.
ConclusionesLas infecciones son una complicación frecuente en los pacientes con EAS, por las alteraciones inmunitarias de la propia enfermedad y por los tratamientos indicados, fundamentalmente corticoides y biológicos. Se destaca la importancia del cribado y profilaxis de infecciones antes del inicio del tratamiento.
Infections are a major cause of morbidity and mortality in patients with systemic autoimmune diseases. The aim of the present study is to describe the frequency of infections in a historical cohort of the SAD polyclinic of the Maciel Hospital, according to the type of disease and treatment received.
Material and methodsAn analytical, retrospective and observational study was conducted in 339 patients with SAD attended at the outpatient clinic in the period from January 1, 2012 to February 28, 2019. Infectious complications were analysed according to treatment and disease.
Results339 cases, median age 56, mostly female. Most cases presented SLE (30.1%) and RA (23.6%), followed by antiphospholipid syndrome (20.4%) and Sjögren's syndrome (12.1%). Hydroxychloroquine (66%), followed by corticosteroids (55.5%) were the most frequently used treatments. Thirteen point three percent received biological therapies: 46.9% of the cases presented some infectious complication, 95% were non-opportunistic. Respiratory infections were the most frequent (48.6%) followed by urinary infections (31.7%) and skin and soft tissue infections (17.6%). On comparing the infected and non-infected groups, significant differences were found in the following variables: methotrexate, mycophenolate, corticoids, biological therapies, combination of drugs, active disease, RA and cases with overlap. The use of hydroxychloroquine and sulfasalazine was associated with a lower risk of infection in patients with RA.
ConclusionsInfections are a frequent complication in patients with RA, due to the immune disturbances of the disease itself and prescribed treatments, mainly corticoids and biologicals. The importance of screening and infection prophylaxis before starting treatment is stressed.
Las infecciones son una importante causa de morbimortalidad en las enfermedades autoinmunes sistémicas (EAS) por alteraciones inmunitarias de la propia enfermedad y del tratamiento inmunosupresor1,2.
La mayoría de los estudios de infecciones en EAS se han realizado en lupus eritematosos sistémico (LES) y en artritis reumatoide (AR). En el LES existe alta prevalencia de infecciones, constituyendo una de las principales causas de mortalidad en los primeros cinco años de la enfermedad. En la AR existe un riesgo dos veces mayor que en la población general1-7.
Las infecciones difieren en severidad; las formas leves son las más frecuentes. Los sitios afectados con mayor frecuencia son respiratorio, urinario, piel y tejidos blandos8-10. Los agentes etiológicos son variados, virales, bacterianos y otros; oportunistas y no oportunistas2,4,6,7,10-17.
Dentro de las infecciones oportunistas, la tuberculosis latente se puede reactivar y generar enfermedad en pacientes bajo tratamiento corticoideo y/o inmunosupresor18-21.
Los factores de riesgo asociados con mayor riesgo de infección en pacientes con LES son: actividad de la enfermedad, presencia de nefritis lúpica, duración de la enfermedad, leucopenia, anticuerpos anti-DNA, dosis y tiempo de tratamiento con corticoides y uso de inmunosupresores1-3,11-14,16. El tratamiento con hidroxicloroquina (HCQ) ha sido señalado en varios estudios como factor protector de infecciones16,22-24.
En pacientes con AR, los factores de riesgo son edad avanzada, enfermedad extraarticular, actividad de la enfermedad, enfermedad pulmonar obstructiva crónica, enfermedad pulmonar intersticial, enfermedad renal crónica, linfopenia, uso de corticosteroides y fármacos modificadores de la enfermedad (FAMEs)6,7.
Las terapias biológicas han cambiado la evolución de las EAS, aunque se asocian a un riesgo tres veces mayor de infecciones6,25-28.
Las EAS representan un desafío diagnóstico y terapéutico para el médico, fundamentalmente ante un paciente con fiebre en que debe dilucidar si corresponde a infección o a actividad de la enfermedad. Se requiere una evaluación clínica y paraclínica completa para lograr el diagnóstico y adoptar las decisions, según el caso24,29.
No existen trabajos de revisión de infecciones en pacientes con EAS en Uruguay, lo que motivó el interés de los autores en el tema.
El objetivo del estudio es describir la frecuencia de infecciones en una cohorte histórica de pacientes con EAS, según enfermedad, actividad de la misma y tratamiento.
Material y métodosSe realizó un estudio analítico, retrospectivo y observacional de una cohorte histórica. Se incluyeron todos los pacientes con diagnóstico confirmado de EAS (339), asistidos en la consulta ambulatoria de EAS del Hospital Maciel, en el período comprendido entre el 1 de enero del 2012 al 28 de febrero del 2019.
Se excluyeron los pacientes que concurrieron en menos de dos oportunidades a la consulta.
Se revisaron las historias clínicas manuscritas obtenidas del archivo médico y de los registros electrónicos del Hospital.
Se registraron las siguientes variables: edad, sexo, procedencia, hipertensión arterial (HTA), diabetes mellitus (DM), dislipemia, obesidad, tabaquismo, enfermedad cardiovascular (ECV), enfermedad renal crónica (ERC), enfermedad pulmonar obstructiva crónica (EPOC); clasificación diagnóstica de EAS (de acuerdo a los criterios clasificatorios actuales); tratamiento en los tres meses previos: hidroxicloroquina, inmunosupresores sintéticos o biológicos; dosis promedio de corticoides (prednisona o equivalente) durante la infección y al registro; complicaciones infecciosas (órgano/sistema comprometido), microorganismo causal, infecciones oportunistas, hospitalización e infecciones intrahospitalarias.
Se consideraron graves las infecciones oportunistas, las que requirieron antibioticoterapia endovenosa u hospitalización y aquellas con riesgo vital.
Se consideraron infecciones oportunistas las producidas por patógenos específicos o presentaciones que llevaran a plantear alteración inmunitaria en el contexto de la terapia biológica8-10.
Análisis estadístico: Las variables cualitativas fueron representadas en tablas, utilizando frecuencias absolutas y frecuencias relativas porcentuales y en gráficos de barras simples (una sola variable) o estratificadas (dos variables simultáneamente) y diagramas sectoriales. Las variables cuantitativas fueron representadas utilizando como medidas de resumen mediana e intervalo intercuartílico (previamente estudiada la normalidad a través de los test Kolmogorov-Smirnov o Shapiro-Wilk) mínimo y máximo. Para estudiar la asociación entre variables cualitativas se utilizó el test de chi-cuadrado y para comparar medianas entre dos grupos independientes se utilizó el test U de Mann-Whitney. El modelo de regresión logística binaria multivariada fue utilizado para detectar predictores independientes de complicaciones infecciosas, calculando la odds ratio e intervalo de confianza 95% para las diferentes covariables de interés. Se realizó una curva ROC para determinar la dosis segura de corticoides y un test de propensión para valorar a los mismos como factor de confusión. Se consideran significativos valores p menores que 0,05. El software utilizado fue Microsoft Excel e IBM SPSS versión 22.0.
La investigación se realizó respetando el marco legal uruguayo y los datos fueron manejados de manera confidencial. Los resultados fueron utilizados con fines de formación y académicos.
ResultadosEl total de pacientes incluidos en el estudio fueron 339, con una mediana de edad de 56 años y rango etario entre 19 y 90; 308 casos (90,9%) fueron de sexo femenino y 31 (9,1%) masculino.
En la población estudiada se identificaron como factores de riesgo cardiovascular, DM en 27 (8,0%), HTA en 129 (38,1%), dislipemia en 35 (10,3%), obesidad en 24 (7,1%). Otras comorbilidades crónicas fueron EPOC en 11 (3,2%) y ERC en 12 (3,5%), tabaquismo en 53 (15,6%) y ECV en 42 (12,4%).
Con respecto al diagnóstico de EAS, 102 casos correspondían a LES (30,1%), 80 a AR (23,6%), 69 a síndrome antifosfolipídico (SAF) (20,4%) y 41 a síndrome de Sjögren (12,1%). Se encontraron 52 casos de solapamiento de EAS. Los solapamientos más frecuentes fueron LES con AR y LES con síndrome de Sjögren, con 12 casos cada uno, seguidos por siete casos de AR solapados con síndrome de Sjögren. Los 21 casos restantes fueron combinaciones variadas de EAS.
En relación con los tratamientos recibidos, hidroxicloroquina (HCQ) fue el fármaco más frecuentemente indicado con 224 casos (66,1%), seguido por corticoides en 188 (55,5%), con una dosis media de 15 mg/día. Los inmunosupresores sintéticos prescritos en orden decreciente fueron: metotrexate, azatioprina, micofenolato y leflunomida.
Los biológicos se utilizaron en 45 casos (13,3%), a saber: adalimumab 17 (38,6%), rituximab 14 (31,8%), tocilizumab 13 (29,5%) y etanercept siete (15,9%). Siete pacientes (15,9%) recibieron más de un biológico en forma secuencial.
En 90 pacientes (26,5%) se asociaron fármacos (tabla 1); 143 casos (46,9%) presentaron alguna complicación infecciosa, 137 infecciones no oportunistas de diversas etiologías (96,4%). Se excluyeron en este análisis los casos de SAF primarios.
Descripción de la población
| Total n = 339 | |
|---|---|
| Edad | Mediana: 56 (19-90) |
| Sexo | |
| Femenino | 308 (90,9%) |
| Masculino | 31 (9,1%) |
| Procedencia | |
| Montevideo | 197 (58,1%) |
| Interior | 90 (26,5%) |
| Sin dato | 51 (15%) |
| ENFERMEDAD AUTOINMUNE | |
| LES | 102 (30,09%) |
| Artritis reumatoide | 80 (23,60%) |
| Esclerosis sistémica | 31 (9,14%) |
| Enfermedad mixta de tejido conectivo | 3 (0,88%) |
| Miopatías inflamatorias | 9 (2,6%) |
| Síndrome de Sjögren | 41 (12,09%) |
| Vasculitis | 18 (5,31%) |
| Enfermedad indiferenciada de tejido conectivo | 14 (4,13%) |
| Síndrome antifosfolipídico | 69 (20,35%) |
| Solapamiento | 52 (15,3%) |
| Otras | 38 (11,21%) |
| COMORBILIDADES | |
| HTA | 129 (38,1%) |
| DM | 27 (8,0%) |
| Dislipemia | 35 (10,3%) |
| Obesidad | 24 (7,1%) |
| Tabaquismo | 53 (15,6%) |
| EPOC | 11 (3,2%) |
| ERC | 12 (3,5%) |
| ECV | 42 (12,4%) |
| TRATAMIENTO RECIBIDOS | |
| Hidroxicloroquina | 224 (66,1%) |
| Metotrexate | 126 (37,2%) |
| Leflunomida | 23 (6,8%) |
| Sulfasalazina | 33 (9,7%) |
| Azatioprina | 81 (23,9%) |
| Ciclofosfamida | 41 (12,1%) |
| Ciclosporina | 2 (0,6%) |
| Micofenolato | 33 (9,7%) |
| Talidomida | 1 (0,3%) |
| Corticoides | 188 (55,5%) |
| Terapias biológicas | 45 (13,3%) |
| Combinación de fármacos | 90 (26,5%) |
| FÁRMACO BIOLÓGICO | N = 45 |
| Adalimumab | 17 (38,6%) |
| Rituximab | 14 (31,8%) |
| Tocilizumab | 13 (29,5%) |
| Etanercept | 7 (15,9%) |
| Más de un biológico (secuencial) | 7 (15,9%) |
En relación con el número de episodios durante el período de seguimiento, 95 pacientes (66,9%) presentaron una infección única y 42 (33,1%) dos o más.
Del total de casos, 53 (37,3%) presentaban enfermedad activa (p 0,009) y 50 (35,2%) recibían combinación de fármacos al momento de la infección (p 0,036).
Dentro de las infecciones no oportunistas, las respiratorias fueron las más frecuentes, con 69 casos (48,6%): 45 (31,7%) neumonía aguda comunitaria, 26 (18,3%) traqueobronquitis aguda y 5 (3,5%) otitis media. Le siguieron en frecuencia las infecciones del tracto urinario 45 (31,7%), piel y partes blandas 25 (17,6%) y un caso de meningitis aguda bacteriana.
El microorganismo causal se logró identificar en 49 casos (32,4%). Los más frecuentes fueron Escherichia coli con 21 aislamientos (14,8%) y Streptococcus pneumoniae con 6 (4,2%). Siete casos (4,9%) correspondieron a infecciones intrahospitalarias.
Se observaron 13 casos (9,2%) de infecciones oportunistas con la siguiente distribución: cuatro casos de tuberculosis pulmonar, uno de ellos asociado posteriormente a neumonía a Pneumocystis jirovecii, ocho casos de herpes zóster y un paciente con toxoplasmosis encefálica.
Con relación a la severidad, 58 casos (40,8%) fueron infecciones graves; 38 casos (26,8%) requirieron hospitalización en una oportunidad, 12 (8,5%) en dos y seis pacientes (4,2%) ingresaron a Unidad de Cuidados Intensivos.
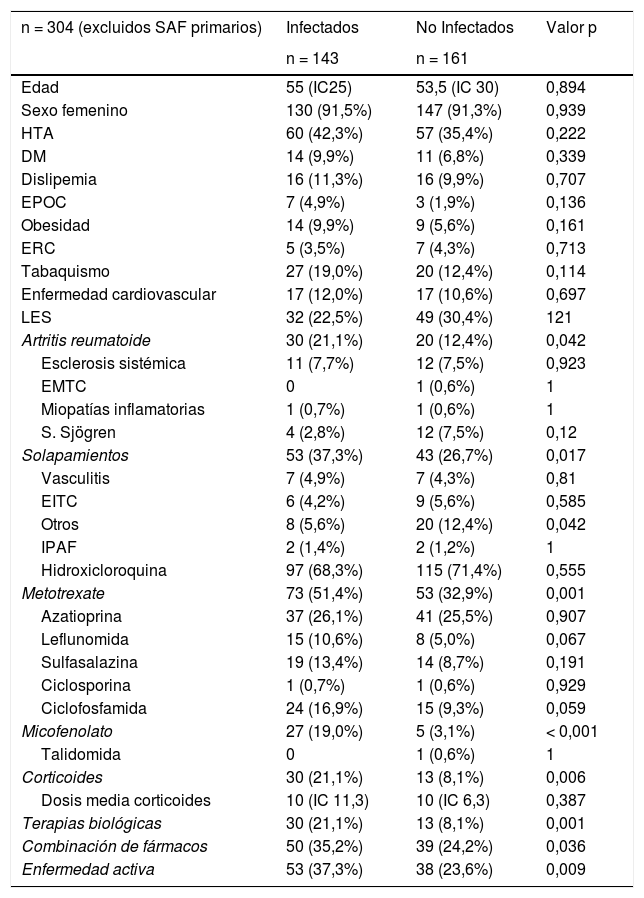
Al comparar los grupos de pacientes con o sin complicación infecciosa se halló diferencia significativa en las variables metotrexate, micofenolato, corticoides, terapias biológicas, combinación de fármacos, enfermedad activa, AR y solapamientos. Con respecto a las comorbilidades, no se halló diferencia estadísticamente significativa entre ambos subgrupos. Se realizó estudio de propensión para eliminar el sesgo atribuible al tratamiento con corticoides y al uso de biológicos. Se mantiene un aumento significativo del riesgo de dos veces y media mayor en pacientes con biológicos en relación con pacientes sin biológicos, OR 2,48 (IC 1,165-4,977) (tabla 2).
Comparación entre infectados y no infectados
| n = 304 (excluidos SAF primarios) | Infectados | No Infectados | Valor p |
|---|---|---|---|
| n = 143 | n = 161 | ||
| Edad | 55 (IC25) | 53,5 (IC 30) | 0,894 |
| Sexo femenino | 130 (91,5%) | 147 (91,3%) | 0,939 |
| HTA | 60 (42,3%) | 57 (35,4%) | 0,222 |
| DM | 14 (9,9%) | 11 (6,8%) | 0,339 |
| Dislipemia | 16 (11,3%) | 16 (9,9%) | 0,707 |
| EPOC | 7 (4,9%) | 3 (1,9%) | 0,136 |
| Obesidad | 14 (9,9%) | 9 (5,6%) | 0,161 |
| ERC | 5 (3,5%) | 7 (4,3%) | 0,713 |
| Tabaquismo | 27 (19,0%) | 20 (12,4%) | 0,114 |
| Enfermedad cardiovascular | 17 (12,0%) | 17 (10,6%) | 0,697 |
| LES | 32 (22,5%) | 49 (30,4%) | 121 |
| Artritis reumatoide | 30 (21,1%) | 20 (12,4%) | 0,042 |
| Esclerosis sistémica | 11 (7,7%) | 12 (7,5%) | 0,923 |
| EMTC | 0 | 1 (0,6%) | 1 |
| Miopatías inflamatorias | 1 (0,7%) | 1 (0,6%) | 1 |
| S. Sjögren | 4 (2,8%) | 12 (7,5%) | 0,12 |
| Solapamientos | 53 (37,3%) | 43 (26,7%) | 0,017 |
| Vasculitis | 7 (4,9%) | 7 (4,3%) | 0,81 |
| EITC | 6 (4,2%) | 9 (5,6%) | 0,585 |
| Otros | 8 (5,6%) | 20 (12,4%) | 0,042 |
| IPAF | 2 (1,4%) | 2 (1,2%) | 1 |
| Hidroxicloroquina | 97 (68,3%) | 115 (71,4%) | 0,555 |
| Metotrexate | 73 (51,4%) | 53 (32,9%) | 0,001 |
| Azatioprina | 37 (26,1%) | 41 (25,5%) | 0,907 |
| Leflunomida | 15 (10,6%) | 8 (5,0%) | 0,067 |
| Sulfasalazina | 19 (13,4%) | 14 (8,7%) | 0,191 |
| Ciclosporina | 1 (0,7%) | 1 (0,6%) | 0,929 |
| Ciclofosfamida | 24 (16,9%) | 15 (9,3%) | 0,059 |
| Micofenolato | 27 (19,0%) | 5 (3,1%) | < 0,001 |
| Talidomida | 0 | 1 (0,6%) | 1 |
| Corticoides | 30 (21,1%) | 13 (8,1%) | 0,006 |
| Dosis media corticoides | 10 (IC 11,3) | 10 (IC 6,3) | 0,387 |
| Terapias biológicas | 30 (21,1%) | 13 (8,1%) | 0,001 |
| Combinación de fármacos | 50 (35,2%) | 39 (24,2%) | 0,036 |
| Enfermedad activa | 53 (37,3%) | 38 (23,6%) | 0,009 |
EMTC: Enfermedad mixta del tejido conectivo; EITC: Enfermedad indiferenciada del tejido conectivo; IPAF: Neumonía intersticial con hallazgos autoinmunes.
Se confeccionó una curva ROC para estimar la dosis de corticoides «segura», estimándola en 6,25 mg/día, con una sensibilidad de 0,81 y especificidad de 0,33. Se señala que se trata de una curva con un área de 0,618 sin diferencia significativa 0,5 (valor p = 0,09).
Al analizar la frecuencia de complicaciones infecciosas, según tipo de EAS a través de regresión logística binaria univariada, se observa un mayor riesgo de infecciones en casos de AR y solapamiento, con un aumento de más del doble del riesgo con un OR de 2,55 (IC 1,157-5,622) y 2,095 (IC 1,058-4,15), respectivamente.
Al comparar de la frecuencia de infecciones en el subgrupo de pacientes con LES, se halló una diferencia significativa con metotrexate, con un riesgo cinco veces mayor, OR 4,91 (IC 1,19-20,18). No se encontró riesgo aumentado con diferencia significativa para el resto de los tratamientos. En el subgrupo de AR se observó que el uso de hidroxicloroquina o sulfasalazina disminuyó el riesgo de infecciones más de un 50%, con un OR de 0,145 (IC 0,039-0,544) y 0,136 (IC 0,031-0,598), respectivamente.
DiscusiónLas infecciones son una complicación frecuente en los pacientes con EAS. En este estudio se observó en 46,9% de los casos, similar a lo reportado en series internacionales1,6,7,12.
Las infecciones fueron más frecuentes en los casos con AR y en formas de solapamiento, que en pacientes con LES (con diferencia estadísticamente significativa), situación distinta a lo que reportan otros estudios. Una explicación posible podría ser el mayor acceso a biológicos en pacientes con AR que con LES, a través del Fondo Nacional de Recursos en Uruguay, y que los pacientes con biológicos tienen mayor frecuencia de infecciones.
El 40% de las infecciones fueron graves, considerando infecciones causadas por oportunistas o que requieren hospitalización, uso de antibioticoterapia endovenosa o que llevan a la muerte. Se clasifican como infecciones no graves aquellas que no entran en la definición de grave8-10.
En esta cohorte, la mayoría de los casos correspondieron a infecciones no oportunistas (95%). Un tercio de los pacientes presentaron más de un episodio de infección.
Las infecciones más frecuentes fueron respiratorias, urinarias, de piel y de partes blandas, similar a lo reportado en otras series2,4,6,7,10-17. Casi un 5% correspondieron a infecciones intrahospitalarias.
Con respecto a lo publicado en relación con la microbiología, las bacterias son los microorganismos más frecuentemente aislados, seguidas de virus y hongos. La frecuencia de bacterias inespecíficas es similar a lo que ocurre en la población general, mientras que algunas de ellas, como las infecciones por Salmonella se producen con mayor frecuencia en pacientes con LES que tienen niveles más bajos de complemento, asplenia o terapia inmunosupresora2,4,6,7,10-17.
En esta serie se logró el diagnóstico microbiológico en la tercera parte de los casos. Las infecciones bacterianas fueron las más frecuentes, con Escherichia coli y Streptococcus pneumoniae como microorganismos más prevalentes, coincidiendo con el perfil microbiológico de los focos infecciosos más frecuentes en ésta y otras series2,4,6,10,11,13,14,16,17.
Los 13 casos de infecciones oportunistas se observaron en pacientes con AR y con LES.
Se encontraron cuatro casos de tuberculosis pulmonar. Se describe que la tuberculosis es más frecuente en sujetos con LES o AR que en la población general. En cuanto a la presentación clínica, la tuberculosis pulmonar es la forma más frecuente (como en esta serie), pero se describen con mayor frecuencia formas extrapulmonares y cuadros más graves que en la población general2,18-21.
Se registraron ocho casos de herpes zóster en pacientes en tratamiento con inmunosupresores sintéticos. Se señala mayor frecuencia de herpes zóster y algunos estudios señalan que no se vincula con la actividad de la enfermedad2,22,23.
Las infecciones micóticas más frecuentes son por Candida albicans y por Pneumocystis jirovecii (PCP). En esta serie, se señala un único caso de PCP en paciente con tratamiento corticoideo asociado a varios fármacos inmunosupresores sintéticos.
Se debe tener presente el riesgo de infecciones oportunistas en esta población para realizar un cribado, profilaxis y vacunaciones cuando corresponda30
La actividad de la enfermedad constituye un factor de riesgo independiente de desarrollo de complicaciones infecciosas en las personas con EAS. En la cohorte analizada, los pacientes con enfermedad activa presentaron mayor frecuencia de infecciones, en concordancia con lo reportado en la literatura internacional1-7.
El riesgo de infecciones varía según los tratamientos realizados, como se reporta en varias bases de datos de AR europeas y norteamericanas.
Cuando se analizó la frecuencia de infecciones, según los tratamientos recibidos, los fármacos que se asociaron en forma independiente a mayor riesgo de infecciones fueron los biológicos, micofenolato, metotrexate y corticoides solos o combinados. El uso combinado de inmunosupresores se asoció significativamente a mayor riesgo de infecciones.
En esta serie, la terapia con biológicos tuvo dos veces y media más riesgo de infecciones con respecto a los casos sin tratamiento biológico, en forma similar a lo reportado en series internacionales6,9,10,25,27. Por otro lado, se destaca que el uso de terapias biológicas se mantiene como factor de riesgo independiente al uso de corticoides.
El registro alemán RABBIT muestra que el riesgo de infecciones con biológicos es mayor que con los tratamientos no biológicos, y que se incrementa en forma directamente proporcional con el aumento de la dosis de corticoides en ambos grupos25.
En el registro español de biológicos BIOBADASER, 35% de los eventos adversos fueron infecciones, con una mortalidad de casi 32%27.
En un metaanálisis de 70 estudios en AR, que incluyó más de 32.000 pacientes, se demostró un aumento global del riesgo de infecciones oportunistas, con 1,7 infecciones por 1.000 pacientes tratados con terapias biológicas9. El registro de datos británico (BSRBR) refiere un riesgo de infecciones que se multiplica por 4, sobre todo en los primeros tres a seis meses del uso de terapias biológicas, siendo la tuberculosis la infección oportunista más frecuente6. En otro metaanálisis, se comparó la tasa de infecciones en diversas enfermedades inflamatorias entre anti-TNFs, mostrando un riesgo ligeramente menor con etanercept, con menor frecuencia de herpes zóster, tuberculosis y otros oportunistas10.
En esta cohorte analizada, el tratamiento con corticoides se asoció con aumento estadísticamente significativo del riesgo de infecciones. Este hallazgo coincide con los distintos registros norteamericanos (CORRONA) y europeos (BSRBR Y RABBIT), que muestran un aumento del riesgo entre 1,5 y 2 veces, incluso cuando se emplean bajas dosis (prednisona 5 mg/día) y cinco veces mayor con el uso de prednisona superior a 15-20 mg/día6. Asimismo, cada incremento de la dosis de corticoides multiplicó el riesgo de sufrir una infección grave, siendo la dosis media de 7,5 mg/día12,16. Si bien en el presente estudio, la dosis «segura» de corticoides se estimó en 6,25 mg/día, la diferencia no fue estadísticamente significativa, hecho que puede atribuirse a la pérdida de datos de la dosis recibida y al tamaño muestral.
En esta serie se encontraron diferencias significativas en la frecuencia de infecciones en relación con el fármaco inmunosupresor sintético recibido.
Un hallazgo a destacar es el riesgo aumentado asociado a metotrexate, acorde con lo reportado en la literatura. En el registro CORRONA se demostró mayor riesgo de infecciones en pacientes tratados con metotrexate que con otros fármacos modificadores de la enfermedad sintéticos. Sin embargo, un metaanálisis publicado en el 2017, que compara el riesgo de infecciones con terapias biológicas y biológicas asociadas a metotrexate, no muestra diferencias significativas entre ambos grupos26. Una posible explicación a esta controversia es que el metotrexate es el fármaco que se asocia con mayor frecuencia a las terapias biológicas en pacientes con AR, además de su uso combinado con otros inmunosupresores sintéticos.
Con respecto al riesgo de infecciones asociado al uso de micofenolato, no debe considerarse en forma aislada un efecto del mismo, ya que habitualmente se utiliza en pacientes con LES grave, mayor actividad de la enfermedad, compromiso de órganos mayores y asociado a otros fármacos como los corticoides.
La hidroxicloroquina presenta propiedades antimicrobianas, además de su rol inmunomodulador. Varios estudios señalan el uso de HCQ en EAS como un factor protector del desarrollo de infecciones16,22,23. En esta cohorte se vio que el uso de hidroxicloroquina, al igual que de sulfasalazina, disminuye en más de un 50% el riesgo de infecciones en pacientes con AR.
Este estudio tiene varias limitaciones, en primer lugar, las derivadas del diseño retrospectivo con un sesgo de información, y a la existencia de categorías con baja frecuencia (lo cual dificulta el análisis estadístico, sobre todo en las infecciones oportunistas). Al igual que en la mayoría de las series, el subregistro de infecciones no graves es debido a que es un motivo de consulta resuelto en otros centros de asistencia no especializados en EAS (sesgo de información). Otras limitaciones son la ausencia de datos microbiológicos en todos los casos, dificultades en el registro de la dosis acumulada de corticoides y tiempos de administración, así como datos de inmunizaciones. Dentro de las fortalezas, los autores señalan el número de pacientes incluidos, amplitud de las patologías autoinmunes y, fundamentalmente, que se trata del primer estudio nacional de infecciones en pacientes con EAS.
Todo esto constituye una motivación para el desarrollo de nuevos estudios con carácter prospectivo e instrumentación de medidas para la disminución de la frecuencia de infecciones en esta población, como el uso de protocolos de cribado y profilaxis de infecciones en pacientes con EAS antes del inicio de tratamientos inmunosupresores.
ConclusionesLas infecciones son una complicación frecuente en pacientes con EAS, vinculadas a la enfermedad en sí misma y a los tratamientos indicados, fundamentalmente corticoides y biológicos. La identificación y el tratamiento oportuno de las mismas, junto con el uso racional de los fármacos pueden reducir su impacto en esta población.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.